Một mảnh đồng có khối lượng 12,8g cho tác dụng với lượng dư dd H2SO4 đặc, có đun nóng. cô cạn dd sau phản ứng thu được 28g muối khan. Tính hiệu suất của phản ứng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi x, y, z là số mol Fe, Mg, Cu
=> \(56x+24y+64z=24,8\) (1)
X+ H2SO4 đặc nóng
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
Mg + 2H2SO4→ MgSO4 + SO2↑ + 2H2O.
Cu + 2H2SO4→ CuSO4 + SO2↑ + 2H2O.
Các muối là \(Fe_2\left(SO_4\right)_3,MgSO_4,CuSO_4\)
=> \(n_{Fe_2\left(SO_4\right)_3}=\dfrac{n_{Fe}}{2}=\dfrac{x.}{2};n_{MgCl_2}=n_{Mg}=y;n_{CuCl_2}=n_{Cu}=z\)
=> \(\dfrac{400x}{2}+120y+160z=132\) (2)
X + HCl dư thu được khí là H2
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
=> x+y=0,5 (mol) (3)
Từ (1), (2), (3) => x, y ,z
Xem lại đề vì hệ vô nghiệm

a, Ta có: \(n_{CH_3COOH}=\dfrac{9,6}{60}=0,16\left(mol\right)\)
PT: \(Mg+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+H_2\)
Theo PT: \(n_{\left(CH_3COO\right)_2Mg}=\dfrac{1}{2}n_{CH_3COOH}=0,08\left(mol\right)\)
\(\Rightarrow m_{\left(CH_3COO\right)_2Mg}=0,08.142=11,36\left(g\right)\)
b, PT: \(CH_3COOH+C_2H_5OH\underrightarrow{t^o,xt}CH_3COOC_2H_5+H_2O\)
Theo PT: \(n_{CH_3COOC_2H_5\left(LT\right)}=n_{CH_3COOH}=0,16\left(mol\right)\)
\(\Rightarrow m_{CH_3COOC_2H_5\left(LT\right)}=0,16.88=14,08\left(g\right)\)
Mà: thực tế thu được 10,56 (g)
\(\Rightarrow H\%=\dfrac{10,56}{14,08}.100\%=75\%\)

\(n_{Cl_2}=\dfrac{2,1168}{22,4}=0,0945\left(mol\right)\)
=> nCl(muối) = 0,39 - 0,0945 = 0,201 (mol)
=> nAgCl = 0,201 (mol)
=> mAgCl = 0,201.143,5 = 28,8435 (g)

Do A, B là hợp chất hữu cơ đơn chức, có khả năng tác dụng với NaOH
=> trong phân tử A,B chứa 2 nguyên tử oxi
=> MA = MB = 32 . 100/21,621= 148 g/mol
=> CTPT của A,B là C9H8O2 .
TN1: nA + nB = 0,74/148=5.10-3
Mà m sản phẩm=1,54
=> cả A,B đều có khả năng tham gia phản ứng cộng với dung dịch Br2 theo tỉ lệ mol 1:1
=> A,B chứa 1 nối đôi C=C trong phân tử ( không phải este của phenol)
TN5: Do A,B bị oxi hóa bởi KMnO4 tạo ra C7H8O2 và CO2 => A,B chứa vòng benzen
TN2: nA + nB= 2,22/148=0,015 mol
Do hỗn hợp X có khả năng tác dụng với NaHCO3 => hỗn hợp có chứa axit
=> naxit= nCO2 = 5.10-3 => neste= 0,01 mol
TN3: trong 4,44 gam hỗn hợp naxit = 0,01 mol, neste= 0,02
=> mmuối sinh ra từ este = 4,58 – 0,01 . MC8H7COONa= 2,88
=> Mmuối sinh ra từ este = 144 g/mol.
=> CT muối sinh ra từ este là: C6H5COONa
=> CTCT A,B là: C6H5COOC2H3 và C6H5-CH=CH-COOH
=> ( loại trường hợp axit có CT C6H5-C(COOH)=CH2 vì axit này không bị oxi hóa tạo C6H5COONa và CO2)
PTHH:
C6H5COOC2H3+ 2KMnO4 +3 H2SO4 → C6H5COOH + 2CO2 + K2SO4 + 2MnSO4 + 4H2O
C6H5-CH=CH-COOH +2 KMnO4 + 3H2SO4 →C6H5COOH + 2CO2 + K2SO4 + 2MnSO4 + 4H2O.

Đáp án A
X là este có dạng: ROOC-R'(NH2)-COOR
Số mol của olefin = 0,03 à Số mol của anol = 0,04 (nol) à Mancol = 46.
Số mol của X = 0,02 (mol) à Chất rắn Z gồm:
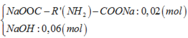
à Khối lượng của muối hữu cơ = 3,82 gam à Mmuối = 191 à R' = 41 −C3H5)
Cho Z tác dụng với HCl dư thu được chất rắn khan R gồm:
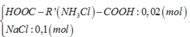
à mchất rắn = 183,5.0,02 + 58,5.0,1 = 9,52 (gam)

PTHH: Mg + H2SO4 ===> MgSO4 + H2
Zn + H2SO4 ===> ZnSO4 + H2
Ta có: nH2 = \(\frac{6,72}{22,4}=0,3\left(mol\right)\)
=> mH2 = 0,3 x 2 = 0,6 (gam)
Theo PTHH, ta thấy nH2SO4 = nH2 = 0,3 (mol)
=> mH2SO4 = 0,3 x 98 = 29,4 (gam)
Áp dụng định luật bảo toàn khối lượng, ta có:
mmuối khan = mkim loại + mH2SO4 - mH2 = 11,3 + 29,4 - 0,6 = 40,1 (gam)

\(n_{Cu}=0,2\left(mol\right)\)
\(Cu+2H_2SO_4\left(đ,đ\right)\underrightarrow{t^0}CuSO_4+SO2+2H_2O\)
\(0,2\) \(0,2\)
\(m_{CuSo_4}=32\left(g\right)\)
Mà thực tế : \(m_{CuSO_4}=28\left(g\right)\)
\(\Rightarrow H=87,5\%\)