Cho m gam muối cacbonat của dung dịch M phản ứng vừa đủ vs 140 dd H2SO4
9,8% thu được dd X. Cô cạn X thu được 19,04g chất rắn khan. XĐ công thức của muối
Giúp mình vs
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{XCl_3}=\dfrac{a}{M_X+106,5}\left(mol\right)\)
PTHH: 2X + 6HCl --> 2XCl3 + 3H2
=> \(n_X=\dfrac{a}{M_X+106,5}\left(mol\right)\)
\(n_{X_2\left(SO_4\right)_3}=\dfrac{b}{2.M_X+288}\left(mol\right)\)
PTHH: 2X + 3H2SO4 --> X2(SO4)3 + 3H2
=> \(n_X=\dfrac{b}{M_X+144}\left(mol\right)\)

Đáp án là A
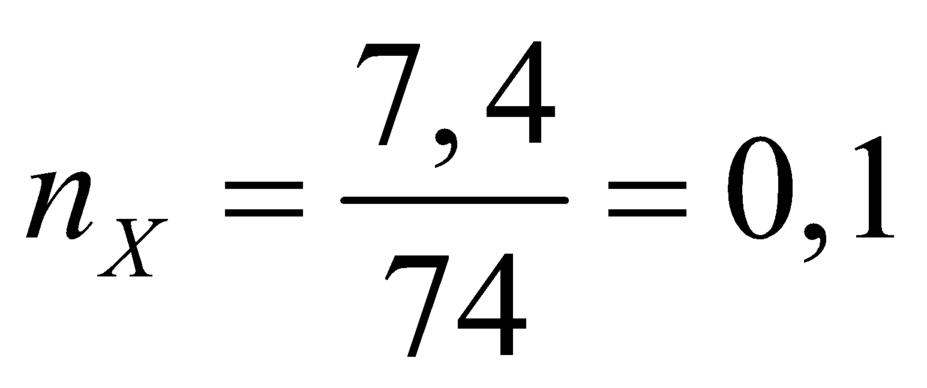
Chất rắn khan sau phản ứng là muối
nmuối= ![]()
Mmuối 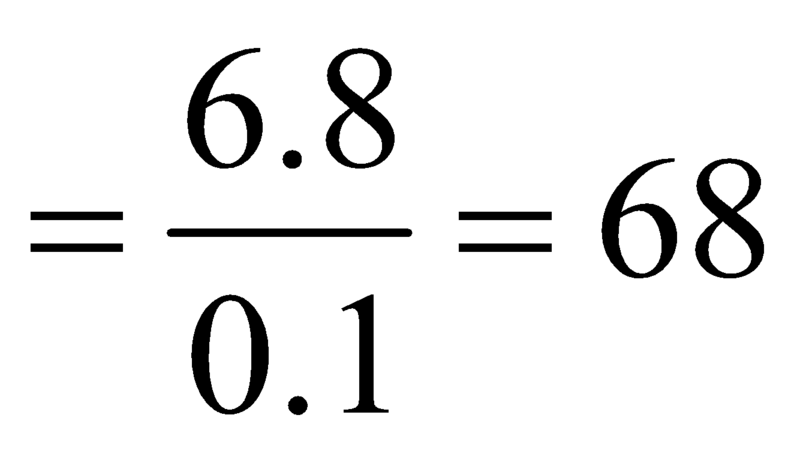
![]() Muối là cần tìm :HCOONa
Muối là cần tìm :HCOONa
![]() công thức X : HCOOC2H5
công thức X : HCOOC2H5

Đáp án D.
Ta có: nAxit glutamic = 0,09 mol, nHCl = 0,2 mol
⇒ ∑nCOOH + H+ = 0,09×2 + 0,2 = 0,38 mol.
+ nNaOH = 0,34 mol < ∑nCOOH + H+ = 0,38 mol
⇒ nH2O tạo thành = 0,38 mol.
Bảo toàn khối lượng ta có:
mChất rắn = 13,23 + 0,2×36,5 + 0,4×40 – 0,38×18 = 29,69 gam.

Phản ứng xảy ra:
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Có:
\(m_{\text{muối}}=m_{kl}+m_{Cl}\rightarrow32,65=14,9+m_{Cl}\)
\(\rightarrow m_{Cl}=17,75g\rightarrow n_{Cl}=0,5mol=n_{HCl}\)
\(\rightarrow m_{HCL}=0,5.36,5=18,25g\)
\(\rightarrow m=m_{ddHCl}=\frac{18,25}{10\%}=182,5g\)

Theo định luật bảo toàn khối lượng ta có:
m 3 o x i t + m H 2 S O 4 = m m u ố i + m H 2 O s a n p h a m
⇔ m m u ố i = m 3 o x i t + m H 2 S O 4 - m H 2 O s a n p h a m
Mà n H 2 O san pham = n H 2 S O 4 = 1.0,05 = 0,05 mol
⇒ m m u o i = 2,8 + 0,05.98 - 0,05.18 = 6,8g
⇒ Chọn C.
\(n_{H_2SO_4}=\dfrac{140\cdot9.8\%}{98}=0.14\left(mol\right)\)
\(M_2\left(CO_3\right)_n+nH_2SO_4\rightarrow M_2\left(SO_4\right)_n+nCO_2+nH_2O\)
\(................0.14.......\dfrac{0.14}{n}\)
\(M_{Muối}=\dfrac{19.04}{\dfrac{0.14}{n}}=136n\)
\(\Rightarrow2M+96n=136n\)
\(\Rightarrow M=20n\)
\(BL:n=2\Rightarrow M=40\)
\(CT:CaCO_3\)