1 hỗn hợp gồm BaSO4 và Fe(OH)3 nặng 100g. nhiệt phân đến khối lượng không đổi thấy hỗn hợp giảm 3,6g . tính thành phần phần trăm khối lượng các chất rắn ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{Mg\left(OH\right)_2}=a\left(mol\right)\)
\(n_{Fe\left(OH\right)_3}=b\left(mol\right)\)
\(m_{hh}=58a+107b=16.9\left(g\right)\left(1\right)\)
\(Mg\left(OH\right)_2\underrightarrow{^{^{t^0}}}MgO+H_2O\)
\(a.............a\)
\(2Fe\left(OH\right)_3\underrightarrow{^{^{t^0}}}Fe_2O_3+3H_2O\)
\(b.............\dfrac{b}{2}\)
\(m_{Cr}=40a+160\cdot\dfrac{b}{2}=12.4\left(g\right)\left(1\right)\)
\(\left(1\right),\left(2\right):a=0.07,b=0.12\)
\(\%m_{Mg\left(OH\right)_2}=\dfrac{0.07\cdot40}{16.9}\cdot100\%=16.57\%\)
\(\%m_{Fe\left(OH\right)_3}=83.43\%\)

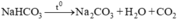
Gọi y, x lần lượt là số mol NaHCO3 và Na2CO3
Theo bài ra ta có hệ
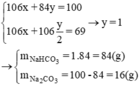
Thành phần % theo khối lượng các chất
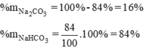

Đáp án C
![]()
Các phản ứng nhiệt phân:
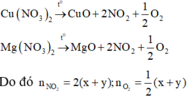
Khối lượng chất rắn giảm chính là khối lượng của NO2 và O2. Có
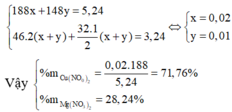

Gọi số mol KMnO4, KClO3 là a, b
=> 158a + 122,5b = 49,975
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
_______a----------------------------------->a
2KClO3 --to--> 2KCl + 3O2
_b---------------------->1,5b
mO2 = mgiảm = 10,4
=> \(n_{O_2}=\dfrac{10,4}{32}=0,325\left(mol\right)\)
=> 0,5a + 1,5b = 0,325
=> a = 0,2; b = 0,15
=> \(\left\{{}\begin{matrix}\%KMnO_4=\dfrac{0,2.158}{49,975}.100\%=63,23\%\\\%KClO_3=\dfrac{0,15.122,5}{49,975}.100\%=36,77\%\end{matrix}\right.\)

Gọi $n_{KMnO_4} = a(mol) ; n_{KClO_3} = b(mol) \Rightarrow 158a + 122,5b = 49,975(1)$
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
$2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
$m_{O_2} = m_{giảm} = 4(gam)$
$\Rightarrow n_{O_2} = 0,5a + 1,5b = \dfrac{4}{32} = 0,125(2)$
Từ (1)(2) suy ra a = 0,339 ; b = -0,029 < 0
(Sai đề)