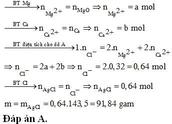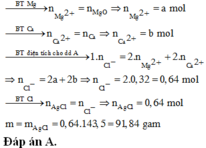Cho 38,775g hỗn hợp bột Al và AlCl3 vào lượng vừa đủ dung dịch NaOH thu được dung dịch A ( kết tủa vừa tan hết) và 6,72 lít khí H2 đktc.Thêm 250ml dung dịch HCl vào dung dịch A thu được 21,84g kết tuat.Nồng độ CM dung dịch HCl
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, \(2Al+6HCl\rightarrow2AlCl_3+3H_2\) (1)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\) (2)
\(n_{HCl}=0,45.2=0,9\left(mol\right)\), \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT (1): \(n_{Al}=\dfrac{2}{3}n_{H_2}=0,2\left(mol\right)\)
\(n_{HCl\left(1\right)}=2n_{H_2}=0,6\left(mol\right)\) \(\Rightarrow n_{HCl\left(2\right)}=0,9-0,6=0,3\left(mol\right)\)
Theo PT: \(n_{Al_2O_3}=\dfrac{1}{6}n_{HCl\left(2\right)}=0,05\left(mol\right)\)
\(\Rightarrow m=m_{Al}+m_{Al_2O_3}=10,5\left(g\right)\)
b, Theo PT (1) + (2): \(n_{AlCl_3}=n_{Al}+2n_{Al_2O_3}=0,3\left(mol\right)\)
Ta có: \(n_{NaOH}=0,5.2=1\left(mol\right)\)
PT: \(AlCl_3+3NaOH\rightarrow Al\left(OH\right)_{3\downarrow}+3NaCl\)
_____0,3_______0,9________0,3 (mol)
\(Al\left(OH\right)_3+NaOH\rightarrow NaAlO_2+2H_2O\)
___0,1________0,1 (mol)
- Hiện tượng: Xuất hiện kết tủa keo trắng, sau đó kết tủa bị hòa tan 1 phần.
\(\Rightarrow n_{Al\left(OH\right)_3}=0,3-0,1=0,2\left(mol\right)\Rightarrow m_{Al\left(OH\right)_3}=0,2.78=15,6\left(g\right)\)

\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH:
`Mg + 2HCl -> MgCl_2 + H_2`
`2Al + 6HCl -> 2AlCl_3 + 3H_2`
`MgCl_2 + 2NaOH -> Mg(OH)_2 + 2NaCl`
`AlCl_3 + 3NaOH -> Al(OH)_3 + 3NaCl`
Theo PTHH: `n_{NaOH} = n_{-Cl} = 2n_{H_2} = 0,4 (mol)`
`=> V = (0,4)/(0,25) = 1,6M`

Đáp án D
► Bảo toàn electron: 3nAl = 2nH2 ⇒ nAl = 0,02 mol.
"vừa đủ" ⇒ X chỉ chứa AlCl3 || 0,09 mol hay 0,13 mol NaOH cho cùng 1 lượng ↓
⇒ 0,09 mol NaOH thì ↓ chưa đạt cực đại và 0,13 mol NaOH thì ↓ bị hòa tan 1 phần.
⇒ n↓ = 0,09 ÷ 3 = 0,03 mol. ||► Mặt khác, khi bị hòa tan 1 phần thì:
nOH– = 4nAl3+ – n↓ ⇒ nAl3+ = (0,03 + 0,13) ÷ 4 = 0,04 mol.
Bảo toàn nguyên tố Al: nAl2O3 = 0,01 mol ||⇒ m = 1,56(g)

Đáp án D
► Bảo toàn electron: 3nAl = 2nH2 ⇒ nAl = 0,02 mol.
"vừa đủ" ⇒ X chỉ chứa AlCl3 || 0,09 mol hay 0,13 mol NaOH cho cùng 1 lượng ↓
⇒ 0,09 mol NaOH thì ↓ chưa đạt cực đại và 0,13 mol NaOH thì ↓ bị hòa tan 1 phần.
⇒ n↓ = 0,09 ÷ 3 = 0,03 mol. ||► Mặt khác, khi bị hòa tan 1 phần thì:
nOH– = 4nAl3+ – n↓ ⇒ nAl3+ = (0,03 + 0,13) ÷ 4 = 0,04 mol.
Bảo toàn nguyên tố Al: nAl2O3 = 0,01 mol ||⇒ m = 1,56(g)

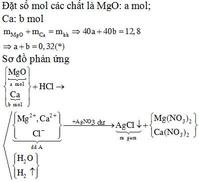
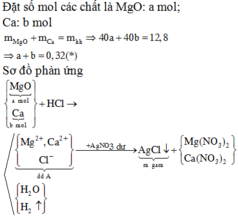
Gọi n lá hóa trị của M
Gọi $n_{Fe} = a(mol) ; n_M = b(mol)$
$\Rightarrow 56a + Mb = 10,4(1)$
$Fe + 2HCl \to FeCl_2 + H_2$
$2M + 2nHCl \to 2MCl_n + nH_2$
Theo PTHH :
$n_{H_2} = a + 0,5bn = \dfrac{6,72}{22,4} = 0,3(2)$
Bảo toàn nguyên tố với Fe,M
$n_{Fe_2O_3} = 0,5a(mol)$
$n_{M_2O_n} = 0,5b(mol)$
Ta có :
0,5a.160 + 0,5b(2M + 16n) = 16(3)
Từ (1)(2)(3) suy ra a = 0,1 ; Mb = 4,8 ; bn = 0,4 => b = 0,4/n
Suy ra :
$M = Mb : b = 4,8 : 0,4/n = 12n$
Với n = 2 thì M = 24(Magie)
$n_{FeCl_2} = a = 0,1(mol)$
$n_{MgCl_2} = n_{Mg} = 0,4 : n = 0,4 : 2 = 0,2(mol)$
Vậy :
$m_{FeCl_2} = 0,1.127 = 12,7(gam)$
$m_{MgCl_2} = 0,2.95 = 19(gam)$

Đáp án : D
.nX = 0,3 mol ; nZ = 0,2 mol
Chỉ có NO phản ứng với O2 tạo NO2 bị hấp thụ vào nước
=> nNO = 0,3 – 0,2 = 0,1 mol
MZ= 40g (Z gồm N2 và N2O )
=> nN2 = 0,05 mol ; nN2O = 0,15 mol
.m(g) P : Mg,Al -> Kết tủa lớn nhất : Mg(OH)2 ; Al(OH)3 : (m + 39,1)g
=> mOH = (m + 39,1) – m = 39,1g => nOH = 2,3 mol = 2nMg + 3nAl
Lại có : nMg : nAl = 4 : 5 => nMg = 0,4 mol ; nAl = 0,5 mol
Bảo toàn e : 2nMg + 3nAl = 10nN2 + 8nN2O + 3nNO + 8nNH4NO3
=> nNH4NO3 = 0,0375 mol
=> Bảo toàn N : nHNO3 pứ = 2nMg + 3nAl + 2nN2 + nNO + 2nN2O + 2nNH4NO3
=> nHNO3 pứ = 2,875 mol
=> nHNO3 đầu = 3,45 mol => mdd HNO3 = 1086,75g
=> mdd sau = mP + mdd HNO3 - mkhí = 1098,85g
=> %CAl(NO3)3 = 9,69%