Cho a mol kim loại R tan vừa hết trong đ chứa a mol H2SO4 thì thu được 1,56g muối và 1 khí A. Hấp thụ hoàn toàn khí A vào 45ml dd NaOH 0,2M thì thấy tạo thành 0,608g muối. Tìm R
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có:
\(n_{CO_2}=\frac{1.12}{22.4}=0.05\left(mol\right)\) \(\Rightarrow m_{CO_2}=0.05\times44=2.2\left(g\right)\)
\(X_2CO_3+2HCl\rightarrow2XCl+H_2O+CO_2\)
\(YCO_3+2HCl\rightarrow YCl_2+H_2O+CO_2\)
Ta thấy
\(n_{HCl}=2n_{CO_2}=2\times0.05=0.1\left(mol\right)\)
\(\Rightarrow\) \(m_{HCl}=0.1\times36.5=3.65\left(g\right)\)
\(n_{H_2O}=n_{CO_2}=0.05\left(mol\right)\)
\(\Rightarrow\) \(m_{H_2O}=0.05\times18=0.9\left(g\right)\)
Áp dụng định luật bảo toàn khối lượng ta được:
\(m_{XCl+YCl_2}=\left(5.95+3.65\right)-\left(2.2+0.9\right)=9.6-3.1=6.5\left(g\right)\)

a)
4FeCO3 + O2 --> 2Fe2O3 + 4CO2 (1)
4FexOy + (3x-2y)O2 --> 2xFe2O3 (2)
CO2 + Ba(OH)2 → BaCO3 + H2O (3)
2CO2 + Ba(OH)2 → Ba(HCO3)2 (4)
b)
Giả sử Ba(OH)2 dư , chỉ xảy ra (3) không xảy ra pư (4)
nBaCO3 = 0,02 mol = nCO2
=> nFe2O3 (1) = 0,01 mol
Mà \(\Sigma\)nFe2O3 (1) + (2) = \(\dfrac{11,2}{160}\)= 0,07 mol => nFe2O3 (2) = 0,07 -0,01 = 0,06 mol
=> nFexOy = \(\dfrac{0,12}{x}\) mol
mFexOy = 12,64 - mFeCO3 = 12,64 - 0,02.116 = 10,32 gam
=> M FexOy = 86x (g/mol)
Với x = 1,2,3 ... đều không thỏa mãn
=> Ba(OH)2 phản ứng hết, xảy ra cả phản ứng (3) và (4)
nBa(OH)2 = 0,03 mol , nBaCO3 = 0,02 mol
=> nBa(OH)2 (4) = 0,03 - 0,02 = 0,01 mol
=> nCO2 (4) = 0,01.2 = 0,02 mol
=> nCO2 (1) = nCO2 (3) + nCO2 (4) = 0,04 mol
<=> nFe2O3 (1) = 0,02 mol , nFeCO3 = 0,04 mol
=> nFe2O3 (2) = 0,07 - 0,02 = 0,05 mol <=> n FexOy = \(\dfrac{0,1}{x}\) mol
mFexOy = 12,64 - mFeCO3 = 12,64 - 0,04.116 = 8 gam
=> M FexOy = 80x (g/mol)
với x = 2 => mFexOy = 160 (g/mol) <=> Fe2O3

Đáp án C
Pt pư:
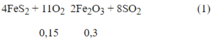
Ta có: nBaC03 = 0,15 mol
nKOH = 0,1 mol ⇒ nBa2+ = 0,15 mol ; nOH- = 0,4 mol
Khi cho SO2 vào dung dịch Y thu được 21,7 (g) BaSO3. Cho Y tác dụng với dung dịch NaOH thấy xuất hiện thêm kết tủa, chứng tỏ trong dung dịch Y có ion HSO3-.
Vì: Ba2+ + HSO3- + OH- " BaSO3 + H2O
Ta có: nBaC03 = 0,1 mol
Ptpứ:
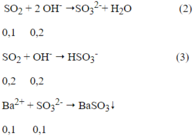
Ta có: nOH- = 0,4 - 0,2 = 0,2 mol
Theo ptpư (2), (3) ta có: n SO2= 0,1 + 0,2 = 0,3 mol
Theo ptpư (1) ta có: n FeS2 = ½ n SO2= 0,15 mol ⇒ m FeS2 = 120.0,15 = 18(g)

Chọn B.
Theo đề ta có: n O 2 = 1 , 225 ; n C O 2 = 1 , 05 v à n H 2 O = 1 , 05 => X no, đơn chức, mạch hở (vì n C O 2 = n H 2 O )
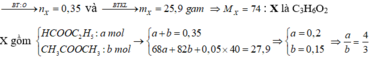

Ta có: số hạt (p,n,e ) trong X là 93 .
\(\Rightarrow\dfrac{93}{3,2222}\le p\le\dfrac{93}{3}\)
\(\Leftrightarrow\left[{}\begin{matrix}p=29\\p=30\\p=31\end{matrix}\right.\)
=> X có hóa trị II
Hỗn hợp A: \(\left\{{}\begin{matrix}Al:a\left(mol\right)\\X:b\left(mol\right)\end{matrix}\right.\)
\(2Al\left(a\right)+6H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Al_2\left(SO_4\right)_3+3SO_2\left(1,5a\right)+6H_2O\)
\(X\left(b\right)+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}XSO_4+SO_2\left(b\right)+2H_2O\)
\(SO_2\left(1,5a+b\right)+2NaOH\rightarrow Na_2SO_3\left(1,5a+b\right)+H_2O\)
\(n_{Na_2SO_3}=0,4\left(mol\right)\)
\(\Rightarrow1,5a+b=0,4\left(I\right)\)
Khi thêm vào A một lượng kim loại X bằng 2 lần lượng kim loại X có trong A ( giữ nguyên lượng Al )
rồi hoà tan bằng H2SO4 đăc nóng thì lượng muối trong dung dịch mới tăng thêm 32g so với muối trong dung dịch B
\(X\left(2b\right)+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}XSO_4\left(2b\right)+SO_2+2H_2O\)
\(\Rightarrow2b\left(X+96\right)=32\left(II\right)\)
Khi giảm một nửa lượng Al có trong A ( giữ nguyên lượng X ) thì khi hoà tan ta thu được là 5,6 lít khí (đktc ) khí C .
\(2Al\left(0,5a\right)+6H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Al_2\left(SO_4\right)_3+3SO_2\left(0,75a\right)+6H_2O\)
\(X\left(b\right)+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}XSO_4+SO_2\left(b\right)+2H_2O\)
\(n_{SO_2}=0,25\left(mol\right)\)
\(\Rightarrow0,75a+b=0,25\left(III\right)\)
Từ \(\left(I\right)\&\left(III\right)\Rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
Thay vào \(\left(II\right)\Rightarrow X=64\left(Cu\right)\)
Suy ra % về khối lượng các kim loại trong A .
Nếu đề cho X có hóa trị = bao nhiêu thì quá dễ dàng.
Còn nếu ko cho thì vs bài này mk sẽ xét 3 tường hợp: a = 1;2;3.
Mặc dù hơi dài nhưng sẽ ra.