có ai biết giải bài này k mình đang cần rất gấp mong các bạn giúp cho
Bài 1: cho 5,6g oxit của kim loại hóa trị (II) vào nước thu đc 200g dd bazo với nồng độ 3,7%. hãy xác định công thức của oxit trên.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi CTHH của oxit kim loại là RO
\(m_{R\left(OH\right)_2}=8,55\%.200=17,1\left(g\right)\)
Áp dụng định luật BTKL ta có: \(m_{H_2O}=17,1-15,3=1,8\left(g\right)\Rightarrow n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\)
PTHH: RO + H2O → R(OH)2
Mol: 0,1 0,1
\(\Rightarrow M_{RO}=\dfrac{15,3}{0,1}=153\left(g/mol\right)\)
⇒ MR = 153 - 16 = 137 (g/mol)
Vậy R là nguyên tố bari (Ba)

Bài 1:
Gọi A là kim loại hóa trị II cần tìm
\(n_{H_2}=\dfrac{0,28}{22,4}=0,0125\left(mol\right)\\ A+2HCl\rightarrow ACl_2+H_2\\ n_A=n_{H_2}=0,0125\left(mol\right)\\ M_A=\dfrac{0,3}{0,0125}=24\left(\dfrac{g}{mol}\right)\)
Vậy: Kim loại A(II) cần tìm là Magie (Mg=24)
Bài 2:
- Chỉ có Zn tác dụng với dd HCl dư chứ Cu thì không.
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{Zn}=n_{H_2}=0,2\left(mol\right)\\ \rightarrow m_{Zn}=0,2.65=13\left(g\right)\\ \rightarrow m_{Cu}=15-13=2\left(g\right)\\ Vậy:m=2\left(g\right)\)

đặt công thức oxit cần tìm là: XO
mX(OH)2= C%*mdd/100=8.55*200/100=17.1g
áp dụng bảo toàn khối lượng: mH2O=17.115.3=1.8g =>nH2O=1.8/18=0.1mol
pt: XO + H2O--> X(OH)2
0.1 0.1
MXO=15.3/0.1=153 g/mol
=> MX= MXO - MO2= 153-16=137
Vậy X là Ba. CTHH của oxit là BaO
Chúc em học tốt!!!:))

goi cthh cua oxit hoa tri 2 la MO
MO+H2SO4->MSO4+H2O
goi khoi luong dd H2SO4 la Q ta co
mH2SO4=Q.4,9/100=0,049Q
=nH2SO4=0,049Q/98=0,0005Q
THEO PT nMSO4=nH2SO4=0,0005Q
theo pt nh2s04=nMO=0,0005Q
=>mMSO4=[M+96].0,0005Q=0,0005QM+0,048Q
mddMSO4=[0,0005QM+0,048Q].100/5,78=0,00865QM+0,8304Q[2]
MẶT KHÁC mdd sau pu =Q+0,0005Q[M+16][ 1]
TU 1 va 2 tasuy RA
này bn ơi chỗ này mình làm r nhưng ko bít đúng ko

Cách 1: Đặt công thức hoá học của oxit là MO ⇒ công thức bazơ là M OH 2
MO + H 2 O → M OH 2
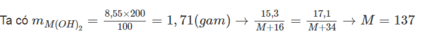
→ Công thức oxit là BaO.
Cách 2: m H 2 O ( p / u ) = m M OH 2 - m MO = 17,1 - 15,3 = 1,8(g)
MO + H 2 O → M OH 2
![]()
Công thức oxit là BaO

Gọi CTHH của oxit kim loại hóa trị II là MO
MO + H2O ------> M(OH)2
\(\frac{15,3}{M+16}\) --------------> \(\frac{15,3}{M+16}\)(mol)
C%(dd bazơ) =[\(\frac{15,3}{M+16}\).(M+34)] : 200 . 100% = 8,55%
=> Giải pt ta được: M=137 (g/mol)
=> M là Ba (Bari)
PTHH: \(RO+H_2O\rightarrow R\left(OH\right)_2\)
Theo PTHH: \(n_{RO}=\dfrac{5,6}{R+16}\left(mol\right)=n_{ROH}\)
\(\Rightarrow\dfrac{\dfrac{5,6}{R+16}\cdot\left(R+34\right)}{200}=0,037\) \(\Leftrightarrow R=40\) (Canxi)
Vậy CTHH của oxit là CaO
cảm ơn bạn 1 lần nữa nhé