Cho 3,36 lít khí SO2 vào 150g dung dịch NaOH 20% sau phản ứng thu được dung dịch X.Tính C% các chất trong dung dịch X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Số mol SO2 và NaOH lần lượt là 0,2 và 0,25.
1 < OH-/SO2=1,25 < 2 ⇒ Dung dịch X chứa hai muối Na2SO3 và NaHSO3.
\(n_{Na_2SO_3}=0,25-0,2=0,05\left(mol\right)\) ⇒ \(n_{NaHSO_3}=0,2-0,05=0,15\left(mol\right)\).
1. Khối lượng muối có trong X:
m=0,05.126+0,15.104=21,9 (g).
2. Nồng độ mol/l các chất trong X:
\(C_{M\left(Na_2SO_3\right)}\)=0,05/0,2=0,25 (mol/l).
\(C_{M\left(NaHSO_3\right)}\)=0,15/0,2=0,75 (mol/l).
3. Khối lượng kết tủa BaSO3 là:
m'=0,2.217=43,4 (g).

X + NaOH ⟶3/2 H2; nA1 = 0,02
CO2 + NaAlO2 + H2O ⟶ NaHCO3 + Al(OH)3
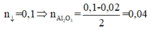
⇒ m = 10,26g
Đáp án A
\(n_{SO_2}=\frac{3,36}{22,4}=0,15\left(mol\right)\)
\(m_{NaOH}=\frac{20.150}{100}=30\left(g\right)\)
=>\(n_{NaOH}=\frac{30}{40}=0,75\left(mol\right)\)
Ta thấy: \(\frac{n_{NaOH}}{n_{SO_2}}=\frac{0,75}{0,15}=5>2\)
=>SO2 tác dụng với dd NaOH tạo ra muối Na2SO3
\(SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\)
0,15___0,3_______0,15
So sánh tỉ lệ:
\(\frac{n_{SO_2}}{1}< \frac{n_{NaOH}}{2}\Leftrightarrow\frac{0,15}{1}< \frac{0,75}{2}\)
=>NaOH dư
=>\(n_{NaOH\left(dư\right)}\)=0,75-0,3=0,45(mol)
=>\(m_{NaOH\left(dư\right)}=0,45.40=18\left(g\right)\)
mdd=\(m_{SO_2}+m_{ddNaOH}=0,15.64+150=159,6\left(g\right)\)
\(m_{Na_2SO_3}=0,15.126=18,9\left(g\right)\)
\(C\%_{Na_2SO_3}=\frac{18,9.100}{159,6}\approx11,84\%\)
\(C\%_{NaOH\left(dư\right)}=\frac{18.100}{159.6}=11,28\%\)