Trong hợp kim Al – Mg, cứ có 9 mol Al thì có 1 mol Mg. Thành phần phần % khối lượng của hợp kim là ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Mg ko pư vs HCl
Gọi số mol của Fe là a(a>0)
=> nAl= 2a(mol)
nMg = 3/2 a (mol)
nH2=49,28/22,4=2,2(mol)
PTHH
Fe + 2HCl ------> FeCl2 + H2
a a (mol)
2Al + 6HCl ------> 2AlCl3 + 3H2
2a 3a (mol)
=> nH2 = a+3a=4a=2,2(mol)
=> a=0,55 = nFe
=> nAl = 2a = 1,1 ( mol)
nMg = 0,825 ( mol)
%mFe = ( 0,55.56)/(0,55.56 + 1,1.27 + 0,825.24) . 100% = 38,35 %
%mAl =(1,1.27)/(0,55.56 + 1,1.27 + 0,825.24) . 100% = 37%
%mMg = 100% - %mFe - %mAl = 100% -38,36%-37% = 24,65%
( kết quả có thể khác , bn tự lm lại theo hướng này )
#Học-tốt

\(\%m_{Al}=\dfrac{27.10}{27.10+59.1}.100\approx82\%\\ \Rightarrow\%m_{Ni}\approx18\%\\ \Rightarrow B\)

1,a,Gọi \(n_{Al}=a\left(mol\right)\rightarrow n_{Mg}=0,5a\left(mol\right)\)
\(\rightarrow27a+24.0,5b=7,8\\ \Leftrightarrow a=0,2\left(mol\right)\\ \rightarrow\left\{{}\begin{matrix}n_{Al}=0,2\left(mol\right)\\n_{Mg}=0,1\left(mol\right)\end{matrix}\right.\)
b, \(\rightarrow\left\{{}\begin{matrix}m_{Al}=0,2.27=5,4\left(g\right)\\m_{Mg}=0,1.24=2,4\left(g\right)\end{matrix}\right.\)
2, \(n_{O_2}=\dfrac{0,16}{32}=0,005\left(mol\right)\)
PTHH: 2HgO --to--> 2Hg + O2
0,01<- 0,05
\(\rightarrow m_{Hg}=0,01.201=2,01\left(g\right)\)

Đáp án B.
Khối lượng Al là mAl = 27 x 10 = 270 (g)
Khối lượng Ni là mNi= 59 . 1 = 59 (g)
Khối lượng hỗn hợp mhh = mAl + mNi = 270 + 59 = 329 (g)
Thành phần % theo khối lượng
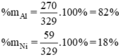

a,gọi mol Al là x(mol)====> nMg=1/2 x( mol)
ta có: mhh= 7,8= 27x+ \(\frac{1}{2}x.24\) ===> x=0,2( m0)=n Al
==> n Mg=0,1(mol)
b, m Al= 5,4 g===> mMg= 7,8-5,4=2,4(g)
c, 4Al+ 302===> 2Al203
0,2 0,1
2Mg+ o2=======> 2Mg0
0,1 0,1
tổng số nO2=0,2( moI)
==> m02= 0,2.32=6,4 g

\(\left\{{}\begin{matrix}Mg:a\left(mol\right)\\Al:b\left(mol\right)\\Fe:c\left(mol\right)\end{matrix}\right.\)
Theo đề bài , ta có :
\(\dfrac{24a+10}{24a+27b+56c}.100\%=28,57\%\)
\(\dfrac{24a}{24a+27b+56c-25}.100\%=14,286\%\)
Gọi : 24a = x ; 24a+27b+56c = y
Ta có :
\(\dfrac{x+10}{y}=\dfrac{28,57}{100}\) ; \(\dfrac{x}{y-25}=\dfrac{14,286}{100}\)
Suy ra: x = 2,8579; y = 45
Suy ra :
\(\%m_{Mg}=\dfrac{2,8579}{45}.100\%=6,35\%\)
mhỗn hợp = y = 45(gam)

Đáp án C
nN2O = 0,56 : 22,4 = 0,025 (mol)
Gọi số mol của Mg và Al lần lượt là x và y (mol)
Ta có: mhh = 24x + 27y = 1,86 (1)
Bảo toàn e: n e Mg, Al nhường = n e N+5 nhận=> 2x + 3y = 0,025.8 (2)
Từ (1) và (2) => x = 0,01 (mol) và y = 0,06 (mol)
%m Mg = [(0,01. 24) : 1,86].100% = 12,9 %
% mAl = 100% - 12,9% = 87,10%