Nhúng một thanh Fe có khối lượng là 50g vào 400ml dd CuSO4 1M sau 1 thời gian phản ứng khối lượng tấm Fe tăng lên 4% so với ban đầu.
a) Tính khối lượng Cu thoát ra bám vào lá Feb) Tính CM các chất có trong dd sau phản ứngHãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, PT: \(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
Gọi nFe (pư) = x (mol) ⇒ nCu = nFe = x (mol)
Ta có: m tăng = mCu - mFe (pư)
⇒ 1,2 = 64x - 56x ⇒ x = 0,15 (mol)
⇒ mCu = 0,15.64 = 9,6 (g)
b, Ta có: \(m_{CuSO_4}=400.10\%=40\left(g\right)\Rightarrow n_{CuSO_4}=\dfrac{40}{160}=0,25\left(mol\right)\)
Theo PT: \(n_{FeSO_4}=n_{CuSO_4\left(pư\right)}=n_{Fe}=n_{Cu}=0,15\left(mol\right)\)
⇒ nCuSO4 (dư) = 0,25 - 0,15 = 0,1 (mol)
Có: m dd sau pư = mFe + m dd CuSO4 - mCu = 0,15.56 + 400 - 9,6 = 398,8 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeSO_4}=\dfrac{0,15.152}{398,8}.100\%\approx5,72\%\\C\%_{CuSO_4\left(dư\right)}=\dfrac{0,1.160}{398,8}.100\%\approx4,01\%\end{matrix}\right.\)

Chọn đáp án B.
Áp dụng tăng giảm khối lượng có:
n C u = 1 , 6 64 - 56 = 0 , 2 m o l
⇒ m C u = 64 . 0 , 2 = 12 , 8 gam

Chọn đáp án D
Fe dư ⇒ Cu phản ứng hết ⇒ mTăng = 0,25.(64-56) = 2.

Gọi số mol Fe phản ứng là a (mol)
PTHH: Fe + CuSO4 --> FeSO4 + Cu
a------------------->a----->a
=> 50 - 56a + 64a = 51
=> a = 0,125 (mol)
=> \(n_{FeSO_4}=0,125\left(mol\right)\)
=> \(m_{FeSO_4}=0,125.152=19\left(g\right)\)
\(Đặt:n_{Fe\left(pứ\right)}=x\left(mol\right)\\ Fe+CuSO_4\rightarrow FeSO_4+Cu\\m_{tăng}=m_{Cu}-m_{Fe\left(pứ\right)}=51-50\\ \Leftrightarrow 64x-56x=1\\ \Rightarrow x=0,125\left(mol\right)\\ n_{FeSO_4}=n_{Fe}=0,125\left(mol\right)\\ \Rightarrow m_{FeSO_4}=0,125.152=19\left(g\right)\)
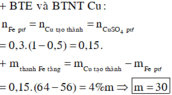
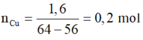
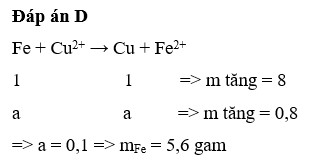
HD:
Fe + CuSO4 ---> FeSO4 + Cu
x x mol x x
a) Khối lượng Fe tăng lên = mCu (thoát ra) - mFe (tan vào dd) ---> 4%.50 = 64.x - 56x ---> x = 0,25 mol.
---> mCu = 64x = 64.0,25 = 16 gam.
b) [FeSO4] = 0,25/0,4 = 0,625 M; [CuSO4] = (0,4 - 0,25)/0,4 = 0,375 M.