Cho 7,36g hỗn hợp X gồm Mg và Fe vào dung dịch chứa AgNO3 và Cu(NO3)2,khi phản ứng kết thúc thu được chất rắn Y và dung dịch Z. Hòa tan hết dung dịch Y bằng dung dịch H2SO4 đẵ nóng dư,thu được 5,04lit SO2,(đktc,spk duy nhất). Cho NaOH dư vào Z, được kết tủa T. Nung T trong không khí đến khối lượng không đổi được 7,2g rắn. Phần trăm khối lượng Fe trong X là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C

- Giả sử Mg, Fe đều phản ứng hết với muối kim loại => Z chứa toàn bộ số mol Mg2+ ; Fex+
=> T chứa Mg(OH)2 và Fe(OH)x => Chất rắn cuối cùng là MgO và Fe2O3 chắc chắn phải có khối lượng lớn hơn lượng kim loại ban đầu trong X => Không thỏa mãn đề bài (7,2 < 7,36)
=> Các muối nitrat phản ứng hết, kim loại dư và đó là Fe (vì Mg phản ứng trước)
=> kết tủa Y gồm Cu, Ag, Fe.
- Gọi nMg = a ; nFe(pứ) = b ; nFe dư = c => mX = 24a + 56b + 56c = 7,36 (1)
- Bảo toàn e cho phản ứng trao đổi muối: 2nMg + 2nFe pứ = nAg + 2nCu = 2a + 2b
- Khi Y + H2SO4 đặc nóng (Fe → Fe3+)
Bảo toàn electron: 2nCu + nAg + 3nFe dư = 2nSO2 = 2.5,04/22,4 = 0,45 mol
=> 2a + 2b + 3c = 0,45 (2)
- Như đã phân tích ở trên. chất rắn cuối cùng gồm MgO và Fe2O3.
Bảo toàn nguyên tố: nMg = nMgO = a ; nFe2O3 = ½ nFe pứ = 0,5b
=> mrắn = mMgO + mFe2O3 = 40a + 160.0,5b = 40a + 80b = 7,2 (3)
Từ (1,2,3) => a = 0,12 ; b = 0,03 ; c = 0,05 mol
=> mFe(X) = 56.(0,03 + 0,05) = 4,48g
=> %mFe(X) = 4,48: 7,36 = 60,87%

Đáp án C
Có mhỗn hợp rắn < mFe => Chứng tỏ X chưa tan hết.
=> Fe bị oxi hóa lên Fe(II)
Đặt số mol Fe phản ứng và Fe dư lần lượt là x, y.
24 . n Mg + 56 . m Fe = 7 , 36 g → BTe 2 . n Mg + 2 x + 3 y = 2 . n SO 2 = 2 . 5 , 04 22 , 4 = 0 , 45 mol m MgO + m Fe 2 O 3 = 40 . n Mg + 160 . x 2 = 7 , 2 g ⇒ n Mg = 0 , 12 mol x = 0 , 03 y = 0 , 05
⇒ % m Fe ( X ) = 56 . ( x + y ) 7 , 36 . 100 % = 60 , 87 %

Đáp án : A
Ta thấy mX > mRắn (gồm oxit) => Y gồm cả Fe , Cu , Ag
Gọi số mol Mg là x ; số mol Fe phản ứng đầu là y và dư sau đó là z mol
=> mX = 24x + 56y + 56z = 7,36g (1)
Bảo toàn e : 2nMg + 2nFe pứ + 3nFe dư = nAg + 2nCu + 3nFe dư = 2nSO2
=> 2x + 2y + 3z = 0,45 mol
,mrắn = mMgO + mFe2O3 = 40x + 80y = 7,2g
=> x = 0,12 mol ; y = 0,03 mol ; z = 0,05 mol
=> %mFe(X) = 60,87%

Đáp án : C
nSO2 = 0,225 mol
Chất rắn sau khi nung chỉ nặng 7,2 gam nên toàn bộ Mg và Fe không thể chuyển hết về oxit được (Lúc đó mrắn > 7,36), tức là trong Y phải có Fe dư —> AgNO3 và Cu(NO3)2 đã hết
Đặt a, b, c là số mol Mg, Fe phản ứng và Fe dư —> 24a + 56(b + c) = 7,36
Chất rắn Y gồm Ag, Cu và Fe dư, phần Ag, Cu do Mg (a) và Fe (b) đẩy ra nên 2a + 2b = nAg + 2nCu
Trong khi đó: nAg + 2nCu + 3nFe dư = 2nSO2 —> 2a + 2b + 3c = 0,225.2
Chất rắn cuối bài gồm MgO (a) và Fe2O3 (b/2) —> 40a + 160b/2 = 7,2
Giải hệ: a = 0,12 mol b = 0,03 mol c = 0,05 mol —> nFe = 0,08 mol —> %mFe = 60,87%

Đáp án A
Có mhỗn hợp rắn =7,2 g < m X
=> Chứng tỏ X chưa phản ứng hết
Trường hợp 1: Mg còn dư, Fe chưa phản ứng
Đặt số mol Mg phản ứng là a, số mol Mg dư là b, số mol Fe là c.
⇒ 24 . ( a + b ) + 56 c = 7 , 36 g → BTe 2 ( a + b ) + 3 c = 2 n SO 2 = 2 . 5 , 04 22 , 4 = 0 , 45 mol m MgO = 40 a = 7 , 2 g ⇒ a = 0 , 18 b = - 0 , 102 c = 0 , 098
=> Loại
Trường hợp 2: Mg phản ứng hết, Fe còn dư
Đặt số mol Fe phản ứng chuyển thành Fe2+ là a, số mol Fe dư là b, số mol Mg là c.
⇒ 56 . ( a + b ) + 24 c = 7 , 36 g → BTe 2 ( c + a ) + 3 b = 2 n SO 2 = 2 . 5 , 04 22 , 4 = 0 , 45 mol m Fe 2 O 3 + m MgO = 160 . a 2 + 40 c = 7 , 2 g ⇒ a = 0 , 03 b = 0 , 05 c = 0 , 12
⇒ % m Fe = 56 . ( 0 , 03 + 0 , 05 ) 7 , 36 . 100 % = 60 , 87 %

T gồm : $Cu(x\ mol) ; Ag(2x\ mol) ; Fe$ dư(y mol)
Suy ra: $64x + 108.2x + 56y = 61,6(1)$
$n_{Fe\ pư} = a - y(mol)$
Bảo toàn electron :
$(a- y).2 + 0,25.2 = 2x + 2x(2)$
$2x + 2x + 3y = 0,55.2(3)$
Từ (1)(2)(3) suy ra a = 0,25 ; x = 0,2 ; y = 0,1
T gồm 3 kim loại là Cu (x), Ag (2x) và Fe dư (y)
\(m_T=64x+108\cdot2x+56y=61.6\left(g\right)\left(1\right)\)
Bảo toàn e :
\(2x+2x+3y=0.55\cdot2\left(2\right)\)
\(\left(1\right),\left(2\right):x=0.2,y=0.1\)
Bảo toàn electron:
\(2\cdot\left(a-0.1\right)+0.25\cdot2=2\cdot0.2+0.2\cdot2\)
\(\Rightarrow a=0.25\)
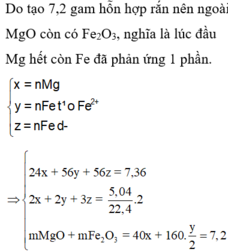
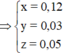
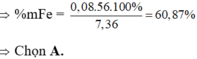

nSO2 = 0,225
Chất rắn sau khi nung chỉ nặng 7,2 gam nên toàn bộ Mg và Fe không thể chuyển hết về oxit được (Lúc đó m rắn > 7,36), tức là trong Y phải có Fe dư \(\rightarrow\) AgNO3 và Cu(NO3)2 đã hết
Đặt a, b, c là số mol Mg, Fe pư và Fe dư \(\rightarrow\) 24a + 56(b + c) = 7,36
Chất rắn Y gồm Ag, Cu và Fe dư, phần Ag, Cu do Mg (a) và Fe (b) đẩy ra nên 2a + 2b = nAg + 2nCu
Trong khi đó: nAg + 2nCu + 3nFe dư = 2nSO2
\(\rightarrow\) 2a + 2b + 3c = 0,225.2
Chất rắn cuối bài gồm MgO (a) và Fe2O3 (b/2) \(\rightarrow\) 40a + 160b/2 = 7,2
Giải hệ:
a = 0,12; b = 0,03 ; c = 0,05
\(\rightarrow\) nFe = 0,08
\(\rightarrow\) %Fe = 60,87%