1. Nhận biết sự có mặt của các khí sau trong cùng hỗn hợp: CO2, SO2, CH4, C2H4
2. Nhận biết mà chỉ dùng quỳ tím các dung dịch sau:
a) Na3PO4, Al(NO3)3, BaCl2, Na2so4, HCl
b) Na2SO4, NaOH, BaCl2, HCl, AgNO3, MgCl2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nhúng giấy quỳ tím lần lượt vào dung dịch mẫu thử. Nhận ra:
- Dung dịch NaOH, Na2SO3 : quỳ hóa xanh (nhóm 1)
- Dung dịch H2SO4 : quỳ hóa đỏ
- Dung dịch Na2SO4,BaCl2 : quỳ không đổi màu (nhóm 2)
Cho H2SO4 vào nhóm 1 nhận ra Na2SO3 vì có khí thoát ra
Na2SO3 + H2SO4 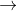 Na2SO4 + SO2 + H2O
Na2SO4 + SO2 + H2O
Chất còn lại là NaOH không hiện tượng.
- Cho Na2SO3 vào nhóm 2 nhận ra BaCl2 vì xuất hiện kết tủa trắng.
BaCl2 + Na2SO3 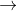 BaSO3 + 2NaCl
BaSO3 + 2NaCl
Ba dung dịch còn lại không hiện tượng
- Cho BaCl2 vào 3 dung dịch còn lại nhận ra Na2SO4 vì có kết tủa trắng xuất hiện
BaCl2 + H2SO4 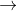 BaSO4 + 2HCl
BaSO4 + 2HCl

Chọn C
+ Dùng quỳ phát hiện ngay ra, Na2CO3 và NaHSO4 (làm thuốc thử)
+ NaOH không có khí. + NaHCO3 có khí CO2.
Chú ý: NaHCO3 có tính bazo yếu nói chung không đổi màu quỳ ở nồng độ thường.

Bài 2 :
1) Trích mẫu thử
Nhúm quỳ tím vào 2 mẫu thử
+ Quỳ Hóa đỏ : H2SO4
+ Quỳ hóa xanh : NaOH
2) Trích mẫu thử
Nhỏ dung dịch BaCl2 vào 2 mẫu thử
+ Mẫu thử tạo kết tủa trắng : Na2SO4
Pt : \(BaCl_2+Na_2SO_4\rightarrow BaSO_4\downarrow+2NaCl\)
Không hiện tượng : HCl
Chúc bạn học tốt
a) BaCl2 + H2SO4 -> BaSO4 + 2HCl
b) Ta có:
Số mol BaCl2 = n = C * V = 1M * 0.3L = 0.3 mol Số mol H2SO4 = n = C * V = 0.5M * 0.4L = 0.2 mol
Do phản ứng xảy ra theo tỉ lệ 1:1 giữa BaCl2 và BaSO4, nên số mol BaSO4 tạo thành cũng là 0.3 mol.
Khối lượng mol của BaSO4 (molar mass) là 233.4 g/mol. Vậy khối lượng kết tủa trắng sau phản ứng là: m = n * M = 0.3 mol * 233.4 g/mol = 70.02 g
c) Để tính nồng độ mol chất tan sau phản ứng, ta phải xác định số mol của H2SO4 còn lại sau phản ứng. Vì phản ứng xảy ra theo tỉ lệ 1:1 giữa H2SO4 và BaCl2, nên số mol H2SO4 còn lại sau phản ứng cũng là 0.2 mol.
Thể tích dung dịch không thay đổi, nên nồng độ mol chất tan sau phản ứng cũng không thay đổi. Vậy nồng độ mol của H2SO4 sau phản ứng vẫn là 0.5M.

bài thì dễ nhưng có 8 chất lười với bây h hầu hết anh chị hay mn đều ôn thi rồi hay sao á bạn à ít người giải lắm

Bài 1:
- Dùng quỳ tím
+) Hóa đỏ: HCl
+) Hóa xanh: NaOH
+) Không đổi màu: NaCl và H2O
- Đổ dd AgNO3 vào 2 chất còn lại
+) Xuất hiện kết tủa: NaCl
PTHH: \(AgNO_3+NaCl\rightarrow NaNO_3+AgCl\downarrow\)
+) Không hiện tượng: H2O
1)
- Dùng quỳ tím ẩm
+) Hóa đỏ: CO2 và SO2 (Nhóm 1)
+) Không đổi màu: CH4 và C2H4 (Nhóm 2)
- Sục các khí trong từng nhóm vào dd Brom
+) Dung dịch Brom nhạt màu: SO2 (Nhóm 1) và C2H4 (Nhóm 2)
PTHH: \(SO_2+Br_2+2H_2O\rightarrow H_2SO_4+2HBr\)
+) Không hiện tượng: CO2 (Nhóm 1) và CH4 (Nhóm 2)
Câu 2:
a)
- Dùng quỳ tím
+) Hóa xanh: Na3PO4
+) Hóa đỏ: HCl và Al(NO3)3 (Nhóm 1)
+) Không đổi màu: BaCl2 và Na2SO4 (Nhóm 2)
- Đổ dd Na3PO4 vào từng nhóm
+) Xuất hiện kết tủa: Al(NO3)3 (Nhóm 1) và BaCl2 (Nhóm 2)
PTHH: \(Na_3PO_4+Al\left(NO_3\right)_3\rightarrow3NaNO_3+AlPO_4\downarrow\)
\(3BaCl_2+2Na_3PO_4\rightarrow6NaCl+Ba_3\left(PO_4\right)_2\downarrow\)
+) Không hiện tượng: HCl (Nhóm 1) và Na2SO4 (Nhóm 2)