Đết cháy hoàn toàn 1,3g hiđrocacbon X(X là chất lỏng ở điều kiện thường) thu được 2,24 lít khí CO2 (đktc). Xác định CTPT của X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có :
$ n_{CO_2} = \dfrac{7,7952}{22,4} = 0,348(mol)$
$n_{H_2O} = \dfrac{4,176}{18} = 0,232(mol)$
Ta có :
$n_C = n_{CO_2} = 0,348(mol)$
$n_H = 2n_{H_2O} = 0,232.2 = 0,464(mol)$
$n_C : n_H = 0,348 : 0,464 = 3 : 4$
Vì X là chất khí nên có số C nhỏ hơn hoặc bằng 4
Suy ra: CTPT là $C_3H_4$

Chọn D.
Đặt CTTQ của X là CxHy (phân tử có chứa k liên kết π). Ta có:
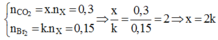
Với x = 2 Þ k = 1: X là C2H4 Þ m = 4,2 (g)
Với x = 4 Þ k = 2: X là C4H6 Þ m = 4,05 (g) Þ giá trị nhỏ nhất.

Đặt CTHH của X là
\(C_nH_{2n+1}COOH\)
\(n_{C_nH_{2n+1}COOH}=\dfrac{2,55}{14n+46}\left(mol\right);n_{CO_2}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\)
BTNT C: \(n_{CO_2}=\left(n+1\right).n_{C_nH_{2n+1}COOH}=\dfrac{2,55.\left(n+1\right)}{14n+46}=0,125\)
\(\Rightarrow n=4\)
Vậy X là \(C_4H_9COOH\)

Đáp án D
Theo phương trình phản ứng n CO2 = n H2O = a
=> n O2 = 1.25 a
2n X+ 2 n O2 = 2 n CO2 + n H2O
=> n X = 0,25 a
=>Số C = a : 0,25 a = 4
=> X là C4H8O2
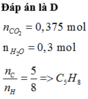
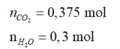
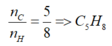

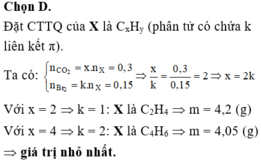
CxHy+(x+y/4)O2==>xCO2+(y/2)H2O
Có nCO2=0.1(mol),nCxHy=1.3:(12x+y)
có nCO2=x nhân vs mol CxHy==>0.1=x nhân với \(\frac{1.3}{12x+y}\)
==>0.1(12x+y)=1.3x
==>x=y.