Hòa tan 17,2 gam hỗn hợp gồm NA và Cả vào H20( nước ) sau phản ứng thu được 8,96 lít H2 (đktc) tính thành phần phần trăm % theo khối lượng mỗi kim loại
p/s Ai biết giải dùm mình ....................mình cần gấp hóa 8 ..............!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!.




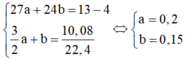
Gọi a là số mol Ca
b là số mol Na
Số mol H2: \(\frac{8,96}{22,4} = 0,4 mol\)
phương trình phản ứng: Ca + 2H2O ----> Ca(OH)2 + H2
a ----------------------------------->a
Na + H2O -----> NaOH + \(\frac{1}{2}\)H2
b -----------------------------------\(\frac{1}{2}\)b
Ta có hệ phương trình 40a + 23b=17,2
a+\(\frac{1}{2}\)b=0,4
<=> a= 0,2 và b=0,4
%Ca=\(\frac{40.0,2}{17,2}.100=46,51\)%
suy ra %Na=100 - 46,51 = 53,49%
nH2=8,96/22,4=0,4 mol
Giả sử số mol Na,Ca lần lượt là x,y mol
PT Na + H2O -> NaOH +1/2 H2
x 1/2x
Ca +2H2O -> Ca(OH)2 + H2
y y
Theo bài và theo ptpu ta có hệ 23x + 40y =17,2
1/2x + y =0,4
=> x=0,4 , y= 0,2
=> %Na = 0,4.23/17,2 .100%=53,5%
%Ca= 0,2.40/17,2 ,100% = 46,5%