Tính thể tích không khí chứa 20% Oxi(ở đktc) cần dùng để đốt cháy hoàn toàn 64 gam khí meetan?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a.\(n_{Cu}=\dfrac{6,4}{64}=0,1mol\)
\(2Cu+O_2\rightarrow\left(t^o\right)2CuO\)
0,1 0,05 ( mol )
\(V_{kk}=\left(0,05.22,4\right).5=5,6l\)
b.\(2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\)
1/30 0,05 ( mol )
\(m_{KClO_3}=\dfrac{1}{30}.122,5=4,08g\)

Đáp án A
Hỗn hợp khí gồm CH4, C2H6 và C3H8 là các hidrocacbon.
Mà khi đốt cháy 1 hidrocacbon bất kì ta luôn có:
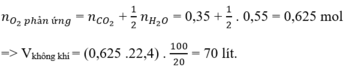

\(2C_2H_2+5O_2-^{t^o}\rightarrow4CO_2+2H_2O\\ n_{C_2H_2}=\dfrac{1,3}{26}=0,05\left(mol\right)\\ n_{O_2}=\dfrac{5}{2}n_{C_2H_2}=0,125\left(mol\right)\\ \Rightarrow V_{O_2}=2,8\left(l\right)\\ Vìtrongkhôngkhíchứa20\%O_2\\ \Rightarrow V_{kk}=\dfrac{2,8}{20\%}=14\left(l\right)\)

nAl = 10,8: 27=0,4 (mol)
pthh : 4Al + 3O2 -t--->2 Al2O3
0,4---> 0,3 (mol)
=>VO2 = 0,3 .22,4 = 6,72 (l)
ta có : VO2 = 1/5 Vkk <=> Vkk = VO2 : 1/5= 33,6 (l)
pthh : 2KClO3 -t--> 2KCl + 3O2
0,2<---------------------0,3 (mol)
=> mKClO3 = 0,2 . 122,5 (g)
pthh : 2KMnO4-t--> K2MnO4 + MnO2+ O2
0,6<-------------------------------- 0,3(mol)
=> mKMnO4 = 0,6.158 = 94,8 (g)

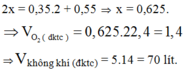
nCH4= 64/16=4 mol
CH4 + 2O2=(t0) CO2+ 2H2O
nO2= 2nCH4=2.4=8 mol
VO2= 8.22,4= 179,2 ( l) => VKK= 179,2.100/20=896 ( l)
672 (l) nhé baì này viết pt cáy ra thôi tính đk số mol oxi suy ra số mol không khí = số mol oxi nhân 100/20