Nung nóng KMnO4 thu được K2MnO4+ MnO2+O2. Dùng oxi ở trên oxi hóa sắt ở nhiệt độ cao thu được Fe3O4
a) Tính lượng sắt và oxi cần dùng để điều chế 2,32g Fe3O4
b) Tính khối lượng KMnO4 cần dùng
Mọi người ơi giúp mình nha, nhớ trình bày cụ thể cho mình đó, cảm ơn rất nhiều ạ

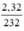 = 0,01 mol.
= 0,01 mol.
2KMnO4 = K2MnO4+MnO2+ O2 (1)
3Fe+ 2O2=(t0)Fe3O4 (2)
nFe3O4=2,32/232=0,01 mol
nO2=2nFe3O4=0,02 mol --> mO2=0,02. 32=0,64 g
nFe= 3nFe3O4=0,03 mol --> mFe=0,03.56=1,68 g
Ta có: nO2(1)=nO2(2)= 0,02 mol --> nKMnO4=2nO2=2. 0,02=0,04 mol => mKMnO4= 0,04. 158=6,32 g
xin lỗi nhé anh nhầm bước cuôi nKMnO4=2NO2=0.04 mol
=> mKMnO4=0.04*158=6.32g
Xin lỗi nhé