Cho 9,36 gam kali vào 70,88 gam nước. Nồng độ % của dung dịch thu được
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, \(n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\)
PTHH: 2K + 2H2O ---> 2KOH + H2
0,1---------------->0,1----->0,05
\(m_{ct}=m_{KOH}=0,1.56=5,6\left(g\right)\\ m_{dd}=m_K+m_{H_2O}-m_{H_2}=96,2+3,9-0,05.2=100\left(g\right)\)
\(C\%_{KOH}=\dfrac{5,6}{100}.100\%=5,6\%\\ b,m_{dd}=100+50=150\left(g\right)\\ C\%_{KOH}=\dfrac{5,6}{150}.100\%=3,37\%\)
c, Gọi \(m_{H_2O}=a\left(g\right)\)
\(\Rightarrow C\%_{KOH}=\dfrac{5,6}{100+a}.100\%=2,8\%\\ \Leftrightarrow a=100\left(g\right)\)
d, Gọi \(m_{KOH}=a\left(g\right)\)
\(\Rightarrow C\%_{KOH}=\dfrac{5,6+a}{100+a}.100\%=22,4\%\\ \Leftrightarrow a=21,65\left(g\right)\)

Đáp án B
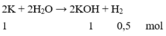
m C t = m K O H = 1.56 = 56 gam.
m d d = m K L + m n ư ớ c - m k h í = 39 + 362 – 0,5.1 = 400 gam.
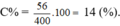

a)
\(n_{K_2O}=\dfrac{18,8}{94}=0,2\left(mol\right)\)
PTHH: K2O + H2O --> 2KOH
0,2-->0,2---->0,4
mct = 0,4.56 = 22,4 (g)
mdm = 81,2 - 0,2.18 = 77,6 (g)
mdd = 22,4 + 77,6 = 100 (g)
b)
\(C\%=\dfrac{22,4}{100}.100\%=22,4\%\)
c)
\(C\%=\dfrac{22,4}{50+100}.100\%=14,933\%\)
d)
\(m_{dd\left(sau.khi.thêm\right)}=\dfrac{22,4.100}{11,2}=200\left(g\right)\)
=> mH2O(thêm) = 200 - 100 = 100 (g)
e) Gọi khối lượng KOH thêm là x (g)
Có: \(C\%_{\left(dd.sau.khi.thêm\right)}=\dfrac{22,4+x}{100+x}.100\%=30\%\)
=> x = 10,857 (g)

\(n_K=\frac{5,85}{15}=0,15(mol)\\ K+H_2O \to KOH +\frac{1}{2}H_2\\ n_{KOH}=n_K=0,15(mol)\\ n_{H_2}=\frac{1}{2}.n_K=\frac{1}{2}.0,15=0,075(mol)\\ m_{dd}=5,85+100-(0,075.2)=105,7(g)\\ C\%=\frac{0,15.56}{105,7}.100=7,95\%\)

K + H2O -------> KOH + 1/2 H2
nK = 5,85/39=0,15 (mol)
Theo PT : nKOH=nK = 0,15 (mol)
=> CM KOH = n/V = 0,15/0,1=1,5M
=> Chọn C
Số mol của kali
nK = \(\dfrac{m_K}{M_K}=\dfrac{5,85}{39}=0,15\left(mol\right)\)
Pt : 2K + 2H2O → 2KOH + H2\(|\)
2 2 2 1
0,15 0,15
Số mol của dung dịch kali hidroxit
nKOH= \(\dfrac{0,15.2}{2}=0,15\left(mol\right)\)
Nồng độ mol của dung dịch kali hidroxit
CMKOH = \(\dfrac{0,15}{0,1}=1,5\left(M\right)\)
⇒ Chọn câu : C
Chúc bạn học tốt

\(n_K=\dfrac{31,2}{39}=0,8\left(mol\right)\)
PTHH :
\(2K+2H_2O\underrightarrow{t^o}2KOH+H_2\uparrow\)
0,8 0,8 0,4
\(a,V_{H_2}=0,4.22,4=8,96\left(l\right)\)
\(b,m_{KOH}=0,8.56=44,8\left(g\right)\)
\(m_{ddKOH}=\left(31,2+200\right)-\left(0,4.2\right)=300,4\left(g\right)\)
\(c,C\%_{KOH}=\dfrac{44,8}{\left(200+31,2\right)-\left(0,4.2\right)}.100\%\approx19,44\%\)

mH2O=71,8.1=71,8(g)
nK2O=28,2/94=0,3(mol)
PTHH: K2O + H2O -> 2 KOH
0,3____________0,6(mol)
mKOH= 0,6.56=33,6(g)
mddKOH= mK2O + mH2O= 28,2+71,8=100(g)
=>C%ddB=C%ddKOH=(33,6/100).100=33,6%
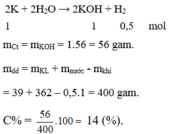
$2K + 2H_2O \to 2KOH + H_2$
$n_{KOH} = n_K = \dfrac{9,36}{39} =0,24(mol)$
$n_{H_2} = \dfrac{1}{2}n_K = 0,12(mol)$
$m_{dd\ sau\ pư} = 9,36 + 70,88 - 0,12.2 = 80(gam)$
$C\%_{KOH} = \dfrac{0,24.56}{80}.100\% = 16,8\%$