Cho m gam hỗn hợp gồm Al và Na vào H2O dư, sau khi các phản ứng xảy ra hoàn toàn, thu được 3,36 lít khí H2 (đktc) và 1,35 g chất rắn không tan. Tính giá trị của m (biết Al là kim loại phản ứng được với dd kiềm : Al + NaOH + H2O -> NaAlO2 + H2. Dd NaAlO2 có tên là Natrialuminat)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Giải thích:
Rắn không tan là Al dư => mAl dư = 1,35 (g)
nH2 = 2,24 : 22,4 = 0,1 (mol)
Gọi số mol Na = số mol Al pư = a (mol)
BT e ta có: nNa + 3nAl = 2nH2 => a + 3a = 2. 0,1
=> a = 0,05 (mol)
=> m = mNa + mAl pư + mAl dư = 0,05.23 + 0,05.27 + 1,35 = 3,85 (g)
Đáp án B

Chọn B
Rắn không tan là Al dư => mAl dư = 1,35 (g)
nH2 = 2,24 : 22,4 = 0,1 (mol)
Gọi số mol Na = số mol Al pư = a (mol)
BT e ta có: nNa + 3nAl = 2nH2 => a + 3a = 2. 0,1
=> a = 0,05 (mol)
=> m = mNa + mAl pư + mAl dư = 0,05.23 + 0,05.27 + 1,35 = 3,85 (g)

Đáp án B
Rắn không tan là Al dư
=> mAl dư = 1,35 (g)
nH2 = 2,24 : 22,4 = 0,1 (mol)
Gọi số mol Na = số mol Al pư = a (mol)
BT e ta có: nNa + 3nAl = 2nH2
=> a + 3a = 2. 0,1
=> a = 0,05 (mol)
=> m = mNa + mAl pư + mAl dư = 0,05.23 + 0,05.27 + 1,35 = 3,85 (g)

nH2 = \(\dfrac{V_{H^2}}{22,4}\) = \(\dfrac{2,24}{22,4}\) = 0,1 (mol)
n = \(\dfrac{m_{NaAlO_2}}{M_{NaAlO_2}}\) = \(\dfrac{1,35}{82}\) \(\approx\) 0,02 (mol)
Ta có phương trình hoá học:
2NaOH + 2Al + 2H2O \(\underrightarrow{t^0}\) 2NaAlO2 + 3H2
PT: 2 : 2 : 2 : 2 : 3 (mol)
ĐB: \(\dfrac{0,02}{2}\) < \(\dfrac{0,1}{3}\) (mol)
⇒ H2 dư, mọi tính toán dựa vào số mol của NaAlO2
Ta có phương trình hoá học:
2NaOH + 2Al + 2H2O \(\underrightarrow{t^0}\) 2NaAlO2 + 3H2
PT: 2 : 2 : 2 : 2 : 3 (mol)
ĐB: 0,02: 0,02: 0,02 : 0,02 : 0,03 (mol)
mNaOH = nNaOH . MNaOH = 0,02 . 40 = 0,8 (g)
mAl = nAl . MAl = 0,02 . 27 = 0,54 (g)
Vậy mNaOH = 0,8 g, mAl = 0,54 g.
* Chú thích: PT là phương trình, ĐB là đề bài.
Dòng 2 bị thiếu nên đây là dòng 2 được viết lại ạ: \(n_{NaAlO_2}\) = \(\dfrac{m_{NaAlO_2}}{M_{NaAlO_2}}=\dfrac{1,35}{82}\approx0,02\left(mol\right)\)

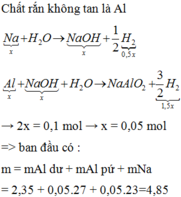
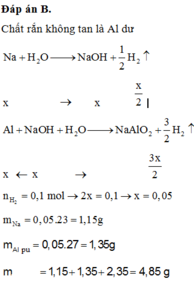
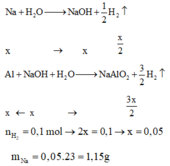
Gọi $n_{Na} = a(mol)$
2Na + 2H2O → 2NaOH + H2
a...........................a..........0,5a.....(mol)
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
..a...........a............................................1,5a....(mol)
Suy ra : $0,5a + 1,5a = \dfrac{3,36}{22,4} = 0,15 \Rightarrow a = 0,075$
Vậy :
$m = 0,075.23 + 0,075.27 + 1,35 = 5,1(gam)$
Gọi nNa=a(mol)���=�(���)
2Na + 2H2O → 2NaOH + H2
a...........................a..........0,5a.....(mol)
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
..a...........a............................................1,5a....(mol)
Suy ra : 0,5a+1,5a=3,3622,4=0,15⇒a=0,0750,5�+1,5�=3,3622,4=0,15⇒�=0,075
Vậy :
m=0,075.23+0,075.27+1,35=5,1(gam)