Hỗn hợp X gồm FeO Fe2O3 Fe304 cho một luồng khí CO đi qua ống sứ đựng m gam hỗn hợp X đun nóng. Sau khi kết thúc thí nghiệm thu được 64 gam chất rắn A trong ống sứ và 11,2 llít khí B ở điều kiện tiêu chuẩn có tỉ khối so với H2 là 20,4. Tính giá trị m Giải bài này hộ e chi tiết xíu :))
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án : C
Tổng quát : CO + OOxit -> CO2
,nB = 0,5 mol ; MB = 40,8g => có CO và CO2
=> nCO = 0,1 ; nCO2 = 0,4 mol
=> mX = mA + mO pứ = 64 + 0,4.16 = 70,4g
Các phản ứng khử sắt oxit có thể có:
3Fe2O3 + CO --> 2Fe3O4 + CO2 (1)
Fe3O4 + CO --> 3FeO + CO2 (2)
FeO + CO --> Fe + CO2 (3)
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 hoặc ít hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, quan trọng là số mol CO phản ứng bao giờ cũng bằng số mol CO2 tạo thành. nB = 11,2/22,5 = 0,5 mol
Gọi x là số mol của CO2 ta có phương trình về khối lượng của B:
44x + 28(0,5 x) = 0,5 x 20,4 x 2 = 20,4
nhận được x = 0,4 mol và đó cũng chính là số mol CO tham gia phản ứng.
Theo ĐLBTKL ta có:
mX + mCO = mA + mCO2
--> m = 64 + 0,4 x 44 - 0,4 x 28 = 70,4 gam
chon C nha

Các phản ứng khử sắt oxit có thể có:
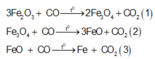
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 Fe2O3 dư hoặc ít chất hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, các bạn chỉ cần quan sát và nhận thấy luôn có: n C O 2 = n C O
n B = 11 , 2 22 , 4 = 0 , 5 m o l .
Ta có B gồm CO2 mới tạo thành và CO dư
Gọi:
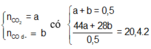

Áp dụng định luật bảo toàn khối lượng ta có:
![]()
⇒ m = 64 + 0,4.44 - 0,4.28 = 60,4 (gam)
Đáp án C.
Các phản ứng khử sắt oxit có thể có:
3Fe2O3 + CO --> 2Fe3O4 + CO2 (1)
Fe3O4 + CO --> 3FeO + CO2 (2)
FeO + CO --> Fe + CO2 (3)
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 hoặc ít hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, quan trọng là số mol CO phản ứng bao giờ cũng bằng số mol CO2 tạo thành. nB = 11,2/22,5 = 0,5 mol
Gọi x là số mol của CO2 ta có phương trình về khối lượng của B:
44x + 28(0,5 x) = 0,5 x 20,4 x 2 = 20,4
nhận được x = 0,4 mol và đó cũng chính là số mol CO tham gia phản ứng.
Theo ĐLBTKL ta có:
mX + mCO = mA + mCO2
--> m = 64 + 0,4 x 44 - 0,4 x 28 = 70,4 gam.
chọn C nha

\(n_{CO\left(dư\right)}=a\left(mol\right)\)
\(n_{CO_2}=b\left(mol\right)\)
\(n_B=a+b=0.5\left(mol\right)\left(1\right)\)
\(m_B=2\cdot20.4\cdot0.5=20.4\left(g\right)\)
\(\Rightarrow28a+44b=20.4\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.4\)
\(n_{CO\left(pư\right)}=n_{CO_2}=0.4\left(mol\right)\)
\(BTKL:\)
\(m_X+m_{CO}=m_A+m_B\)
\(\Leftrightarrow m_X=64+0.4\cdot44-0.4\cdot28=70.4\left(g\right)\)
Các phản ứng khử sắt oxit có thể có:
3Fe2O3 + CO --> 2Fe3O4 + CO2 (1)
Fe3O4 + CO --> 3FeO + CO2 (2)
FeO + CO --> Fe + CO2 (3)
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 hoặc ít hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, quan trọng là số mol CO phản ứng bao giờ cũng bằng số mol CO2 tạo thành. nB = 11,2/22,5 = 0,5 mol
Gọi x là số mol của CO2 ta có phương trình về khối lượng của B:
44x + 28(0,5 x) = 0,5 x 20,4 x 2 = 20,4
nhận được x = 0,4 mol và đó cũng chính là số mol CO tham gia phản ứng.
Theo ĐLBTKL ta có:
mX + mCO = mA + mCO2
--> m = 64 + 0,4 x 44 - 0,4 x 28 = 70,4 gam.

Đáp án D
Hỗn hợp khí thu được gổm: CO dư và CO2 sinh ra
Gọi n(CO) =a, n(CO2)= b
Ta có: a+b = 11,2:22,4 và 28a+ 44b= 11,2/22,4. 20,4. 2
Tìm được a= 0,1 và b= 0,4. Vậy n(CO) p.ư = 0,4
BTKL: m + m(CO p.ư) = m(CR) +m(CO2)
m= 63,6 + 0,4. 44- 0,4. 28 = 70 (g)

Đáp án D
Hỗn hợp khí thu được gổm: CO dư và CO2 sinh ra
Gọi n(CO) =a, n(CO2)= b
Ta có: a+b = 11,2:22,4 và 28a+ 44b= 11,2/22,4. 20,4. 2
Tìm được a= 0,1 và b= 0,4. Vậy n(CO) p.ư = 0,4
BTKL: m + m(CO p.ư) = m(CR) +m(CO2)
m= 63,6 + 0,4. 44- 0,4. 28 = 70 (g)

bạn hãy xác định xem khí B gồm những khí gì (99.9% các bài đều có lẫn khí CO và H2) .sau đó dùng qui tắc đường chéo để xđ tỉ lệ số mol 2 khí như vậy sẽ dễ làm hơn
Các phản ứng khử sắt oxit có thể có:
3Fe2O3 + CO --> 2Fe3O4 + CO2 (1)
Fe3O4 + CO --> 3FeO + CO2 (2)
FeO + CO --> Fe + CO2 (3)
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 hoặc ít hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, quan trọng là số mol CO phản ứng bao giờ cũng bằng số mol CO2 tạo thành. nB = 11,2/22,5 = 0,5 mol
Gọi x là số mol của CO2 ta có phương trình về khối lượng của B:
44x + 28(0,5 x) = 0,5 x 20,4 x 2 = 20,4
nhận được x = 0,4 mol và đó cũng chính là số mol CO tham gia phản ứng.
Theo ĐLBTKL ta có:
mX + mCO = mA + mCO2
--> m = 64 + 0,4 x 44 - 0,4 x 28 = 70,4 gam.
chon C nha

B gồm CO(a mol) ; CO2( b mol)
Ta có:
\(n_B = a + b = \dfrac{11,2}{22,4}=0,5(mol)\\ m_B = 28a + 44b = 0,5.2.20,4 = 20,4(gam)\\ \Rightarrow a = 0,1 ; b = 0,4\\ CO + O_{oxit} \to CO_2\\ n_O = n_{CO_2} = 0,4(mol)\\ \Rightarrow m = m_A + m_{O\ pư} = 6,4 + 0,4.16 = 12,8(gam)\)
Các phản ứng khử sắt oxit có thể có:
3Fe2O3 + CO --> 2Fe3O4 + CO2 (1)
Fe3O4 + CO --> 3FeO + CO2 (2)
FeO + CO --> Fe + CO2 (3)
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 hoặc ít hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, quan trọng là số mol CO phản ứng bao giờ cũng bằng số mol CO2 tạo thành. nB = 11,2/22,5 = 0,5 mol
Gọi x là số mol của CO2 ta có phương trình về khối lượng của B:
44x + 28(0,5 x) = 0,5 x 20,4 x 2 = 20,4
nhận được x = 0,4 mol và đó cũng chính là số mol CO tham gia phản ứng.
Theo ĐLBTKL ta có:
mX + mCO = mA + mCO2
--> m = 64 + 0,4 x 44 - 0,4 x 28 = 70,4 gam.

Khí B gồm : $CO(a\ mol) ; CO_2(b\ mol)$
Ta có :
$a + b = \dfrac{11,2}{22,4} = 0,5(mol)$
$M_B = \dfrac{28a + 44b}{a + b} = 20,4.2$
Suy ra : a = 0,1 ; b = 0,4
$CO + O_{oxit} \to CO_2$
$n_{O(oxit)\ pư} = n_{CO_2} = 0,4(mol)$
$\Rightarrow m = m_A + m_O = 64 + 0,4.16 = 70,4(gam)$

\(n_{CO}=a\left(mol\right),n_{CO_2}=b\left(mol\right)\)
\(n_B=a+b=0.5\left(mol\right)\)
\(m_B=20.4\cdot2\cdot0.5=20.4\left(g\right)\)
\(\Leftrightarrow28a+44b=20.4\)
\(KĐ:a=0.1,b=0.4\)
\(n_{CO\left(pư\right)}=n_{CO_2}=0.4\left(mol\right)\)
\(BTKL:\)
\(m=0.4\cdot44+64-0.4\cdot28=70.4\left(g\right)\)