Sục rất từ từ V lít CO2 (đktc) vào 184g dung dịch Ca(OH)2 20% thì thu được 30g kết tủa. Tính V và nồng độ phần trăm của các chất có trong dung dịch sau phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, Ta có : \(\left\{{}\begin{matrix}n_{CaCO3}=\dfrac{m}{M}=0,2\left(mol\right)\\n_{Ca\left(OH\right)2}=C_M.V=0,4\left(mol\right)\end{matrix}\right.\)
\(BTNT\left(Ca\right):n_{Ca\left(HCO_3\right)_2}=n_{Ca\left(OH\right)2}-n_{CaCO3}=0,2\left(mol\right)\)
\(BTNT\left(C\right):n_{CO2}=n_{CaCO3}+2n_{Ca\left(HCO3\right)2}=0,6\left(mol\right)\)
\(\Rightarrow V_{CO2}=13,44l\)
b, Ta có : \(\left\{{}\begin{matrix}n_{BaCO3}=\dfrac{m}{M}=0,025\left(mol\right)\\n_{Ba\left(OH\right)2}=C_M.V=0,2\left(mol\right)\end{matrix}\right.\)
\(BTNT\left(Ba\right):n_{Ba\left(HCO_3\right)_2}=n_{Ba\left(OH\right)2}-n_{BaCO3}=0,175\left(mol\right)\)
\(BTNT\left(C\right):n_{CO2}=n_{BaCO3}+2n_{Ba\left(HCO3\right)2}=0,375\left(mol\right)\)
\(\Rightarrow V_{CO2}=8,4l\)
c, Ta có : \(1< T=\dfrac{n_{NaOH}}{n_{SO2}}=1,875< 2\)
- Áp dụng phương pháp đường chéo :
Ta được : \(\dfrac{n_{NaHSO3}}{n_{Na2SO3}}=\dfrac{1}{7}\)
\(\Leftrightarrow7n_{NaHSO3}-n_{Na2SO3}=0\)
\(BTNT\left(Na\right):n_{NaHSO3}+2n_{Na2SO3}=0,375\)
\(\Rightarrow\left\{{}\begin{matrix}n_{NaHSO3}=0,025\\n_{Na2SO3}=0,175\end{matrix}\right.\)
\(\Rightarrow m_M=24,65g\)

Chọn đáp án A
NaOH + X → kết tủa ⇒ ban đầu tạo 2 muối || Đọc kĩ giả thiết:
Cho TỪ TỪ NaOH vào X ĐẾN KHI thu được ↓ max ⇒ chỉ xảy ra phản ứng:
Ca(HCO3)2 + NaOH → CaCO3 + NaHCO3 + H2O
⇒ nCa(HCO3)2 = nNaOH = 0,12 mol ⇒ nHCO3– = 0,24 mol.
Ta có: nOH– = 2nCO2 - nHCO3– = 0,36 mol ⇒ a = 0,36 ÷ 2 ÷ 0,4 = 0,45M.

Đáp án A
NaOH + X → kết tủa ⇒ ban đầu tạo 2 muối || Đọc kĩ giả thiết:
Cho TỪ TỪ NaOH vào X ĐẾN KHI thu được ↓ max
⇒ chỉ xảy ra phản ứng:Ca(HCO3)2 + NaOH → CaCO3 + NaHCO3 + H2O
⇒ nCa(HCO3)2 = nNaOH = 0,12 mol ⇒ nHCO3– = 0,24 mol.
Ta có: nOH– = 2nCO2 - nHCO3– = 0,36 mol ⇒ a = 0,36 ÷ 2 ÷ 0,4 = 0,45M.

Bài 23 :
n BaCO3 = 0,1(mol) > n Ba(OH)2 = 0,15 mol
- TH1 : Ba(OH)2 dư
$Ba(OH)_2 + CO_2 \to BaCO_3 + H_2O$
n CO2 = n BaCO3 = 0,1(mol)
=> V = 0,1.22,4 = 2,24 lít
- TH1 : BaCO3 bị hòa tan một phần
$Ba(OH)_2 + CO_2 \to BaCO_3 + H_2O(1)$
$Ba(OH)_2 + 2CO_2 \to Ba(HCO_3)_2(2)$
n CO2(1) = n Ba(OH)2 (1) = n BaCO3 = 0,1(mol)
=> n Ba(OH)2 (2) = 0,15 - 0,1 = 0,05(mol)
=> n CO2 (2) = 2n Ba(OH)2 (2) = 0,1(mol)
=> V = (0,1 + 0,1).22,4 = 4,48 lít

nCa(OH)2= 0,2.1 = 0,2 mol.
nCaCO3 = 15 : 100 = 0,15mol
Cho NaOH vào dung dịch sau PƯ thấy xuất hiện kết tủa nên trong dd có muối Ca(HCO3)2
Vậy xảy ra 2 phản ứng:
CO2 + Ca(OH)2 -----> CaCO3 + H2O (1)
0,15 mol 0,15 mol 0,15 mol
2CO2 + Ca(OH)2 ------> Ca(HCO3)2 (2)
2. 0,05 mol 0,05 mol
Theo (1) : nCO2(1) = nCa(OH)2 (1) = nCaCO3 = 0,15mol
=> nCa(OH)2 (2) = 0,2 - 0,15 = 0,05 mol
Theo (2) : nCO2 (2) = 2. 0,05 = 0,1 mol
=> nCO2 = 0,15 + 0,1 = 0,25 mol
=> VCO2 = 0,25 . 22,4 = 5,6 (L)
nCaCO3 = 10 / 100 = 0,1 chứ ạ !!
vì m kết tủa bằng 10 chứ ạ ???? giải thích hộ vs ạ

\(n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(n_{KOH}=0,15.1,5=0,225\left(mol\right)\)
Có: \(\dfrac{n_{KOH}}{n_{CO_2}}=0,45< 1\) → Pư tạo muối KHCO3 và CO2 dư.
PT: \(CO_2+KOH\rightarrow KHCO_3\)
____0,225_____0,225_____0,225 (mol)
\(\Rightarrow C_{M_{KHCO_3}}=\dfrac{0,225}{0,15}=1,5\left(M\right)\)

Đáp án B
nCaCO3 = 20: 100 = 0,2 mol. Vì Ca(OH)2 dư nên chỉ có phản ứng tạo muối trung hòa.
Ca(OH)2 + CO2 → CaCO3 + H2O
Mol 0,2 ← 0,2
=> VCO2 = 0,2.22,4 = 4,48 lit
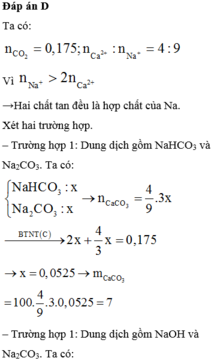
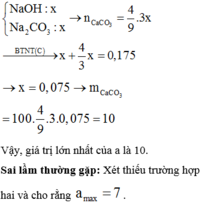
$n_{Ca(OH)_2} = \dfrac{185.20\%}{74} = 0,5(mol)$
$n_{CaCO_3} = 0,3(mol)$
TH1 : Ca(OH)2 dư
Ca(OH)2 + CO2 → CaCO3 + H2O
0,3..............0,3.........0,3........................(mol)
V = 0,3.22,4 = 6,72 lít
$m_{dd} = 0,3.44 + 185 - 30 = 168,2(gam)$
$C\%_{Ca(OH)_2\ dư} = \dfrac{(0,5 - 0,3).74}{168,2}.100\% = 8,8\%$
TH2 : Có tạo muối axit
Ca(OH)2 + CO2 → CaCO3 + H2O
0,3..............0,3.........0,3........................(mol)
Ca(OH)2 + 2CO2 → Ca(HCO3)2
0,2.............0,4...............0,2.........................(mol)
V = (0,3 + 0,4).22,4 = 15,68 lít
$m_{dd} = 0,7.44 + 185 - 30 = 185,8(gam)$
$C\%_{Ca(HCO_3)_2} = \dfrac{0,2.162}{185,8}.100\% = 17,4\%$
Theo gt ta có: $n_{Ca(OH)_2}=\frac{92}{185}(mol)$
+, Xét trường hợp 1: Chỉ tạo muối $CaCO_3$
$\Rightarrow n_{CO_2}=n_{CaCO_3}=0,3(mol)\Rightarrow V=6,72(l)$
Bảo toàn khối lượng ta có: $m_{dd}=167,2(g)$
$\Rightarrow \%C_{Ca(OH)_2}=8,73\%$
+, Xét trường hợp 2: Tạo 2 muối
Bảo toàn Ca ta có: $n_{Ca(HCO_3)_2}=\frac{73}{370}(mol)$
Bảo toàn C ta có: $n_{CO_2}=\frac{257}{370}(mol)\Rightarrow V_{CO_2}=15,56(l)$
$\Rightarrow \%m_{Ca(HCO_3)_2}=17,3\%$