Một nguyên tử y có tổng số các loại hạt là 40,trong đó số hạt không mang điện là 35% hỏi số proton của nguyên tử y là bao nhiêu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi số hạt proton = Số hạt electron = p
Gọi số hạt notron = n
Hạt mang điện là proton, electron
Hạt không mang điện là notron
Bài 1 :
Ta có :
$2p + n = 40$ và $2p - n = 12$
Suy ra p = 13 ; n = 14
Bài 2 :
Ta có :
$2p + n = 58$ và $n - p = 1$
Suy ra p = 19 ; n = 20
Bài 3 :
Ta có :
$2p + n = 48$ và $2p = 2n$
Suy ra p = n = 16

Gọi tổng số hạt proton , electron , notron của 2 nguyên tử X và Y là M
gọi số proton , electron , notron của M lần lượt là p ,e ,n . TA CÓ :
p+e+n = 76 => 2p + n = 76 ( vì nguyên tử trung hòa về điện) (1)
do tổng số hạt mang điện tích lớn hơn tổng số hạt không mang điện tích là 24 hạt
=> 2p - n = 24
Kết hợp (1) ta được 2p = 50 => tổng số hạt mang điện tích của 2 nguyên tử X và Y là 50 hạt (*)
Từ đề ra ta lại có :
số hạt mang điện(Y) - số hạt mang điện(X) = 18(**)
Từ (*) và (**) => số hạt mang điện của Y = 34 (hạt) => Y có 17 proton => Y là nguyên tố Clo
=> số hạt mang điện của X = 16 (hạt) => X có 8 proton => X là nguyên tố Oxi
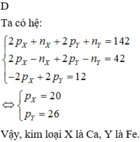
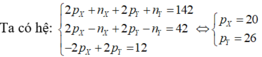
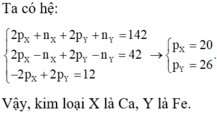
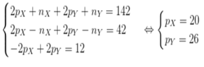
Tổng số các loại hạt là 40
\(2p+n=40\left(1\right)\)
Số hạt không mang điện là 35% .
\(\dfrac{n}{40}\cdot100\%=35\%\)
\(\Leftrightarrow n=14\)
\(\left(1\right):p=e=\dfrac{40-14}{2}=13\left(hạt\right)\)
1. Ta có: Tổng sô hạt của nguyên tử R là 40
⇒⇒ p + e + n = 40 ⇒⇒ 2p + n = 40 (1)
Vì số hạt không mang điện tích chiếm 35%
⇒%n=35%⇒n=35.40100=14(2)⇒%n=35%⇒n=35.40100=14(2)
Ta thế (2) vào (1) ta được:
2p + n = 40
⇔⇔ 2p + 14 = 40
⇔⇔ 2p = 26
⇔⇔ p = 13
⇒⇒ p = e = 13 ; n = 14