Cho 160 gam dung dịch Copper (II) sulfate 10% tác dụng hết VmL dung dịch sodium hydroxide 1M. Thu được dung dịch A và kết tủa B. Lọc lấy kết tủa B nung đến khối lượng không đổi thu được chất rắn D. a. Viết các PTHH xảy ra b. Tính V c. Tính khối lượng chất rắn D
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

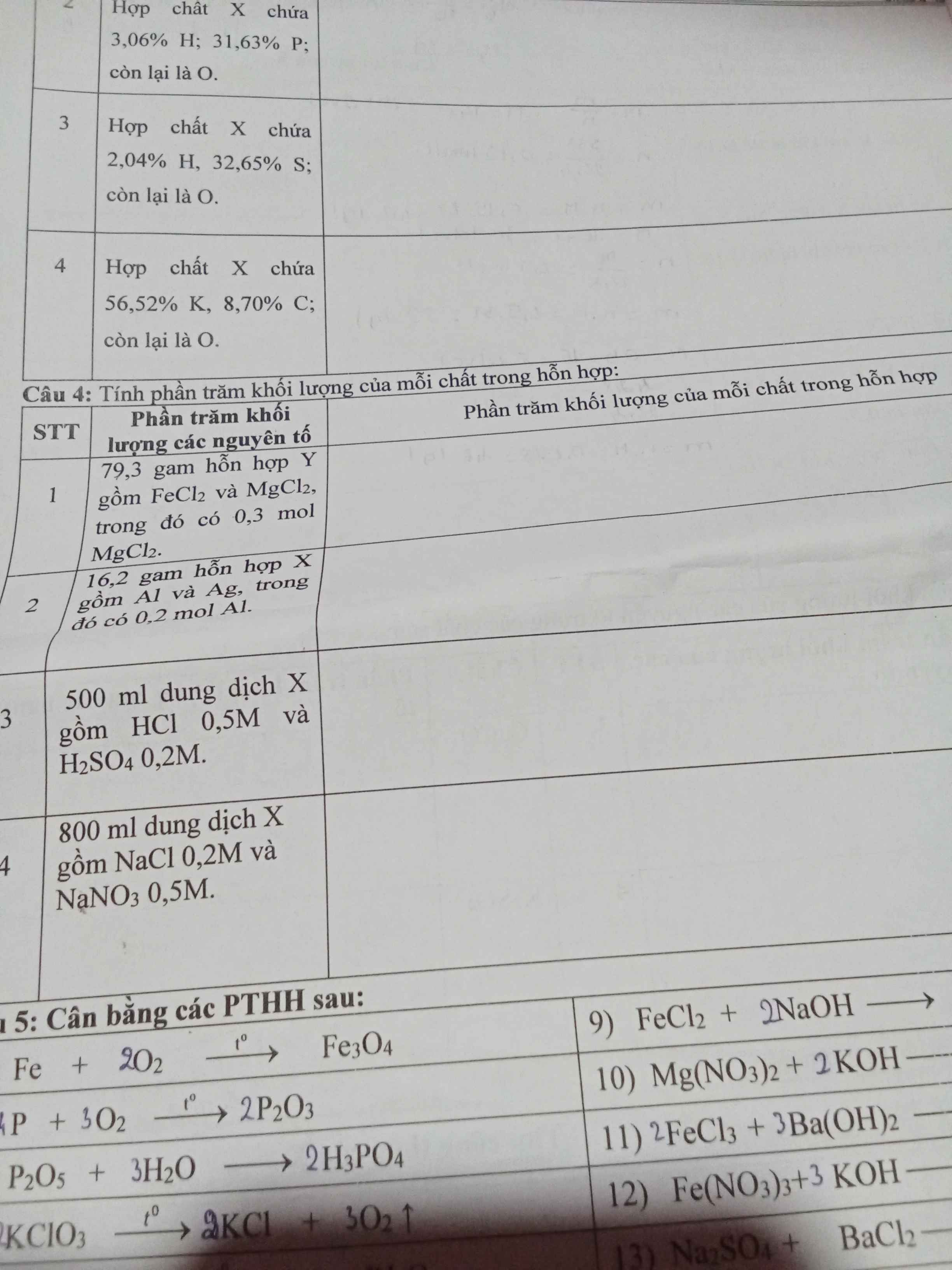
Câu 4:
\(\%m_{MgCl_2}=\dfrac{0,3.95.100\%}{79,3}=35,94\%,\%m_{FeCl_2}=100\%-35,94\%=64,06\%,\)
2) \(\%m_{Al}=\dfrac{0,2.27.100\%}{16,2}=33,33\%\\ \%m_{Ag}=100\%-33,33=66,67\%\)
3) \(n_{HCl}=0,5.0,5=0,25;n_{H_2SO_4}=0,2.0,5=0,1\left(mol\right)\)
\(\%m_{HCl}=\dfrac{0,25.36,5.100\%}{0,25.36,5+0,1.98}=48,22\%\\ \%m_{H_2SO_4}=100\%-48,22\%=51,78\%\)
4)
\(n_{NaCl}=0,2.0,8=0,16\left(mol\right),n_{NaNO_3}=0,5.0,8=0,4\left(mol\right)\Rightarrow\%m_{NaCl}=\dfrac{0,16.58,5.100\%}{0,16.58,5+0,4.85}=21,59\%\Rightarrow\%m_{NaNO_3}=100\%-21,59\%=78,41\%\)

1)
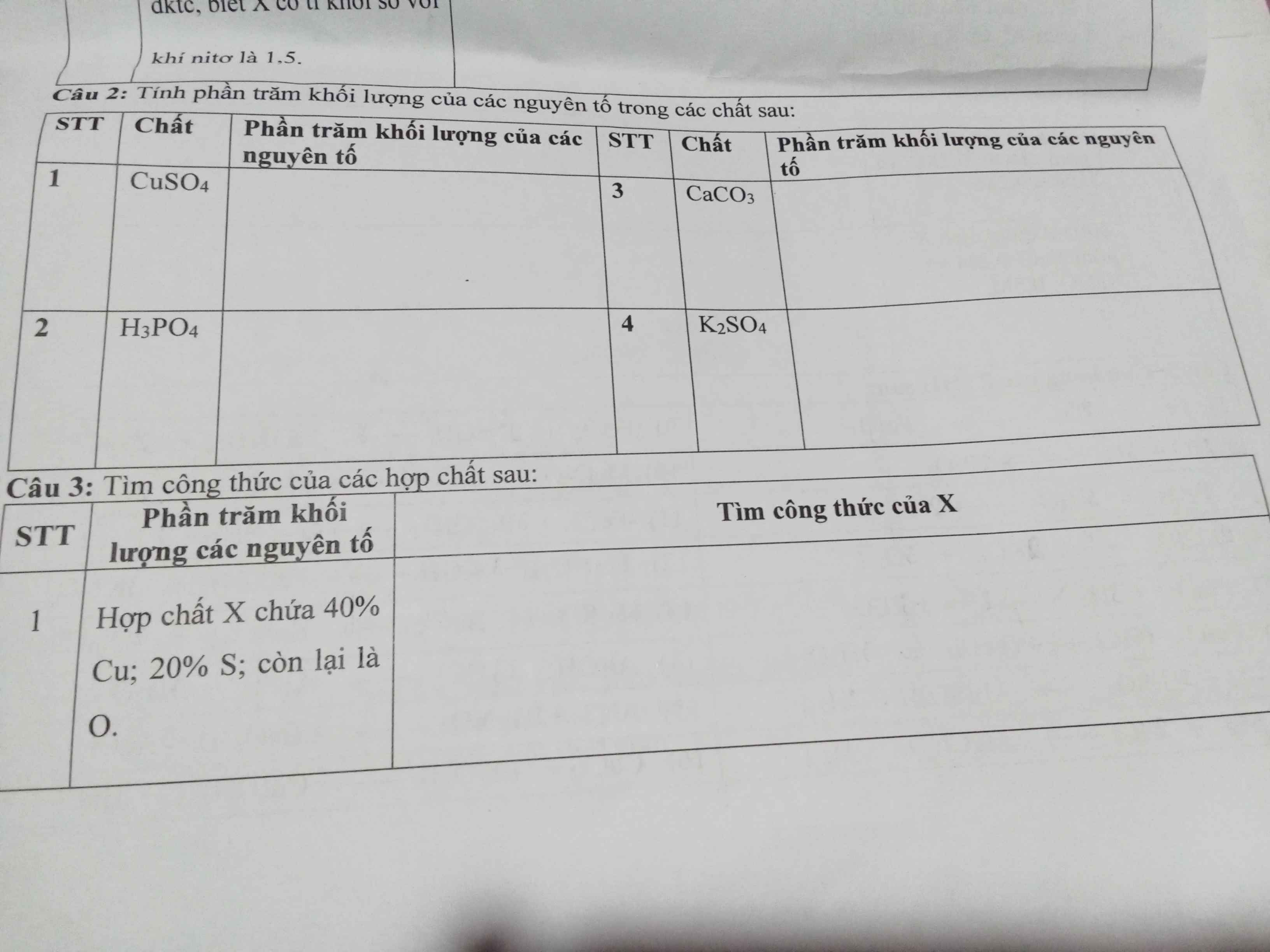
\(\%_{Cu}=\dfrac{64.100\%}{64+96}=40\%,\%_S=\dfrac{32.100\%}{64+96}=20\%,\%_O=100\%-40\%-20\%=40\%\)
2)
\(\%_H=\dfrac{3.100\%}{3+31+16.4}=3,06\%,\%_P=\dfrac{31.100\%}{3+31+16.4}=31,63\%\\ \%_O=100\%-3,06\%-31,63\%=65,31\%\)
3)
\(\%_{Ca}=\dfrac{40.100\%}{100}=40\%,\%_C=\dfrac{12.100\%}{100}=12\%,\%_O=\dfrac{16.100\%}{100}=16\%\text{_}\)
4)
\(\%_K=\dfrac{39.100\%}{39.2+32+16.4}=22,41\%,\%_S=\dfrac{32.100\%}{39.2+32+16.4}=18,39\%\\ \%_O=100\%-22,41\%-18,39\%=59,2\%\)
Câu 3:
Gọi Công thức hóa học của X là: \(Cu_xS_yO_z\)
Ta có:;
\(x:y:z=\dfrac{40}{64}:\dfrac{20}{32}:\dfrac{40}{16}=0,625:0,625:2,5=1:1:4\)
=> CTHC: \(CuSO_4\)

a, Lã kẽm có một lớp Sắt màu xám bao phủ bên ngoài.
PTHH:
\(Zn+FeCl_2\rightarrow ZnCl_2+Fe\)
0,03 0,03 0,03 0,03
Gọi nZn = nFe = a(mol)
0,27g = 65a - 56a
=> a = 0,03(mol)
b, \(m_{Zn\left(pư\right)}=0,03.65=1,95\left(g\right)\)
\(m_{Fe\left(sra\right)}=0,03.56=1,68\left(g\right)\)
c, \(m_{FeCl_2}=0,03.127=3,81\left(g\right)\)
\(m_{dd}=1,95+200=201,95\left(g\right)\)
\(C\%FeCl_2=\dfrac{3,81}{201,95}.100\%=1,89\left(\%\right)\)

a.
C% = \(\dfrac{m_{ct}}{m_{dd}}\) ⇒ \(m_{ct}\) = 250 . \(\dfrac{7,3}{100}\) = 18,25 gam
⇒\(n_{HCl}\) = 0,5 mol
PTHH: Mg + 2HCl →MgCl2 + H2
⇒\(n_{Mg}\) = 0,25 mol
⇒\(m_{Mg}\)= 12 gam
b. C% = \(\dfrac{m_{ct}}{m_{dd}}\) = \(\dfrac{m_{Mg}}{m_{Mg}+m_{HCl}}\) = 4,58%
a) Khối lượng HCl tham gia PƯ là:
mct= mdd.\(\dfrac{C\%}{100\%}\)= 250. \(\dfrac{7,3\%}{100\%}\)= 18,25 (g)
Số mol HCl tham gia PƯ là:
n=m:M= 18,25 : 36,5 = 0,5 (mol)
PTHH: Mg + 2HCl -> MgCl2 + H2
số mol Mg tham gia PƯ là
0,5 . 1 : 2 = 0,25 (mol)
Khối lượng Mg tham gia PƯ là
m= n.M = 0,25 . 24 = 6 (g)
b) Số mol MgCl2 là:
0,5 . 1 : 2 = 0,25 (mol)
Khối lượng MgCl2 thu được là
m = n.M = 0,25 . 95 = 23,75 (g)
C% MgCl2 trong dd là
23,75 : (250 + 6) . 100% \(\approx\) 9,3%

số mol Cu điều chế được là:
n = m:M = 9,6 : 64 = 0,15 (mol)
PTHH: CuCl2 + Fe -> FeCl2 + Cu
Khối lượng Fe cần dùng là:
m=n.M= 0,15 . 56 = 8,4 (g)
Khối lượng CuCl2 cần dùng là:
m=n.M= 0,15 . 135 = 20,25 (g)
nồng độ % CuCl2 trong dd là:
20,25 : 200 . 100% = 10,125 (%)

Ta có: \(n_{Cu}=\dfrac{8,32}{64}=0,13\left(mol\right)\)
\(n_{O_2}=\dfrac{6,81725}{24,79}=0,275\left(mol\right)\)
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
Theo PT: \(n_{O_2}=\dfrac{2}{3}n_{Fe}+\dfrac{1}{2}n_{Cu}\) \(\Rightarrow n_{Fe}=0,315\left(mol\right)\)
\(\Rightarrow a=0,315.56=17,64\left(g\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{Fe_3O_4}=\dfrac{1}{3}n_{Fe}=0,105\left(mol\right)\\n_{CuO}=n_{Cu}=0,13\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%n_{Fe_3O_4}=\dfrac{0,105}{0,105+0,13}.100\%\approx44,7\%\\\%n_{CuO}\approx55,3\%\end{matrix}\right.\)
\(\overline{M_{hh}}=\dfrac{m_{Fe_3O_4}+n_{CuO}}{n_{Fe_3O_4}+n_{CuO}}=\dfrac{0,105.232+0,13.80}{0,105+0,13}=147,91\left(g/mol\right)\)

Gọi x, y là số mol của Mg và Cu.
Theo đề có: \(\dfrac{24x}{64y}=\dfrac{3}{4}\Leftrightarrow x-2y=0\left(1\right)\)
Lại có: \(24x+64y=11\left(2\right)\)
Từ (1), (2) giải hệ phương trình ta được: \(\left\{{}\begin{matrix}x=\dfrac{11}{56}\\y=\dfrac{11}{112}\end{matrix}\right.\)
BTNT:
\(n_{MgO}=n_{Mg}=\dfrac{11}{56},n_{CuO}=n_{Cu}=\dfrac{11}{112}\)
\(\Rightarrow m_{sp}=m_{MgO}+m_{CuO}=\dfrac{11}{56}.40+\dfrac{11}{112}.80=15,7\left(g\right)\)
\(n_{O_2}=\dfrac{1}{2}\left(x+y\right)=\dfrac{1}{2}\left(\dfrac{11}{56}+\dfrac{11}{112}\right)=0,15\left(mol\right)\Rightarrow V_{O_2}=0,15.22,4=3,36\left(l\right)\)

a, \(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_{2\downarrow}+Na_2SO_4\)
\(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
b, \(m_{CuSO_4}=160.10\%=16\left(g\right)\Rightarrow n_{CuSO_4}=\dfrac{16}{160}=0,1\left(mol\right)\)
Theo PT: \(n_{NaOH}=2n_{CuSO_4}=0,2\left(mol\right)\Rightarrow V_{NaOH}=\dfrac{0,2}{1}=0,2\left(l\right)=200\left(ml\right)\)
c, \(n_{CuO}=n_{Cu\left(OH\right)_2}=n_{CuSO_4}=0,1\left(mol\right)\)
\(\Rightarrow m_{CuO}=0,1.80=8\left(g\right)\)