Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- muối tác dụng với kim loại tạo ra muối mới và kim loại mới (với kim loại tham gia phản ứng mạnh hơn kim loại có trong muối)
- muối tác dụng với aicd tạo thành muối mới và acid mới (với sản phẩm là chất khí, chất kết tủa hoặc nước)
- muối tác dụng với base tạo thành muối mới và base mới (với sản phảm là chất khí, chất kết tủa hoặc nước)
- muối tác dụng với muối tạo thành 2 muối mới (với sản phẩm là chất khí, chất kết tủa hoặc nước)

Mình hệ thống lại tính chất hóa học của các loại oxit để bạn dễ học nhé 👇
1. Oxit axit (thường là oxit của phi kim hoặc kim loại có số oxi hoá cao, ví dụ: SO₂, CO₂, P₂O₅, N₂O₅, …)
- Tác dụng với nước → tạo dung dịch axit.
\(S O_{3} + H_{2} O \rightarrow H_{2} S O_{4}\) - Tác dụng với bazơ → tạo muối và nước.
\(C O_{2} + C a \left(\right. O H \left.\right)_{2} \rightarrow C a C O_{3} \downarrow + H_{2} O\)
2. Oxit bazơ (thường là oxit của kim loại, ví dụ: Na₂O, CaO, CuO, Fe₂O₃, …)
- Tác dụng với nước → tạo dung dịch bazơ (nếu oxit tan).
\(C a O + H_{2} O \rightarrow C a \left(\right. O H \left.\right)_{2}\) - Tác dụng với axit → tạo muối và nước.
\(C u O + 2 H C l \rightarrow C u C l_{2} + H_{2} O\)
3. Oxit lưỡng tính (ZnO, Al₂O₃, Cr₂O₃, …)
- Tác dụng với axit → tạo muối và nước.
\(Z n O + 2 H C l \rightarrow Z n C l_{2} + H_{2} O\) - Tác dụng với bazơ mạnh (khi nung nóng hoặc dung dịch kiềm đặc) → tạo muối và nước.
\(Z n O + 2 N a O H \rightarrow N a_{2} Z n O_{2} + H_{2} O\)
4. Oxit trung tính (CO, NO, N₂O, …)
- Không tác dụng với axit, bazơ, muối, cũng không tác dụng với nước.
✅ Tóm gọn:
- Oxit axit + bazơ → muối + nước.
- Oxit bazơ + axit → muối + nước.
- Oxit lưỡng tính + axit/bazơ → muối + nước.
- Oxit trung tính: hầu như không phản ứng.

Tham khảo :
Đề xuất thí nghiệm:
Chuẩn bị:
- Dụng cụ: Ống nghiệm, ống hút nhỏ giọt, giá đỡ thí nghiệm.
- Hoá chất: Các dung dịch acid: HCl, HNO3, H2SO4; giấy quỳ tím; nước cất.
Tiến hành:
- Lấy 4 ống nghiệm, đánh số từ 1 đến 4.
- Cho vào ống nghiệm 1 khoảng 2 mL dung dịch HCl, ống nghiệm 2 khoảng 2 mL dung dịch HNO3, ống nghiệm 3 khoảng 2 mL dung dịch H2SO4, ống nghiệm 4 khoảng 2 mL nước cất.
- Sau đó cho lần lượt vào mỗi ống nghiệm 1 mẩu quỳ tím. Quan sát sự đổi màu của quỳ tím và rút ra nhận xét.

a, Dấu hiệu của pư: Có hiện tượng sủi bọt khí.
b, Sodium hydrogen carbonate + Acetic acid → Acetate sodium + Nước + Carbondioxide
- Chất tham gia: Sodium hydrogen carbonate và Acetic acid
- Sản phẩm: Acetate sodium, nước và Carbondioxide
c, Theo ĐLBT KL, có: mNaHCO3 + mCH3COOH = mCH3COONa + mH2O + mCO2
⇒ mCH3COONa = 8,4 + 6 - 1,8 - 4,4 = 8,2 (g)

Trả lời:
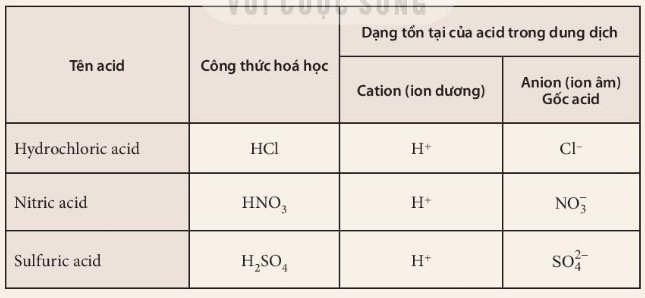
1. Công thức hoá học của các acid đều có chứa nguyên tử H.
2. Dạng tồn tại của acid trong dung dịch đều chứa cation (ion dương) H+.
3. Acid là những hợp chất trong phân tử có nguyên tử hydrogen liên kết với gốc acid. Khi tan trong nước, acid tạo ra ion H+.
1. Đều có nguyên tử H
2. Dạng tồn tại đều chưa ion H+
3. Acid là những hợp chất trong phân tử có nguyên tử hydrogen liên kết với gốc acid. Khi tan trong nước, acid tạo ra ion H+
Bạn đã tóm tắt rất tốt về các đặc điểm của acid. Hãy để tôi tổng kết lại những điểm chính:
Bạn đã tóm tắt rất đầy đủ và chính xác về các đặc điểm cơ bản của acid. Đây là những kiến thức quan trọng cần nắm vững về các hợp chất acid.