Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

F O Cl N
Độ âm điện: 3,98 3,44 3,16 3,14
Nhận xét: tính phi kim giảm dần.
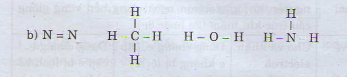
N2 CH4 H2O NH3
Hiệu độ âm điện: 0 0,35 1,24 0,84
Phân tử N2, CH4 có liên kết cộng hóa trị không phân cực. Phân tử H2O có liên kết cộng hóa trị phân cực mạnh nhất trong dãy.

a) PTHH: 2KClO3 → 2KCl + 3O2
b) Theo ĐLBTKL:
mKClO3 = mKCl + mO2
=> mKCl = mKClO3 – mO2 = 24,5 – 9,6=14,9 g

a.
2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2
nAl (dư, trong ½ phần) = 2/3.nH2 = 2/3.8,96/22,4 = 4/15 mol
nH2 = 26,88/22,4 = 1,2 mol
2Al + 6HCl = 3H2 + 2AlCl3
4/15..............0,4 mol
Fe + 2HCl = H2 + FeCl2
0,8..............0,8 mol
Phần không tan chỉ gồm Fe
Ta có : mFe = 44,8%m1 => m1 = m2 = 0,8.56.100/44,8 = 100g
b.
nFe (trong cả 2 phần) = 0,8.2 = 1,6 mol
2Al + Fe2O3 = Al2O3 + 2Fe
1,6....0,8.........0,8.........1,6 mol
=> mFe2O3 (ban đầu) = 0,8.160 = 128g
nAl (ban đầu) = nAl (ph.ư) + nAl (dư, trong 2 phần) = 1,6 + 2.4/15 = 32/15 mol
=> mAl (ban đầu) = 27.32/15 = 57,6g
sai rồi bạn ơi . 2 phần này có bằng nhau đâu mà làm theo kiểu v @@

1. Khối lượng chất tan trong dung dịch 1 = m1C1/100 (g)
Khối lượng chất tan trong dung dịch 2 = m2C2/100 (g).
mà (m3 = m1 + m2)
Khối lượng chất tan trong dung dịch 3 = (m1 + m2)C3/100 (g).
Áp dụng định luật bảo toàn khối lượng ta có: C3.(m1 + m2) = C1.m1 + C2.m2
2. Đặt công thức của muối là: MgSO4.nH2O
Khối lượng MgSO4 trong dung dịch ban đầu: 200.35,1/135,1 = 51,961 gam
Ở 20oC:
- 135,1 gam dung dịch có chứa 35,1 gam MgSO4
- (200+2 – m) gam dung dịch có chứa (51,961 + 2 – 3,16) gam MgSO4.
Từ đó tìm được m = 6,47 gam
Khi nung muối ta có:
MgSO4.nH2O → MgSO4 + nH2O (1)
Theo (1) ta được mH2O = 6,47 – 3,16 = 3,31 gam
=> 3,16/120.18n = 3,31 => n = 7
Vậy muối là: MgSO4.7H2O
tham khảo nhé

a) Tên hóa học của phân bón:

b) Nhóm phân bón dạng đơn: KCl, NH4NO3, NH4Cl, (NH4)2SO4, Ca3(PO4)2, Ca(H2PO4)2.
Nhóm phân bón dạng kép: NH4H2PO4, KNO3.
c) Để có phân bón kép NPK ta trộn các phan bón MH4NO3, NH4H2PO4 và KCl theo tỉ lệ thích hợp.
a) Tên hóa học của phân bón: KCl: Kali clorua; NH4NO3: Amoni nitrat; NH4Cl: Amoni clorua; (NH4)2SO4: Amoni sunphat; Ca3(PO4)2: Canxi photphat; Ca(H2PO4)2: Canxi đihiđrophotphat; (NH4)2HPO4: Điamoni hiđrophotphat; KNO3: Kali nitrat.
b) Hai nhóm phân bón:
– Phân bón đơn: KCl, NH4NO3, NH4Cl, (NH4)2SO4, Ca3(PO4)2, Ca(H2PO4)2.
– Phân bón kép: (NH4)2HPO4, KNO3.
c) Phân bón kép NPK: Trộn các phân bón NH4NO3, (NH4)2HPO4 và KCl theo tỉ lệ thích hợp, được phân bón NPK.

a) Đặt công thức oxít M2On
Ptpư: M2On + nH2SO4 → M2(SO4)n + nH2O
mol 1 n 1
mddH2SO4 = n.98.100/10 = 980n gam
mdd muối = 2M + 996n (gam)
→ C% muối = (2M + 96n) : (2M + 996n) = 0,11243
→ M = 9n → M = 27 (Al)
→ Công thức oxít: Al2O3
b) ptpứ: Al2O3 ---> 2Al + 3/2O2
Al2O3 + 2NaOH ---> 2NaAlO2 + H2O
Al2(SO4)3 + 3Na2CO3 + 3H2O ---> 2Al(OH)3 + 3Na2SO4 + 3CO2

a) Đặt công thức oxít M2On
Ptpư: M2On + nH2SO4 --->M2(SO4)n + nH2O
mol 1 n 1
mddH2SO4 = n.98.100/10 = 980n gam
mdd muối = 2M + 996n (gam)
→ C% muối = (2M + 96n) : (2M + 996n) = 0,11243
→ M = 9n → M = 27 (Al)
→ Công thức oxít: Al2O3
b) ptpứ: Al2O3 ------> 2Al + 3/2O2
Al2O3 + 2NaOH --->2NaAlO2 + H2O
Al2(SO4)3 + 3Na2CO3 + 3H2O --->2Al(OH)3+ 3Na2SO4 + 3CO2

Câu 1:
c) CM (HCl) dư = \(\frac{0,11}{0,25}\) = 0,44 (M)
ddAgồm \(\begin{cases}HCl:0,11mol\\AlCl_3:0,1mol\\CuCl_2:0,045mol\end{cases}\)
d) Các pư xảy ra theo thứ tự:
Mg + 2HCl \(\rightarrow\) MgCl2 + H2 (1)
Mg + CuCl2 \(\rightarrow\) MgCl2 + Cu (2)
3Mg + 2AlCl3 \(\rightarrow\) 3MgCl2 + 2Al (3)
Giả sử CR chỉ gồm Cu => ko xảy ra pt(3)
nCu = \(\frac{1,92}{64}\) = 0,03 (mol)
Theo pt(1) nMg= \(\frac{1}{2}\) nHCl = 0,055 (mol)
PT(2) nCu < nCuCl2 (0,03 < 0,045 )
=> CuCl2 dư
=> Giả sử đúng
mMg = (0,055 + 0,03) . 24 =2,04 (g)
Câu 3: a) Hiện tượng: Khi sục khí Cl2 vào nước vừa có tính chất vật lí , vừa tính chất hóa học:
- Vật lí: Có một phần khí tan trong nước
- Hóa học: Có chất mới tạo thành
PT: Cl2 + H2O \(\rightarrow\) HCl + HClO
b) Hiện tượng: tạo thành chất khí, cháy ở nhiệt độ cao hoặc có ánh sáng
PT: Cl2 + H2 \(\underrightarrow{t^0}\) 2HCl (khí)

Câu 2. (3.0 điểm)
Trích mẫu thử, đánh số thứ tự và tiến hành thí nghiệm.
Cho lần lượt các mẫu thử tác dụng với nhau, quan sát hiện tượng.
Mẫu thử nào cho kết quả ứng với 1↑ => HCl
Mẫu thử nào cho kết quả ứng với 1↓ => NaOH
Mẫu thử nào cho kết quả ứng với 2↓ => Ba(OH)2
Mẫu thử nào cho kết quả ứng với 2↓ và 1↑ => K2CO3
Mẫu thử nào cho kết quả ứng với 3↓ => MgSO4
Các PTHH:
2HCl + K2CO3 → 2KCl + H2O
2NaOH + MgSO4 → Na2SO4 + Mg(OH)2
Ba(OH)2 + K2CO3 → BaCO3 + 2KOH
Ba(OH)2 + MgSO4 → Mg(OH)2 + BaSO4
K2CO3 + MgSO4 → MgCO3 + K2SO4

Để tính độ dinh dưỡng của phân đạm, phân lân, và phân kali, ta sẽ thực hiện theo từng phần.
a. Tính độ dinh dưỡng của đạm và kali trong KNO₃
KNO₃ có công thức hóa học là Kali nitrat, bao gồm:
Tính phần trăm N và K trong KNO₃
Tổng khối lượng mol của KNO₃:
\(�_{� � �_{3}} = 39 + 14 + 48 = 101 \&\text{nbsp};\text{g}/\text{mol}\)
\(\% � = \left(\right. \frac{�_{�}}{�_{� � �_{3}}} \left.\right) \times 100 = \left(\right. \frac{14}{101} \left.\right) \times 100 \approx 13.86 \%\)
\(\% � = \left(\right. \frac{�_{�}}{�_{� � �_{3}}} \left.\right) \times 100 = \left(\right. \frac{39}{101} \left.\right) \times 100 \approx 38.61 \%\)
Kết quả phần a:
b. Tính độ dinh dưỡng của loại phân bón superphosphate kép
Superphosphate kép chứa 69,62% Calcium dihydrophosphate (Ca(H₂PO₄)₂) theo khối lượng.
Tính phần trăm P₂O₅ trong Ca(H₂PO₄)₂
Tổng khối lượng mol của Ca(H₂PO₄)₂:
\(�_{� � \left(\right. �_{2} � �_{4} \left.\right)_{2}} = 40 + 4 + 62 + 128 = 234 \&\text{nbsp};\text{g}/\text{mol}\)
\(\% �_{2} �_{5} = \left(\right. \frac{�_{�_{2} �_{5}}}{�_{� � \left(\right. �_{2} � �_{4} \left.\right)_{2}}} \left.\right) \times 100 = \left(\right. \frac{142}{234} \left.\right) \times 100 \approx 60.68 \%\)
\(Độ\&\text{nbsp};\text{dinh}\&\text{nbsp};\text{d}ưỡ\text{ng}\&\text{nbsp};\text{c}ủ\text{a}\&\text{nbsp};\text{P}_{2}\text{O}_{5} = 69.62 \% \times 60.68 \% \approx 42.24 \%\)
Kết quả phần b: