Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

`Cl_2`
Mỗi nguyên tử `Cl` có `7e` ở lớp ngoài cùng. Để có cấu trúc electron bền vững giống khí hiếm `Ar`, `2` nguyên tử `Cl` đã liên kết với nhau bằng cách mỗi nguyên tử `Cl` góp chung `1e` ở lớp ngoài cùng tạo thành `1` cặp electron dùng chung.
`N_2`
Mỗi nguyên tử `N` có `5e` ở lớp ngoài cùng. Để có cấu trúc electron bền vững giống khí hiếm `Ne`,`2` nguyên tử `N` đã liên kết với nhau bằng cách mỗi nguyên tử `N` góp chung `3e` ở lớp ngoài cùng tạo thành `3` cặp electron dùng chung.

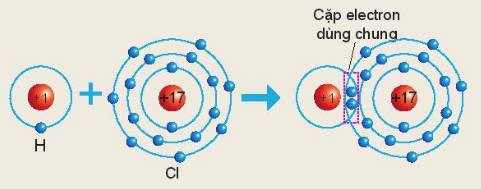
Nguyên tử `Cl` dùng chung `1` cặp electron với nguyên tử `H`
`->` Trong phân tử muối `HCl,` nguyên tử nguyên tố `Cl` sẽ có hóa trị là `I`.

`-` Khi hình thành liên kết cộng hóa trị trong phân tử `CO_2`, các nguyên tử đã liên kết với nhau như sau:
Mỗi nguyên tử `C` và `O` lần lượt có `12e` và `16e`. Để hình thành phân tử `CO_2`, nguyên tử `C` đã liên kết với `2` nguyên tử `O` bằng cách nguyên tử `C` góp chung với mỗi nguyên tử `O` là `2e` ở lớp ngoài cùng tạo thành các cặp electron dùng chung.
`NH_3`
Mỗi nguyên tử `N` và `H` lần lượt có `14e` và `1e`. Để hình thành phân tử ammonia, nguyên tử `N` liên kết với nguyên tử `H` bằng cách nguyên tử `N` góp chung với nguyên tử `H` là `1e` ở lớp ngoài cùng tạo thành `3` cặp electron dùng chung.

Khi tạo thành phân tử nước, nguyên tử O góp 2 electron, mỗi nguyên tử H góp 1 electron. Như vậy, giữa nguyên tử O và nguyên tử H có 1 đôi electron dùng chung. Hạt nhân nguyên tử O và H cùng hút đôi electron dùng chung, liên kết với nhau tạo ra phân tử nước.

- Quá trình tạo thành liên kết cộng hóa trị trong phân tử hydrogen:
+ Nguyên tử H chỉ có 1 electron và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
+ Khi hai nguyên tử H liên kết với nhau, mỗi nguyên tử góp chung 1 electron để tạo ra đôi electron dùng chung.
+ Hạt nhân của hai nguyên tử H cùng hút đôi electron dùng chung và liên kết với nhau tạo thành phân tử hydrogen.
- Quá trình tạo thành liên kết cộng hóa trị trong phân tử oxygen:
+ Nguyên tử O có 6 electron lớp ngoài cùng, cần thêm 2 electron để có lớp vỏ bền vững tương tự khí hiếm.
+ Khi hai nguyên tử O liên kết với nhau, mỗi nguyên tử góp 2 electron để tạo ra hai cặp electron dùng chung.
+ Hạt nhân của hai nguyên tử O cùng hút các cặp electron dùng chung và liên kết với nhau tạo thành phân tử oxygen.

Nguyên tử Cl có 7 electron lớp ngoài cùng và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
Từ đây em tự vẽ khi mỗi nguyên tử góp 1e dùng chung

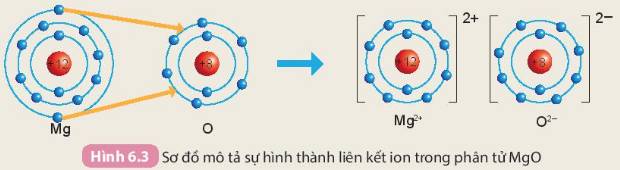
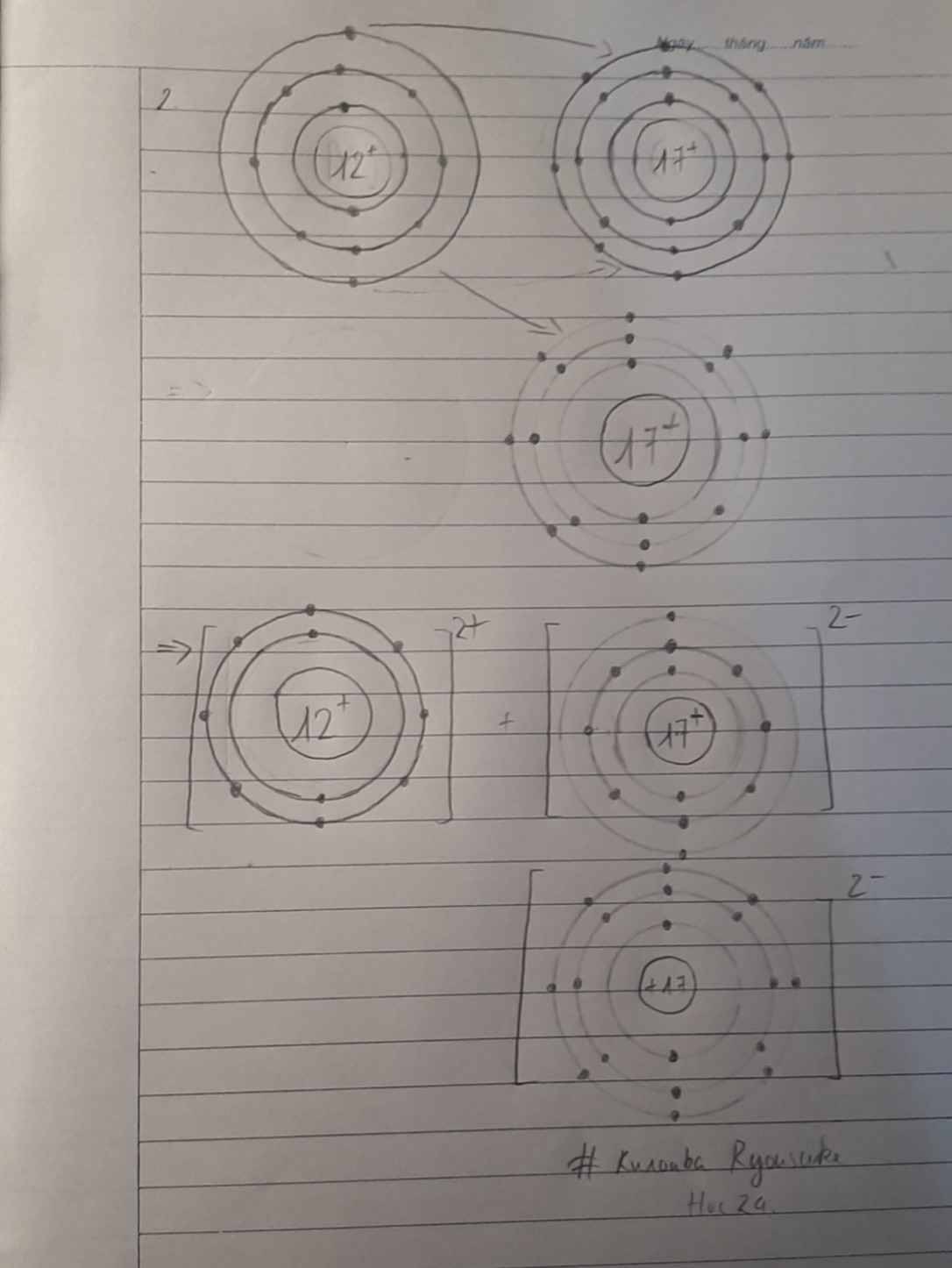
Khi hình thành phân tử `MgO,` các nguyên tử đã có sự nhường nhận `e` như sau:
`-` Nguyên tử `Mg` nhường `2e` ở lớp ngoài cùng cho nguyên tử `O` để tạo thành ion dương \(Mg^{2+}\) có vỏ bền vững giống khí hiếm `Ne`.
`-` Nguyên tử `O` nhận `2e` vào lớp ngoài cùng từ nguyên tử `Mg` để tạo thành ion âm \(O^{2-}\) có vỏ bền vừng giống khí hiếm `Ne`.
Hai ion trái dấu hút nhau, hình thành nên liên kết ion trong phân tử `MgO`.
Đây là mô tả sự hình thành liên kết cộng hóa trị trong phân tử khí chlorine (Cl2) và khí nitrogen (N2):
1. Phân tử khí chlorine (Cl2)
2. Phân tử khí nitrogen (N2)
Tóm lại: