Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a,n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
bđ 0,3 0,4
pư 0,3 0,15
sau pư 0 0,25 0,3
=> H2 hết, O2 dư
\(m_{O_2\left(dư\right)}=0,25.32=8\left(g\right)\)
b) \(A_{H_2O}=0,3.6.10^{23}=1,8.10^{23}\left(phân.tử\right)\)
c) \(m_{O_2\left(pư\right)}=0,15.32=4,8\left(g\right)\)
PTHH: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,3<-------------------------------------0,15
\(\rightarrow m_{KMnO_4}=0,3.158=47,4\left(g\right)\)

a, PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Ta có: \(n_{H_2}=n_{O_2}=\dfrac{6,1975}{24,79}=0,25\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,25}{2}< \dfrac{0,25}{1}\), ta được O2 dư.
Theo PT: \(n_{O_2\left(pư\right)}=\dfrac{1}{2}n_{H_2}=0,125\left(mol\right)\)
\(\Rightarrow n_{O_2\left(dư\right)}=0,25-0,125=0,125\left(mol\right)\)
\(\Rightarrow V_{O_2\left(dư\right)}=0,125.24,79=3,09875\left(l\right)\)
b, Theo PT: \(n_{H_2O}=n_{H_2}=0,25\left(mol\right)\)
\(\Rightarrow m_{H_2O}=0,25.18=4,5\left(g\right)\)
c, PT: \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
Theo PT: \(n_{KClO_3}=\dfrac{2}{3}n_{O_2}=\dfrac{1}{6}\left(mol\right)\)
\(\Rightarrow m_{KClO_3}=\dfrac{1}{6}.122,5\approx20,42\left(g\right)\)

bạn ơi mk đang mắc câu này bạn có thể trả lời giúp mình đc ko
3) Cho 6 gam Mg phản ứng 2,24 lít khí oxi(đktc).Sau phản ứng thu được magie oxit(MgO)
a) viết phường trình hóa học
2Mg + O2 → 2MgO
b) tính khối lượng MgO được tạo thành
mO2 = 2,24/ 22,4 . 16 = 1,6(g)
mMgO = mO2 + mMg = 1,6 + 6 = 7,6(g)

a. \(n_{H_2}=\dfrac{1.12}{22,4}=0,05\left(mol\right)\)
\(n_{O_2}=\dfrac{2.24}{22,4}=0,1\left(mol\right)\)
PTHH : 2H2 + O2 ---to---> 2H2O
0,05 0,025 0,05
b. Ta thấy : 0,05 < 0,1 => H2 đủ , O2 dư
\(V_{O_2\left(dư\right)}=\left(0,1-0,025\right).22,4=1,68\left(l\right)\)
c. \(m_{H_2O}=0,05.18=0,9\left(g\right)\)
Ta có
nH2 = 1,12 / 22,4 = 0,05 ( mol )
nO2 = 0,1 ( mol )
2H2 + O2 ---to ---> 2H2O
có : 0,05 0,1
pư : 0,05 0,025 0,05
dư : 0 0,075
Xét tỉ lệ : 0,05 / 2 < 0,1 / 1 , ta được O2 dư
=> nO2 dư = 0,1 - 0,025 = 0,075 ( mol )
=> V = 0,075 . 22,4 = 1,68 ( l )
mH2O = 0,05 . 18 = 0,9 ( g )

Câu 2:
PTHH: 4P+ 5O2 -to-> 2P2O5
Ta có:
\(n_P=\frac{3,1}{31}=0,1\left(mol\right);\\ n_{O_2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(\frac{0,1}{4}>\frac{0,1}{5}\)
b) => P dư, O2 hết nên tính theo \(n_{O_2}\)
=> \(n_{P\left(phảnứng\right)}=\frac{4.0,1}{5}=0,08\left(mol\right)\\ =>n_{P\left(dư\right)}=0,1-0,08=0,02\left(mol\right)\)
Khối lượng P dư:
\(m_{P\left(dư\right)}=0,02.31=0,62\left(g\right)\)
c) Theo PTHH và đề bài, ta có:
\(n_{P_2O_5}=\frac{2.0,1}{5}=0,04\left(mol\right)\)
Khối lượng P2O5:
\(m_{P_2O_5}=0,04.142=5,68\left(g\right)\)
1) PTHH: Zn+2HCl->ZnCl2+H2
b) \(n_{Zn}=\frac{13}{65}=0,2mol\)
\(n_{H_2}=n_{Zn}=0,2mol\Rightarrow V_{H_2}=0,2.22,4=4,48l\)c) 2H2+O2=>2H2O
\(n_{O_2}=\frac{1}{2}.n_{H_2}=\frac{1}{2}.0,2=0,1mol\Rightarrow V_{O_2}=0,1.22,4=2,24l\Rightarrow V_{kk}=5.V_{O_2}=5.2,24=11,2l\)d) H2+CuO=>Cu+H2O
\(n_{CuO}=\frac{24}{80}=0,3mol\)
Vì: 0,3>0,2=> CuO dư
\(n_{Cu}=n_{H_2}=0,2mol\Rightarrow m_{Cu}=0,2.64=12,8g\)\(n_{CuO\left(dư\right)}=0,3-\left(0,2.1\right)=0,1mol\Rightarrow m_{CuO}=0,1.64=6,4g\Rightarrow m_{rắn}=12,8+6,4=19,2g\)

a)
\(n_P = \dfrac{62}{31} = 2(mol)\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\\ n_{O_2} = \dfrac{5}{4}n_P = 2,5(mol)\\ V_{O_2} = 2,5.22,4 = 56(lít)\\ V_{không\ khí} = \dfrac{56}{20\%} = 280(lít)\)
b)
\(n_P = \dfrac{31}{31} = 1(mol) ; n_{O_2} = \dfrac{23}{32} = 0,71875(mol)\\ \dfrac{n_P}{4} = 0,25 > \dfrac{n_{O_2}}{5} = 0,14375 \to P\ dư\\ n_{P\ pư} = \dfrac{4}{5}n_{O_2} = 0,575(mol)\\ m_{P\ dư} = 31 - 0,575.31 = 13,175(gam)\\ n_{P_2O_5} = \dfrac{2}{5}n_{O_2} = 0,2875(mol) \Rightarrow m_{P_2O_5} = 0,2875.142=40,825(gam)\)

Ta có: \(n_{O_2}=\dfrac{2,856}{22,4}=0,1275\left(mol\right)\)
\(\dfrac{V_{CO_2}}{V_{H_2O}}=\dfrac{4}{3}\Rightarrow\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{4}{3}\)
Gọi: nCO2 = 4x (mol) ⇒ nH2O = 3x (mol)
Theo ĐLBT KL, có: mA + mO2 = mCO2 + mH2O
⇒ 2,82 + 0,1275.32 = 4x.44 + 3x.18
⇒ x = 0,03
⇒ nCO2 = 0,03.4 = 0,12 (mol) = nC
nH2O = 0,03.3 = 0,09 (mol) ⇒ nH = 0,09.2 = 0,18 (mol)
Ta có: mC + mH = 0,12.12 + 0,18.1 = 1,62 (g) < 2,82 (g)
→ A chứa C, H và O.
⇒ mO = 2,82 - 1,62 = 1,2 (g) \(\Rightarrow n_O=\dfrac{1,2}{16}=0,075\left(mol\right)\)
Gọi CTPT của A là CxHyOz
⇒ x:y:z = 0,12:0,18:0,075 = 8:12:5
→ CTPT của A có dạng là (C8H12O5)n (n nguyên dương)
Mà: \(M_A< 29.7=203\left(g/mol\right)\)
\(\Rightarrow\left(12.8+12.1+16.5\right)n< 203\)
⇒ n < 1,08 ⇒ n = 1
Vậy: CTPT của A là C8H12O5.

a. \(n_P=\frac{6,2}{31}=0,2mol\)
\(V_{O_2}=V_{kk}.\frac{1}{5}=\frac{18,48}{5}=3,696l\)
\(n_{O_2}=\frac{3,696}{22,4}=0,165mol\)
PTHH: \(4P+5O_2\xrightarrow{t^o}2P_2O_5\)
Tỷ lệ \(\frac{0,2}{4}>\frac{0,165}{5}\)
Vậy P dư
\(n_{P\left(\text{phản ứng }\right)}=\frac{4}{5}n_{O_2}=0,132mol\)
\(n_{P\left(dư\right)}=0,2-0,132=0,068mol\)
\(\rightarrow m_{P\left(dư\right)}=0,068.31=2,108g\)
b. \(n_{P_2O_5}=\frac{2}{5}n_{O_2}=0,066mol\)
\(\rightarrow m_{P_2O_5}=0,066.142=9,372g\)
c. PTHH: \(2KClO_3\xrightarrow{t^o}2KCl+3O_2\)
\(n_{KClO_3}=\frac{2}{3}n_{O_2}=0,11mol\)
\(\rightarrow m_{KClO_3}=0,11.122,5=13,475g\)

PTHH: \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
a) Ta có: \(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(\Rightarrow n_{P_2O_5}=0,05\left(mol\right)\) \(\Rightarrow m_{P_2O_5}=0,05\cdot142=7,1\left(g\right)\)
b) Ta có: \(n_{O_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,1}{4}< \dfrac{0,25}{5}\) \(\Rightarrow\) Photpho p/ứ hết, Oxi còn dư
\(\Rightarrow n_{O_2\left(dư\right)}=0,25-0,125=0,125\left(mol\right)\)
\(\Rightarrow m_{O_2\left(dư\right)}=0,125\cdot32=4\left(g\right)\)
\(a) n_P = \dfrac{3,1}{31} = 0,1(mol)\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\\ n_{P_2O_5} = \dfrac{1}{2}n_P = 0,05(mol)\\ m_{P_2O_5} = 0,05.142 = 7,1(gam)\\ b) n_{O_2} = \dfrac{5,6}{22,4} = 0,25(mol)\\ \dfrac{n_P}{4} = 0,025<\dfrac{n_{O_2}}{5} = 0,05 \to O_2\ dư\\ n_{O_2\ pư} = \dfrac{5}{4}n_P = 0,125(mol) \Rightarrow m_{O_2\ dư} = (0,25 - 0,125).32 = 4(gam)\)
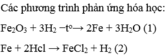
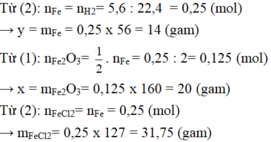
a, Ta có: MA = 0,5.32 = 16 (g/mol)
Gọi CTHH của A là CxHy.
\(\Rightarrow\left\{{}\begin{matrix}x=\dfrac{16.75\%}{12}=1\\y=\dfrac{16.25\%}{1}=4\end{matrix}\right.\)
→ CTHH cần tìm là CH4.
b, \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
Xét tỉ lệ: \(\dfrac{0,25}{1}< \dfrac{0,75}{2}\) ta được O2 dư.
Theo PT: \(V_{O_2\left(pư\right)}=2V_{CH_4}=0,5\left(l\right)\Rightarrow V_{O_2\left(dư\right)}=0,75-0,5=0,25\left(l\right)\)
a khí là ch4
B dư 0,25 lít O2