Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

phần 1:
Fe[0]--->Fe[+2] + 2e
x------------------------2xmol
R[0]----->R[+n] + ne
y---------------------->yn mol
2H[+] + 2e---->H2[0] (nH2=0.095 mol)
----------0.19<----0.095mol
====> theo đl bảo toàn e: 2x + yn= 0.19 mol (1)
Phần 2:
Fe[0]---->Fe[+3] + 3e
x------------------------->3x mol
R[0]----->R[+n] + ne
y---------------------->yn mol
N[+5] + 3e---->N[+2] ( nNO= nN[+2] =0.08 mol)
-----------0.24<----0.08mol
====>theo đl bảo toàn e: 3x + yn=0.024 (2)
Lấy (2) trừ (1) ta được: x=0.05mol
**** Cả hai phần R phản ứng đều ở mức oxh [+n] nên em không cần quan tâm đến nó. Nếu đây là bài toán trắc nghiệm em có thể tính nhanh số mol Fe mỗi phần bằng cách ( khỏi phải viết mấy cái quá trình như trên dài lắm em nhá) :
n Fe = ( 3nNO) - (2nH2) =0.05 mol
Khối lượng mỗi phần = 7.22/2=3.61 g
=>m(R)= 3.61 - (0,05*56)=0.81 g
=>%mR= 0.81/3.61=22,4%
thế các số liệu vào ( phần 1)
Fe[0] -----.Fe[+2] + 2e
0.05------------------------0.1mol
R[0] -----R[+n] + ne
0.81/R--------------0.81n/R
2H[+] + 2e---->H2[0]
----------0.19<----0.095mol
Theo đl bảo toàn e: 0.1 + 0.81n/R = 0.19
=>R=9n
n=1 ==>R= 9 (l)
n=2 ==>R= 18(l)
n=3 ==>R=27( nhận)
.....
Vậy R là Al

Câu 1

Áp dụng định luật bảo toàn nguyên
tố H ta có:
nHCl = 2nH2 = 2.0,045 = 0,09 mol
Áp dụng định luật bảo toàn khối lượng
ta có: mA + mHCl = m muối + mH2
=> m = m muối + mH2 – mA = 4,575 + 0,045.2 – 0,09.36,5 = 1,38 (gam)
Câu 2

Do cho kim loại phản ứng với H2SO4 đặc và HNO3 đặc nên khí sinh ra là SO2 và NO2.
Áp dụng phương pháp đường chéo ta có:
SO2: 64 4,5
50,5
NO2: 46 13,5
→nSO2=nNO2=4,513,5=13

Đặt số mol của Fe và M lần lượt là x và y (mol)
- Khi cho hỗn hợp tác dụng với HCl:
Fe + 2HCl → FeCl2 + H2
x x (mol)
M + nHCl → MCln + 0,5nH2
y 0,5ny (mol)
nH2 = 0,045 => x + 0,5ny = 0,045 (1)
- Khi cho hỗn hợp tác dụng với HNO3 đặc và H2SO4 đặc:
Ta có các bán phản ứng oxi hóa – khử:
Fe → Fe3+ + 3e
x 3x
M → Mn+ + ne
y ny
S+6 + 2e → S+4 (SO2)
0,021 0,042
N+5 + 1e → N+4 (NO2)
0,063 0,063
Áp dụng định luật bảo toàn electron ta có: 3x + ny = 0,042 + 0,063 hay 3x + ny = 0,105 (2)
Từ (1) và (2) ta có hệ phương trình sau:

Mặt khác: mA = mFe + mM => 1,38 = 0,015.56 + My => My = 0,54(4)
Từ (3) và (4) suy ra M = 9n
Ta có bảng sau:
| n |
1 |
2 |
3 |
| M |
9 (loại) |
18 (loại) |
27 (nhận) |
Vậy kim loại M là nhôm, kí hiệu là Al.

a a
2M + 2nHCl -> 2MCln + nH2
b 0,5bn
P2: Fe + 4HNO3 -> Fe(NO3)3 + NO + 2H2O
a a
3M + 4nHNO3 -> 3M(NO3)n + nNO + 2nH2O
b bn/3
nH2(P1)=2,128/22,4=0,095 mol
nNO(P2)=1,792/22,4=0,08 mol
Gọi a,b là số mol Fe và M trong mỗi phần
m mỗi phần=7,22/2=3,61g
=> 56a + bM=3,61 (1)
a+0,5bn=0,095 (2)
a+bn/3=0,08 (3)
Lấy (2) - (3) ta có: 0,5bn - bn/3=0,015
=> bn=0,09 =>b=0,09/n
=>a=0,08-0,09/3=0,05 mol
=> bM=3,61 - 56.0,05=0,81 => (0,09/n) .M=0,81 => M=9n
Chạy nghiệm ta đc n=3 => M=27 (Al)
Kim loại M là Al
%mFe=0,05.2.56/7,22 .100%=77,56%
%mAl=100%-77,56%=22,44%

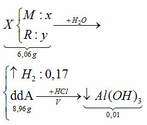
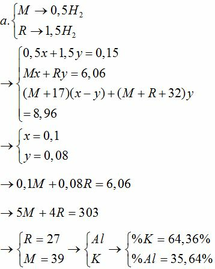
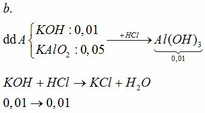
TH1: kết tủa Al(OH)3 chưa bị hòa tan
KAlO2 + HCl +H2O → KCl + Al(OH)3↓
0,01 ←0,01
→ nHCl = 0,02
→ V = 0,02 (lít) = 20 (ml)
TH2: kết tủa Al(OH)3 bị hòa tan một phần
KAlO2 + HCl +H2O → KCl + Al(OH)3↓
0,05 → 0,05 0,05
Al(OH)3 + 3HCl → AlCl3 + 3H2O
0,04` → 0,12
→ nHCl = 0,18 → V = 0,18 (l) = 180 (ml)
Vậy có 2 giá trị của V thỏa mãn là: 20 ml và 180 ml

Gọi số mol trong mỗi phần: Fe = x mol; M = y mol.
Phần 1:
Fe + 2HCl FeCl2 + H2
(mol): x x
2M + 2nHCl 2MCln + nH2
(mol): y 0,5ny
Số mol H2 = 0,07 nên x + 0,5ny = 0,07.
Phần 2:
2Fe + 6H2SO4 (đặc) Fe2(SO4)3 + 3SO2 + 6H2O
(mol): x 1,5x
2M + 2nH2SO4 (đặc) M2(SO4)n + nSO2 + 2nH2O
(mol): y 0,5nx
Số mol SO2 = 0,09 nên 1,5x + 0,5ny = 0,09. Vậy x = 0,04 và ny = 0,06.
Mặt khác: 56x + My = 2,78 nên My = 0,54. Vậy hay M = 9n.
Ta lập bảng sau:
| n | 1 | 2 | 3 |
| M | 9 ( loại ) | 18 ( loại ) | 27 ( nhận ) |
Vậy M là \(Al\) ( nhôm ) .
Đặt a là số mol Fe, b là số mol của M,trong mỗi phần,n là hóa trị của M
PTHH: Fe +2HCl ---> FeCl2 + H2
a a
2M + 2n HCl ---> 2 MCln + n H2
b bn/2
n H2= 0.07
---> a + bn/2 = 0.07 (1)
m hh A = 56a + Mb = 2.78 (2)
PTHH: Fe + 4HNO3 ----> Fe(NO3)3 + NO + 2H2O
a a
3M +4n HNO3 ---->3M(NO3)n +nNO + 2n H2O
b bn/3
n NO = a + bn/3 = 0.06 (3)
Từ (1) và (3) giải hệ ta dc : a= 0.04
bn = 0.06---> b= 0.06/n (4)
Thế à= 0.04vào pt (2) giải ra ta đc : 2.24 + Mb = 2.78
-----> b = 0.54/ M (5)
Từ (4) và (5) ----> M= 9n
Biện luận n
n=1 ----> M = 9 (loại)
n=2 ----> M= 18 (loại)
n=3-----> M=27 (nhận)
Do đó : M là Al

Gọi: M là NTK của R
a là số oxi hóa của R trong muối --> CTPT muối của R là R(2/a)CO3.
a) Từ nCO2 = n hỗn hợp = 0,5 nHCl = 3,36/22,4 = 0,15
--> nHCl = 0,15 x 2 = 0,3 mol nặng 0,3 x 36,5 = 10,95 gam.
--> dung dịch axit HCl 7,3% nặng 10,95/0,073 = 150 gam.
Mà
m dung dịch sau phản ứng = m dung dịch axit + m C - m CO2 bay ra
= 150 + 14,2 - (0,15 x 44) = 157,6 gam
--> m MgCl2 = 0,06028 x 157,6 = 9,5 gam
--> n MgCl2 = 9,5/95 = 0,1 mol = n MgCO3
--> m MgCO3 = 0,1 x 84 = 8,4 gam chiếm 8,4/14,2 = 59,154929%
--> m R(2/a)CO3 = 14,2 - 8,4 = 5,8 gam chiếm 5,8/14,2 = 40,845071%
--> n R(2/a)CO3 = 0,15 - 0,1 = 0,05 mol.
--> PTK của R(2/a)CO3 = 5,8/0,05 = 116.
--> 2M/a = 116 - 60 = 56 hay M = 23a.
Chọn a = 2 với M = 56 --> R là Fe.
b) Khối lượng chất rắn sau khi nung đến khối lượng không đổi là khối lượng của 0,1 mol MgO và 0,05 mol FeO(1,5). (FeO(1,5) là cách viết khác của Fe2O3. Cũng là oxit sắt 3 nhưng PTK chỉ bằng 80).
m chất rắn sau khi nung = (0,1 x 40) + (0,05 x 80) = 8 gam.

\(n_{H_2}=\dfrac{8,96}{22,4}=0,4(mol)\\ n_{Al}=x(mol);n_{Mg}=y(mol)\\ \Rightarrow 27x+24y=7,8(1)\\ a,2Al+6HCl\to 2AlCl_3+3H_2\\ Mg+2HCl\to MgCl_2+H_2\\ \Rightarrow 1,5x+y=0,4(2)\\ (1)(2)\Rightarrow x=0,2(mol);y=0,1(mol)\\ \Rightarrow \%_{Al}=\dfrac{0,2.27}{7,8}.100\%=69,23\%\\ \Rightarrow \%_{Mg}=100\%-69,23\%=30,77\%\)
\(b,\Sigma n_{HCl}=3x+2y=0,8(mol)\\ \Rightarrow C\%_{HCl}=\dfrac{0,8.36,5}{192,2}.100\%=15,19\%\\ c,n_{AlCl_3}=0,2(mol);n_{MgCl_2}=0,1(mol)\\ \Rightarrow C\%_{AlCl_3}=\dfrac{0,2.133,5}{0,2.27+192,2-0,3.2}.100\%=13,55\%\\ C\%_{MgCl_2}=\dfrac{0,1.95}{0,1.24+192,2-0,1.2}.100\%=4,89\%\)


phần 1:
Fe[0]--->Fe[+2] + 2e
x------------------------2xmol
R[0]----->R[+n] + ne
y---------------------->yn mol
2H[+] + 2e---->H2[0] (nH2=0.095 mol)
----------0.19<----0.095mol
====> theo đl bảo toàn e: 2x + yn= 0.19 mol (1)
Phần 2:
Fe[0]---->Fe[+3] + 3e
x------------------------->3x mol
R[0]----->R[+n] + ne
y---------------------->yn mol
N[+5] + 3e---->N[+2] ( nNO= nN[+2] =0.08 mol)
-----------0.24<----0.08mol
====>theo đl bảo toàn e: 3x + yn=0.024 (2)
Lấy (2) trừ (1) ta được: x=0.05mol
**** Cả hai phần R phản ứng đều ở mức oxh [+n] nên em không cần quan tâm đến nó. Nếu đây là bài toán trắc nghiệm em có thể tính nhanh số mol Fe mỗi phần bằng cách ( khỏi phải viết mấy cái quá trình như trên dài lắm em nhá) :
n Fe = ( 3nNO) - (2nH2) =0.05 mol
Khối lượng mỗi phần = 7.22/2=3.61 g
=>m(R)= 3.61 - (0,05*56)=0.81 g
=>%mR= 0.81/3.61=22,4%
thế các số liệu vào ( phần 1)
Fe[0] -----.Fe[+2] + 2e
0.05------------------------0.1mol
R[0] -----R[+n] + ne
0.81/R--------------0.81n/R
2H[+] + 2e---->H2[0]
----------0.19<----0.095mol
Theo đl bảo toàn e: 0.1 + 0.81n/R = 0.19
=>R=9n
n=1 ==>R= 9 (l)
n=2 ==>R= 18(l)
n=3 ==>R=27( nhận)
.....
Vậy R là Al
cách 2 bài 1
KL M hóa trị n
Gọi x và y là số mol của Fe và KL M sau khi chia thành 2 phần và n là hóa trị của M
2x + ny = (2,128/22,4) *2
3x + ny = (1,792/22,4) *3
=>x= 0,05 ; ny = 0,09
m X =7,22/2=3,61 = 56x + My = 3,61 =>56*0,05 + My = 3,61 => My =0,81 ta có ny =0,09
lấy My/ny=0,81/0,09 <=>M/n =9
Ta có: M= 9n =>chọn M=27,n=3 .Vậy kim loại M là Al