Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Sự chuyển thể của các chất SVIP
I. SƠ LƯỢC CẤU TRÚC CỦA CHẤT RẮN, CHẤT LỎNG, CHẤT KHÍ
1. Mô hình động học phân tử
Mô hình động học phân tử về cấu tạo chất gồm 3 nội dung chính:
- Chất được cấu tạo từ các hạt riêng biệt gọi là phân tử.
- Phân tử luôn chuyển động không ngừng; nhiệt độ càng cao, phân tử chuyển động càng nhanh.
- Giữa các phân tử tồn tại lực hút và lực đẩy, gọi chung là lực liên kết phân tử.
Mô hình động học phân tử giúp giải thích cấu trúc của chất rắn, lỏng, khí và quá trình chuyển thể giữa các trạng thái này (như nóng chảy, bay hơi, ngưng tụ,…).
Câu hỏi:
@202702067802@
2. Sơ lược cấu trúc của chất rắn
Trong chất rắn, các phân tử ở rất gần nhau.
 - Copy.jpg)
Mô hình cấu trúc chất rắn (kết tinh)
Lực tương tác
- Lực tương tác mạnh giữa các phân tử giữ chúng dao động quanh vị trí cân bằng, không di chuyển tự do. Vì vậy, chất rắn có hình dạng và thể tích xác định.
Phân loại
- Chất rắn kết tinh: có cấu trúc tinh thể rõ ràng, ví dụ: thạch anh, muối ăn, kim cương, kim loại, nước đá,...
- Chất rắn vô định hình: không có cấu trúc tinh thể, ví dụ: thủy tinh, nhựa, sô-cô-la,...
Câu hỏi:
@202702070200@
3. Sơ lược cấu trúc của chất lỏng
Trong chất lỏng, các phân tử ở xa nhau hơn so với các phân tử trong chất rắn.
 - Copy - Copy.jpg)
Mô hình cấu trúc chất lỏng
Lực tương tác
- Lực tương tác giữa các phân tử lớn hơn trong chất khí, nên các phân tử không bị tách rời, giúp chất lỏng có thể tích xác định.
- Tuy nhiên, lực liên kết chưa đủ mạnh như trong chất rắn, nên các phân tử dao động quanh vị trí không cố định, khiến chất lỏng không có hình dạng riêng mà phụ thuộc vào bình chứa. Chất lỏng cũng rất khó bị nén.
4. Sơ lược cấu trúc của chất khí
Trong chất khí, các phân tử ở xa nhau hơn so với các phân tử trong chất lỏng.

Mô hình cấu trúc chất khí
Lực tương tác
- Lực tương tác giữa chúng rất yếu, nên chuyển động hoàn toàn hỗn loạn. Vì vậy, chất khí không có hình dạng và thể tích cố định, mà phụ thuộc vào bình chứa và có thể bị nén dễ dàng.
II. SỰ CHUYỂN THỂ
1. Sự chuyển thể của chất
Các chất có thể chuyển từ thể này sang thể khác.
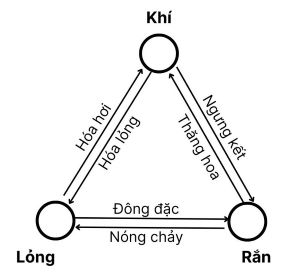
Sơ đồ các hình thức chuyển thể
2. Giải thích sự nóng chảy
Ở trạng thái rắn, phân tử trong chất kết tinh xếp chặt và có trật tự, tạo thành lưới tinh thể cứng và ổn định.
Khi nhiệt độ tăng, các phân tử hấp thụ năng lượng và dao động mạnh hơn.
Đến nhiệt độ nóng chảy, năng lượng đủ lớn giúp phân tử vượt qua liên kết, chuyển sang chuyển động tự do và chất rắn trở thành chất lỏng.

Câu hỏi:
@202702094467@@202702095258@
3. Giải thích sự hóa hơi
Sự hoá hơi có thể xảy ra dưới hai hình thức là bay hơi và sôi.
Sự bay hơi là quá trình hóa hơi xảy ra trên mặt thoáng chất lỏng. Một số phân tử có động năng đủ lớn sẽ thoát khỏi mặt thoáng, trở thành phân tử hơi.
Sự sôi là quá trình hóa hơi xảy ra cả trong lòng và trên mặt chất lỏng. Khi nước đạt khoảng 100 °C, các bọt khí và hơi nước hình thành, nổi lên và vỡ ở mặt thoáng, giải phóng hơi nước ra môi trường.

Chất | Nhiệt độ nóng chảy (oC) | Nhiệt độ sôi (oC) |
Tungsten (wolfram) | 3422 | 5555 |
Đồng | 1300 | 2580 |
Chì | 327 | 1 749 |
Thủy ngân | -39 | 357 |
Rượu | -117 | 80 |
Bạn có thể đăng câu hỏi về bài học này ở đây
