Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Glucose và fructose SVIP
1. Khái niệm và phân loại carbohydrate
Carbohydrate là những hợp chất hữu cơ tạp chức, thường có công thức chung là Cn(H2O)m.
Carbohydrate được chia thành ba loại chính:
| Nhóm | Đặc điểm | Ví dụ |
| Monosaccharide | Không bị thủy phân thành các phân tử nhỏ hơn | Glucose, fructose |
| Disaccharide | Thủy phân hoàn toàn mỗi phân tử tạo thành hai phân tử monosaccharide | Saccharose, maltose |
| Polysaccharide | Thủy phân hoàn toàn mỗi phân tử tạo thành nhiều phân tử monosaccharide | Tinh bột, cellulose |
2. Glucose - fructose
Trạng thái tự nhiên
Glucose là chất rắn, dễ tan trong nước, có vị ngọt. Glucose hình thành trong thực vật nhờ quá trình quang hợp và có trong các bộ phận như hoa, lá,... và nhất là quả chín.

Glucose có trong cơ thể con người và động vật. Glucose đóng vai trò cung cấp năng lượng cho tế bào.
Fructose là chất rắn, dễ tan trong nước, có vị ngọt. Fructose có trong nhiều loại trái cây (táo, nho, lựu, nho, lê,...), trong một số loại rau củ (cà rốt, củ cải đường,...) và có nhiều nhất trong mật ong.

Công thức cấu tạo dạng mạch hở và mạch vòng của glucose và fructose
Glucose (C6H12O6) ở dạng mạch hở có năm nhóm hydroxy và một nhóm aldehyde.
Glucose có một dạng mạch hở và hai dạng mạch vòng chuyển hóa qua lại lẫn nhau.
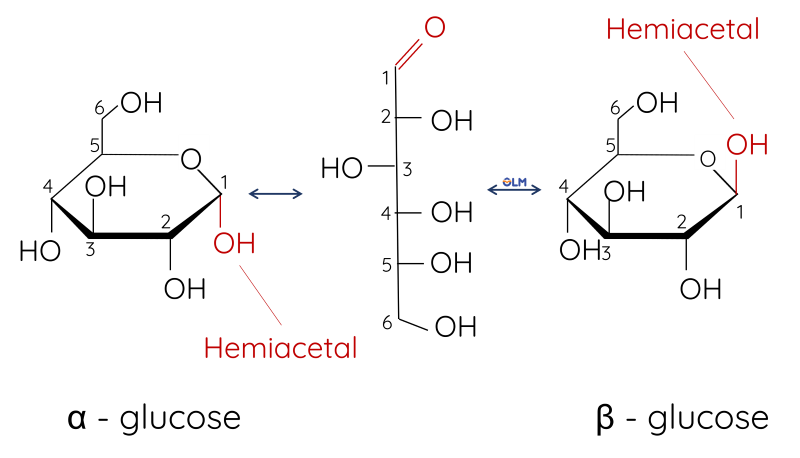
Fructose (C6H12O6) ở dạng mạch hở chứa năm nhóm hydroxy và một nhóm ketone.
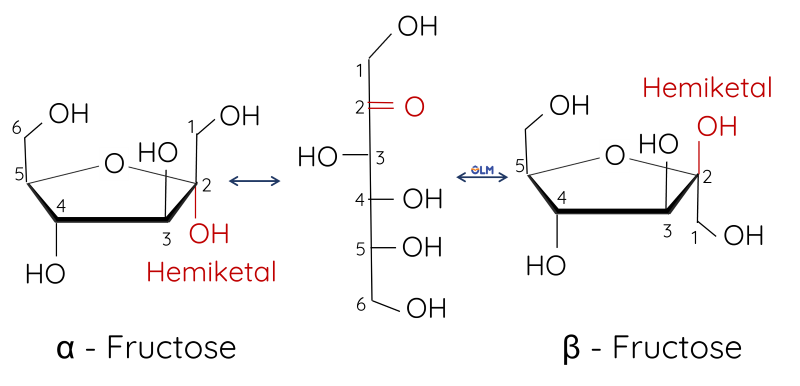
Tính chất hóa học cơ bản của glucose và fructose
1. Tính chất polyalcohol
Thí nghiệm 1: Phản ứng của glucose với Cu(OH)2
Bước 1: Thêm 2 mL dung dịch NaOH 10% 0,5 mL vào dung dịch CuSO4 5%.
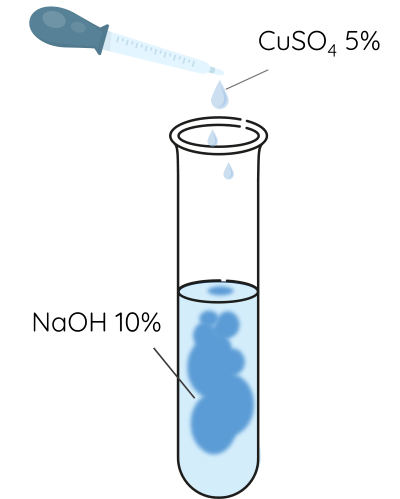
Bước 2: Thêm tiếp vào ống nghiệm 3 mL dung dịch glucose 2% vào ống nghiệm và lắc đều.
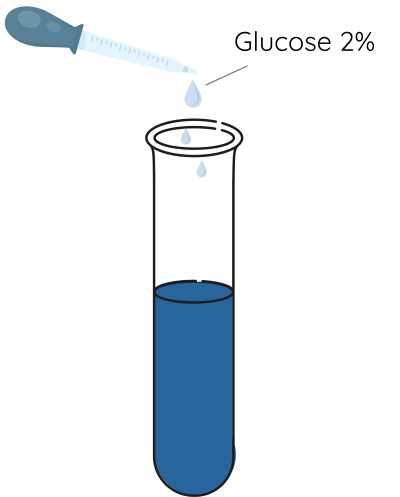
Phân tử glucose và fructose có nhiều nhóm hydroxy liền kề nên có thể hòa tan được Cu(OH)2 trong môi trường kiềm, tạo thành dung dịch màu xanh lam.
2C6H12O6 + Cu(OH)2 → (C6H11O6)2Cu + 2H2O
2. Tính chất aldehyde
a) Phản ứng với thuốc thử Tollens
Thí nghiệm 2: Phản ứng với thuốc thử Tollens
Bước 1: Thêm từ từ dung dịch NH3 5% vào 2 mL dung dịch AgNO3 1%. Lắc đến khi kết tủa tan hết.
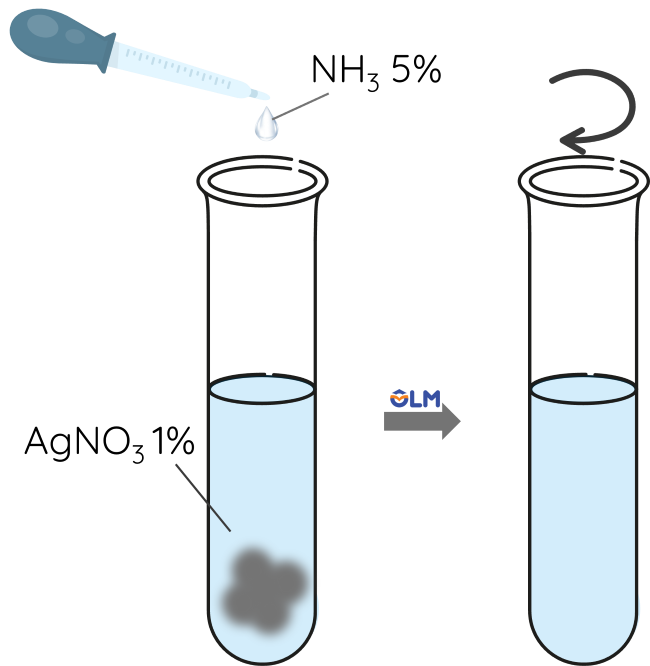
Bước 2: Thêm 2 mL dung dịch glucose 2%, lắc đều.
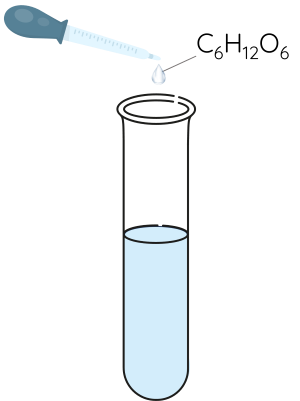
Bước 3: Ngâm ống nghiệm vào cốc thủy tinh chứa nước nóng và chờ trong vài phút.
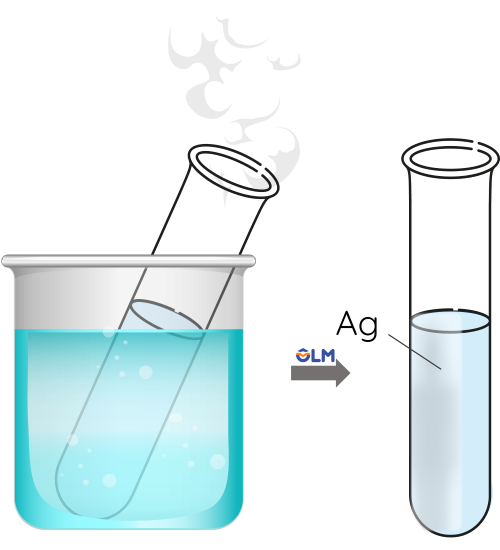
Glucose phản ứng với thuốc thử Tollens trong điều kiện đun nóng nhẹ tạo thành kim loại bạc.
CH2OH[CHOH]4CH=O + 2[Ag(NH3)2]OH \(\underrightarrow{t^o}\) CH2OH[CHOH]4COONH4 + 2Ag + 3NH3 + H2O
Tuy không có nhóm -CHO nhưng trong môi trường kiềm, fructose chuyển hóa thành glucose, nên fructose cũng có phản ứng với thuốc thử Tollens tương tự glucose.
b) Phản ứng với Cu(OH)2 trong môi trường base. đun nóng
Thí nghiệm 3: Phản ứng với Cu(OH)2, đun nóng
Bước 1: Thêm 2 mL dung dịch NaOH 10% 0,5 mL vào dung dịch CuSO4 5%.

Bước 2: Thêm tiếp vào ống nghiệm 3 mL dung dịch glucose 2% vào ống nghiệm và lắc đều.

Bước 3: Đun nóng ống nghiệm bằng ngọn lửa đèn cồn trong vài phút.
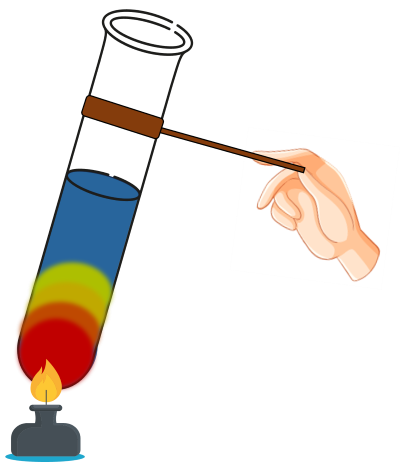
Dung dịch glucose và fructose đều có phản ứng với Cu(OH)2 trong môi trường base đun nóng tạo kết tủa đỏ gạch.
CH2OH[CHOH]4CH=O + 2Cu(OH)2 + NaOH \(\underrightarrow{t^o}\) CH2OH[CHOH]4COONa + Cu2O + 3H2O
c) Phản ứng với nước bromine
Thí nghiệm 4: Phản ứng của glucose với bromine
Cho khoảng 1 mL nước bromine loãng vào ống nghiệm. Sau đó, thêm từ từ 2 mL dung dịch glucose 2%, lắc đều.

Nhóm aldehyde của glucose có thể bị oxi hóa bởi nước bromine thành nhóm -COOH.
CH2OH[CHOH]4CH=O + Br2 + H2O → CH2OH[CHOH]4COOH + 2HBr
d) Phản ứng lên men
Dưới tác dụng của các enzyme từ các vi sinh vật khác nhau, glucose được lên men tạo thành các hợp chất có nhiều ứng dụng trong đời sống như ethanol, lactic acid,...
Ví dụ:
C6H12O6 \(\underrightarrow{enzyme}\) 2C2H5OH + 2CO2
C6H12O6 \(\underrightarrow{enzyme}\) 2CH3CH(OH)COOH
3. Tính chất của nhóm - OH hemiacetal
Ở dạng cấu tạo mạch vòng, nhóm - OH hemiacetal của glucose tác dụng với methanol khi có mặt của HCl khan, tạo thành methyl glucoside.

Ứng dụng của glucose và fructose
Glucose còn có nhiều ứng dụng trong cuộc sống như sản xuất thực phẩm, đồ uống; sản xuất ruột phích, tráng gương; nguyên liệu sản xuất ethanol; dung dịch truyền tĩnh mạch,...
- Fructose cũng được sử dụng phổ biến trong lĩnh vực sản xuất siro, kẹo, mứt, nước trái cây đóng hộp,...
1. Carbohydrate là những hợp chất hữu cơ tạp chức, thường có công thức chung là Cn(H2O)m.
2. Carbohydrate được phân thành 3 loại: monosaccharide, disaccharide và polysaccharide.
3. Glucose và fructose tồn tại đồng thời cấu tạo dạng mạch hở và mạch vòng. Fructose chuyển hóa thuận nghịch thành glucose trong môi trường kiềm.
4. Glucose và fructose là những chất rắn có vị ngọt, dễ tan trong nước.
5. Glucose có nhiều trong trái cây chín, fructose có nhiều trong mật ong.
6. Glucose và fructose tồn tại ở dạng mạch vòng và mạch hở.
7. Glucose và fructose đều có:
- Phản ứng với Cu(OH)2 trong môi trường base ở nhiệt độ thường và khi đun nóng.
- Phản ứng với thuốc thử Tollens.
Glucose còn làm mất màu nước bromine, có phản ứng ở nhóm -OH hemiacetal và phản ứng lên men.
8. Glucose và fructose là những hợp chất được sử dụng nhiều trong lĩnh vực y tế, công nghiệp thực phẩm.
Bạn có thể đăng câu hỏi về bài học này ở đây
