Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Điện phân (phần 1) SVIP

Lưu ý: Ở điểm dừng, nếu không thấy nút nộp bài, bạn hãy kéo thanh trượt xuống dưới.
Bạn phải xem đến hết Video thì mới được lưu thời gian xem.
Để đảm bảo tốc độ truyền video, OLM lưu trữ video trên youtube. Do vậy phụ huynh tạm thời không chặn youtube để con có thể xem được bài giảng.
Nội dung này là Video có điểm dừng: Xem video kết hợp với trả lời câu hỏi.
Nếu câu hỏi nào bị trả lời sai, bạn sẽ phải trả lời lại dạng bài đó đến khi nào đúng mới qua được điểm dừng.
Bạn không được phép tua video qua một điểm dừng chưa hoàn thành.
Dữ liệu luyện tập chỉ được lưu khi bạn qua mỗi điểm dừng.
Thứ tự điện phân:
- Tại anode: chất khử mạnh hơn bị oxi hóa trước.
- Tại cathode: chất oxi hóa yếu mạnh hơn bị khử trước.
Thực hiện điện phân CuCl2 với điện cực than chì theo sơ đồ sau:
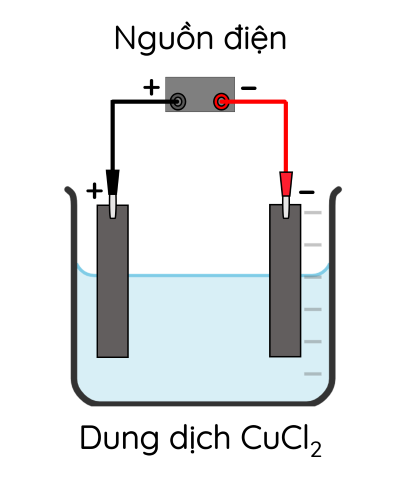
Phương trình phân li CuCl2 trong dung dịch là
Quá trình nào dưới đây xảy ra ở cathode?
Quá trình nào dưới đây xảy ra ở anode?
Phương trình hóa học của quá trình điện phân là
Hiện tượng quan sát được trong quá trình điện phân là gì?
Cho giá trị thế điện cực chuẩn của một số cặp oxi hóa - khử như sau:
Cặp oxi hóa - khử | Thế điện cực chuẩn (V) |
Na+/Na | -2,713 |
Fe2+/Fe | -0,440 |
H2O/H2, OH- | -0,414 |
Cu2+/Cu | +0,340 |
Trong dung dịch chứa đồng thời các cation Na+, Fe2+, Cu2+, chất/ion nào bị điện phân đầu tiên ở cathode?
Thực hiện điện phân dung dịch NaCl bão hòa với điện cực trơ (graphite).
Sản phẩm thu được tại anode là
Sản phẩm thu được tại cathode là
Ion halide nào dưới đây không bị oxi hóa ở anode?
Điện phân dung dịch AgNO3, quá trình đầu tiên xảy ra ở anode là
Tiến hành điện phân có màng ngăn lần lượt các dung dịch sau: KCl, CuSO4, Na2SO4, AgNO3, BaCl2. Có bao nhiêu dung dịch sau khi điện phân có pH > 7?
Trả lời: .
Thực hiện điện phân dung dịch Cu(NO3)2 với điện cực graphite.
(Nhấp vào ô màu vàng để chọn đúng / sai)| a) Ion Cu2+ di chuyển về phía anode. |
|
| b) Khối lượng cathode không thay đổi. |
|
| c) Nồng độ Cu(NO3)2 trong dung dịch giảm dần. |
|
| d) Dung dịch sau điện phân có pH < 7. |
|
Văn bản dưới đây là được tạo ra tự động từ nhận diện giọng nói trong video nên có thể có lỗi
- Cô thân ái chào mừng các em đã quay trở
- lại với khóa học khóa học lớp 12 tại
- trang web olm.vn.
- Bài học hôm nay chúng ta sẽ cùng tìm
- hiểu về điện phần làm một số bài tập
- minh
- họa. Bài học này gồm hai nội dung chính
- là hiện tượng điện phân và ứng dụng của
- quá trình điện
- phân. Đầu tiên chúng ta cùng tìm hiểu về
- hiện tượng điện phân. Các em đã được học
- phản ứng trong pin điện là phản ứng tự
- xảy ra. Năng lượng hóa học của phản ứng
- oxy hóa khử chuyển thành năng lượng
- điện.
- Vậy còn đối với những phản ứng không tự
- xảy ra thì như thế
- nào? Theo lý thuyết có thể sử dụng năng
- lượng điện để giúp phản ứng xảy ra. Quá
- trình này gọi là hiện tượng điện
- phân. Ta có khái niệm như
- sau. Điện phân là quá trình oxy hóa khử
- xảy ra tại các điện cực khi có dòng điện
- một chiều với hiệu điện thế đủ lớn đi
- qua chất điện ly nóng chảy hoặc dung
- dịch điện
- ly. Tổng quát như sau.
- Khi nóng chảy hoặc hòa tan tạo thành
- dung dịch thì xảy ra phản ứng phân ly
- của các chất điện ly mạnh tạo thành
- cation và
- enion. Lúc này các enion di chuyển về
- phía cực dương enố tham gia vào quá
- trình oxy hóa. Ngược lại các cion mang
- điện tích dương do lực hút tĩnh điện nên
- di chuyển về cực âm
- catốt. Tại đây xảy ra quá trình khử.
- Để hiểu rõ hơn, chúng ta cùng xét ví dụ
- cụ thể là điện phân sodium chloride nóng
- chảy. Quá trình này được thực hiện qua
- hai bước như
- sau. Bước một, dùng sâu chloride rắn đến
- nóng chảy. Lúc này sâu điểm cloride phân
- ly thành Cion Na+ và Cl-.
- Sau đó nhúng hai điện cực than trì vào
- sâu chloride nóng chảy. Nối hai điện cực
- với hai cực của dòng điện một chiều như
- sơ đồ dưới
- đây. Do tác dụng của lực hút tĩnh điện,
- non Cl- di chuyển về cực dương enố tham
- gia vào quá trình oxy hóa tạo thành khí
- clorin thoát ra
- ngoài. Đồng thời C Na+ di chuyển về cực
- âm catố tham gia quá trình khử tạo thành
- kim loại sodium bám lên trên điện cực.
- Như vậy phản ứng điện phân nóng chạy
- sodium chloride tạo ra sản phẩm là
- sodium và khí
- chlorin. Tương tự các em hãy phân tích
- quá trình điện phân dung dịch copper to
- chloride với điện cực trơ thông qua việc
- trả lời các câu hỏi sau.
- Thứ nhất, viết phương trình phân lý
- copper to chloride trong dung dịch. Sau
- đó viết quá trình xảy ra ở mỗi điện cực
- và phương trình hóa học của phản ứng xảy
- ra trong quá trình điện phân. Từ đó, nếu
- hiện tượng quan sát được trong quá trình
- điện
- [âm nhạc]
- phân. Xin chúc mừng các em đã có câu trả
- lời chính xác.
- Cô biểu diễn quá trình điện phân thông
- qua sơ đồ dưới đây. Trong dung dịch
- copper to chloride phân ly thành ion
- CO2+ và Cl- trong đó Cl- di chuyển về
- enố tham gia quá trình oxy hóa giải
- phóng khí chlorin ra khỏi dung dịch. Còn
- CO2+ di chuyển về catốt. Tại đây xảy ra
- quá trình khử Cu+ thành Cu bám lên trên
- điện cực.
- Như vậy quá trình điện phân tạo ra kim
- loại đồng và khí
- chlorin. Do đó hiện tượng quan sát được
- là có chất rắn màu đỏ đồng bám lên trên
- điện cực âm cà tốt và tại enố thì có khí
- thoát
- ra. Có một lưu ý quan trọng trong quá
- trình điện phân dung dịch là nước trong
- dung dịch cũng có thể bị điện phân ở cả
- hai điện cực. Ở enố nước bị oxy hóa
- thành khí oxygen và ion H+. Còn tại
- catốp, nước bị khử thành khí hydrogen và
- ion
- OH- hai quá trình điện phần của nước
- tương ứng với hai cặp oxy hóa khử liên
- quan đến nước mà chúng ta đã đề cập khi
- học bài thế điện cực chuẩn. Để hiểu rõ
- hơn, chúng ta cùng phân tích ví dụ điện
- phân dung dịch Copper to Surpate với
- điện cực trơ.
- Trong dung dịch, Copper to sulfate bị
- phân ly thành ion CO2+ và ion
- SO42- lúc này, ion SO42- di chuyển về
- phía
- en, ion CO2+ di chuyển về phía
- catố. Tại Enos có ion SO42- và nước,
- trong đó ion SO42- không bị điện phân mà
- nước bị điện phân thành khí oxygen và
- ion H+. Ion H+ tạo thành kết hợp với ion
- SO42- không bị điện phân tạo thành
- H2SO4. Còn tại catố có ion CO2+ và nước,
- trong đó CO2+ được ưu tiên điện phân
- trước tạo thành kim loại đồng.
- Như vậy, quá trình điện phân dung dịch
- copper to surfate tạo thành kim loại
- đồng, sulphuric a và giải phóng khí
- oxygen. Vậy làm thế nào để xác định được
- chất nào được ưu tiên điện phân trước,
- chất nào không bị điện
- phân? Trong trường hợp mỗi điện cực có
- nhiều hơn một chất bị khử hoặc bị oxy
- hóa thì cần tuân theo nguyên tắc về thứ
- tự điện phân.
- Cụ thể tại cốt chất có tính oxy hóa mạnh
- hơn bị khử trước. Để xác định chất nào
- có tính oxy hóa mạnh hơn, các em cần dựa
- vào thế điện cực chuẩn của cặp oxy hóa
- khử liên quan đến ion hoặc chất
- đó. Chẳng hạn, tư thế điện cực chuẩn ta
- sắp xếp được chiêu dạm dần tính oxy hóa
- như sau.
- Đây cũng chính là thứ tự điện phần ở
- catố, tức là ion AU3+ bị khử trước, sau
- đó đến Ag, Hg2+, Cu2+, H+, sau đó đến
- nước vân
- vân. Ngược lại, ở Enố, chất có tính khự
- mạnh hơn sẽ bị oxy hóa trước và thông
- thường thì các ion highlight trừ ion
- fluoride bị điện phân, sau đó đến nước.
- Còn các gốc axit khác thì hầu như không
- bị oxy
- hóa. Tuy nhiên, trên thực tế lượng nước
- trong dung dịch tương đối nhiều. Đồng
- thời khi nước bị điện phân ở cả hai điện
- cực thì tạo thành OH- và H+. Hai ion này
- trung hòa nhau lại tạo thành nước nên
- chúng ta thường không xét đến các ion bị
- điện phân sau nước.
- Từ lý thuyết về thứ tự điện phân, các em
- hãy cho biết trong dung dịch chứa đồng
- thời các kat CO2+, Na+, Fe2+ thì chất
- nào bị điện phân đầu tiên ở catố thông
- qua giá trị thế điện cực chuẩn cho ở bạn
- dưới
- đây? Xin chúc mừng các em đã có câu trả
- lời chính
- xác. Chúng ta đã được học ở bài Thế điền
- cực chuẩn. là thế điền cực chuẩn càng
- lớn thì dạng oxy hóa có tính oxy hóa
- càng mạnh. Như vậy thứ tự tăng dần tính
- oxy hóa là Na+, Fe2+, nước và mạnh nhất
- là
- CO2+. Do đó tại cá tốt, ion CO2+ bị điện
- phân đầu tiên. Tiếp theo, các em hãy
- phân tích quá trình điện phân dung dịch
- NaCl bão hòa với điện cực trơ để từ đó
- cho biết các sản phẩm thu được ở mỗi
- điện cực là gì.
- Cũng như khi điện phân nóng chạy NaCl
- trong dung dịch NaCl phân ly thành Na+
- và Cl- các ion này di chuyển về hai điện
- cực. Tại Enod có ion Cl- và nước trong
- đó Cl- có tính khự mạnh hơn nên bị oxy
- hóa trước tạo thành khí
- clorin. Tại catố có ion Na+ và nước. Tuy
- nhiên, nước có tính oxy hóa mạnh hơn nên
- bị khử trước, tạo thành ion OH- và giải
- phóng khí
- hydrogen. Ion OH- kết hợp với ion Na+
- tạo thành
- NaOH. Như vậy, tại catố thu được khí
- hydrogen và sodium hydroxide, còn tại
- Enos thu được khí
- clorin. Lúc này ta có phản ứng điện phân
- dung dịch sodium chloride như sau.
- Trên thực tế, Clu tán vào dung dịch NaOH
- tạo thành NaCl và NaClO là nước da ven
- có tính tẩy màu. Do đó, để thu được các
- sản phẩm là dung dịch NaOH, khí H2 và
- khí
- Clăn ngăn cách Clách tán vào dung dịch
- NaOH. Như vậy, chúng ta vừa tìm hiểu về
- hiện tượng điện phân. Trước khi kết thúc
- bài học hôm nay, cô sẽ hướng dẫn các em
- cách làm một số bài tập liên quan đến
- điện
- phân. Câu hỏi đầu tiên là câu hỏi trắc
- nghiệm nhiều phương án lựa chọn. Các em
- hãy cho biết ion highlight nào dưới đây
- không bị oxy hóa ở
- [âm nhạc]
- enố? Xin chúc mừng các em đã có câu trả
- lời chính xác. Trong các ion highlight
- chỉ duy nhất ion floride không bị oxy
- hóa do ion này có tính khử
- yếu. Câu hỏi thứ hai. Khi thực hiện điện
- phân dung dịch silver nitrate, quá trình
- đầu tiên xảy ra ở en quá trình
- nào? Đáp án của cô là đáp án D. Tương tự
- như điện phân dung dịch copper to
- surface.
- Silver nitrate trong dung dịch phân ly
- thành Ag+ và
- NO3- trong đó Ag+ di chuyển về phía catố
- bị khự thành kim loại bạc còn ion
- nitrate di chuyển về phía enố tuy nhiên
- ion này không bị oxy hóa mà nước bị oxy
- hóa thành khí oxygen và ion H+.
- Câu hỏi tiếp theo thuộc dạng câu hỏi
- trắc nghiệm đúng sai về quá trình thực
- hiện điện phân dung dịch copper to
- nitrate với điện cực
- graphit. Các em hãy cho biết các phát
- biểu dưới đây đúng hay
- [âm nhạc]
- sai? Xin chúc mừng các em đã có câu trả
- lời chính xác. Đáp án của cô như sau.
- Chúng ta cùng phân tích quá trình điện
- phân dung dịch Copper to
- Nitrate. Copper to nitrate phân ly thành
- CO2+ và NO3- trong đó NO3- di chuyển về
- phía Enod, CO2+ di chuyển về phía catố.
- Tại Enod có ion NO3- và nước. Tuy nhiên,
- NO3- không bị oxy hóa mà nước bị oxy hóa
- giải phóng khí oxygen và tạo thành ion
- H+.
- Tại catố có ion CO2+ và nước. Do CO2+ có
- tính oxy hóa mạnh hơn nên bị khửu trước
- tạo thành đồng. Do đó phát biểu a sai
- ion CO2+ di chuyển về phía catốt. Kim
- loại đồng tạo thành do quá trình khử
- CO2+ bám lên trên catố làm cho khối
- lượng catố tăng dần. phát biểu B là
- sai. Đồng thời do ion CO2+ bị khử nên
- nồng độ CO2+ trong dung dịch giảm dần.
- Do đó nồng độ copper to nitrate cũng dạm
- dần. Phát biểu C là
- đúng. Do tại en ion H+ được tạo thành
- nên dung dịch sau phản ứng có tính axit
- pH có giá trị nhỏ hơn 7. Do đó phát biểu
- D đúng. Câu hỏi cuối cùng là câu hỏi
- trắc nghiệm trả lời ngắn.
- Thực hiện phân dung dịch với màng ngăn
- xốp các dung dịch KCl, CuSO4,
- Na2SO4,
- AgnCl2. Sau điện phân thu được bao nhiêu
- dung dịch có pH lớn hơn
- [âm nhạc]
- 7? Đáp án của cô là 2. Phân tích quá
- trình điện phân của các dung dịch, ta
- viết được phương trình hóa học của phản
- ứng điện phân như sau.
- Trong các phản ứng này có hai phản ứng
- tạo ra sản phẩm là kiềm bao gồm KCl và
- BACl2 nên pH của dung dịch sau điện phân
- có giá trị lớn hơn
- 7. Như vậy chúng ta vừa đi tìm hiểu các
- nội dung về hiện tượng điện phân và làm
- một số ví dụ minh họa. Để luyện tập thêm
- các em hãy truy cập vào trang web olm.vn
- và ấn theo dõi kênh học trực tuyến OLM
- để cập nhật các bài dạng sớm nhất nhé.
- Xin chào và hẹn gặp lại các em trong các
- bài học tiếp theo. không
- [âm nhạc]
Bạn có thể đăng câu hỏi về bài học này ở đây
