Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Đề thi thử cuối học kì II lần 3 SVIP
Yêu cầu đăng nhập!
Bạn chưa đăng nhập. Hãy đăng nhập để làm bài thi tại đây!
Cách pha loãng H2SO4 đặc an toàn là

Bóp mạnh quả bóp cao su của ống nghiệm chứa dung dịch HCl đặc vào dung dịch KMnO4. Hơ nhẹ ngọn lửa đèn cồn chỗ có miếng bông tẩm dung dịch KI.
Phát biểu đúng về thí nghiệm trên là
(1) O3+dung dịch KI→to (2) F2+H2O →to
(3) MnO2+HCl đặc→to (4) SO2+Br2+H2O→
Các phản ứng tạo ra đơn chất là
Bài 1:
Phân biệt các dung dịch sau bằng phương pháp hóa học, viết phương trình hóa học minh họa: Na2SO4, H2SO4, HCl.
Bài 2:
Viết các phương trình hóa học sau (ghi rõ điều kiện phản ứng, nếu có):
a. Br2+H2S+H2O→
b. Mg+O2→
c. CaCO3+HCl→
d. S+H2SO4đ→
Bài 3:
Cho 14,8 gam hỗn hợp A gồm Mg và Fe tác dụng với dung dịch H2SO4 đặc nguội, dư. Sau khi phản ứng hoàn toàn, thu được 3.36 lít một khí SO2 có mùi hắc (sản phẩm khử duy nhất, ở điều kiện tiêu chuẩn).
a. Tính khối lượng các kim loại trong hỗn hợp A.
b. Dẫn 3,36 lít khí SO2 (ở đktc) vào 500 ml dung dịch KOH 0.6M. Tính khối lượng chất tan thu được trong dung dịch sau phản ứng.
Bài 4:
Cho hình vẽ mô tả thí nghiệm điều chế khí Cl2 từ MnO2 và dung dịch HCl đặc sau:
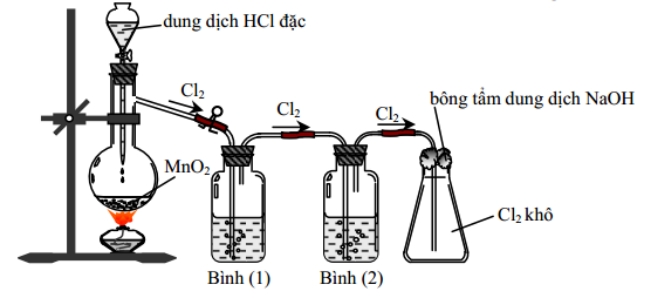
Em hãy cho biết:
- Bình (1) và bình (2) lần lượt chứa những dung dịch gì?
- Tác dụng của bông tẩm dung dịch NaOH. Viết phương trình hóa học minh họa.
