Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Trong 140 gam dung dịch KClO3 bão hòa ở 80°C có 40 gam KClO3. Nên trong 350 gam dung dịch KClO3 bão hào ở 80°C có 100 gam KClO3.
Trong 108 gam dung dịch KClO3 bão hòa ở 20°C có 8 gam KClO3. Gọi số gam KClO3 tách ra khỏi dung dịch là a. Khi đó khối lượng dung dịch và khối lượng KClO3 trong dung dịch thu được lần lượt là 350 – a và 100 – a (gam).
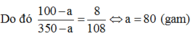

Độ tan của AgNO3 ở 60oC là 525(g)
Ở 60oC cứ 100g dung môi có 525g AgNO3
⇒Cứ 2500-mAgNO3 60o g dung môi có mAgNO3 60o g AgNO3
Lập tỉ lệ:\(\dfrac{100}{2500-m_{AgNO_3}}=\dfrac{525}{m_{AgNO_3}}\) ⇒ mAgNO3 60o=2100 (g) ⇒ mdm=400(g)
Ở 10oC cứ 100g dung môi có 170g AgNO3
⇒Cứ 400 g dung môi có mAgNO3 10oC g AgNO3
Lập tỉ lệ: \(\dfrac{100}{400}=\dfrac{170}{m_{AgNO_3}}\)⇒ mAgNO3 10oC=680(g)
⇒mtách ra=mAgNO3 60o -mAgNO3 10oC=2100-680=1420(g)

Nhiệt độ | Chất tan | Dung dịch |
10oC | 21,7 | 100 |
90oC | a + 21,7 | 100 + a |
a + 21,7 = 34,7%.(100 + a) → a = 19,908 (gam)
b) Giả sử nMgSO4.7H2O: b (mol)
Nhiệt độ | Chất tan | Dung dịch |
10oC | 41,608 | 119,908 |
90oC | 41,608 – 120b | 119,908 – 246b |
Suy ra: 41,608 – 120b = 21,7%.(119,908 – 246b) → b = 0,235
→ mMgSO4.7H2O = 57,802

Gọi khối lượng NaCl trong 1900 gam dd NaCl bão hòa ở 90oC là a (gam)
Có: \(S_{NaCl\left(90^oC\right)}=\dfrac{a}{1900-a}.100=50\)
=> a = \(\dfrac{1900}{3}\left(g\right)\)
=> \(m_{H_2O}=1900-\dfrac{1900}{3}=\dfrac{3800}{3}\left(g\right)\)
Gọi khối lượng NaCl trong dd NaCl bão hòa ở 0oC là b (gam)
Có: \(S_{NaCl\left(0^oC\right)}=\dfrac{b}{\dfrac{3800}{3}}.100=35\)
=> \(b=\dfrac{1330}{3}\left(g\right)\)
=> mNaCl (tách ra) = \(\dfrac{1900}{3}-\dfrac{1330}{3}=190\left(g\right)\)
\(m_{NaCl\left(tách\right)}=m_{NaCl\left(dd.bão.hoà.90^oC\right)}-m_{NaCl\left(dd.bão.hoà.0^oC\right)}\\ =\dfrac{1900}{100}.50-\dfrac{1900}{100}.35=285\left(g\right)\)
Em xem có gì không hiểu thì hỏi lại nha!

\(n_{Mg}=\dfrac{10,8}{24}=0,45\left(mol\right)\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
0,45-->0,45------>0,45--->0,45
=> \(m_{H_2SO_4}=0,45.98=44,1\left(g\right)\)
=> \(m_{ddH_2SO_4}=\dfrac{44,1.100}{20}=220,5\left(g\right)\)
mdd (20oC) = 10,8 + 220,5 - 0,45.2 - 14,76 = 215,64 (g)
\(m_{MgSO_4\left(dd.ở.20^oC\right)}=\dfrac{215,64.21,703}{100}=46,8\left(g\right)\)
=> nMgSO4 (tách ra) = \(0,45-\dfrac{46,8}{120}=0,06\left(mol\right)\)
=> nH2O (tách ra) = \(\dfrac{14,76-0,06.120}{18}=0,42\left(mol\right)\)
Xét nMgSO4 (tách ra) : nH2O (tách ra) = 0,06 : 0,42 = 1 : 7
=> CTHH: MgSO4.7H2O

Đặt công thức của tinh thể ngậm nước tách ra là MgSO4.nH2O
Trong 120 + 18n gam MgSO4.nH2O có 120 gam MgSO4 và 18n gam H2O
1,58 gam 0,237n gam
Khối lượng các chất trong 100 gam dung dịch bão hoà:
\(m_{H_2}=\frac{100.100}{35,1+100}=74,02g\)
\(m_{MgSO_4}=\frac{100.35,1}{35,1+100}\) = 25,98 gam
Khối lượng các chất trong dung dịch sau khi kết tinh:
\(m_{H_2O}\) = 74,02 – 0,237n gam
\(m_{MgSO_4}\)= 25,98 + 1 – 1,58 = 25,4 gam
Độ tan: s = \(\frac{25,4}{74,02-0,237n}.100=35,1\) . Suy ra n = 7.
Vậy công thức tinh thể ngậm nước kết tinh là MgSO4.7H2O

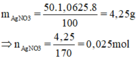
Phương trình hóa học của phản ứng:
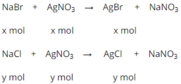
Biết nồng độ phần trăm của mỗi muối trong dung dịch bằng nhau và khối lượng dung dịch là 50g, do đó khối lượng NaCl bằng khối lượng NaBr.
Gọi nNaBr = x, nNaCl = y.
Theo pt: nNaBr = nAgNO3; nNaCl = nAgNO3
⇒ nNaBr + nNaCl = nAgNO3
Ta có hệ phương trình đại số: 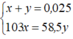
Giải ra, ta có x ≈ 0,009 mol
→ mNaBr = mNaCl = 103 x 0,009 = 0,927g
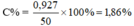
Ở 80 độ C, 192 gam KI tan trong 100 gam nước tạo 292 gam dung dịch bão hòa.
Suy ra 438 gam dung dịch bão hòa chứa
mKI=438.192\292=288 gam
→mH2O=438−288=150 gam
ở 20 độ C thì 144 gam KI tan trong 100 gam nước tạo dung dịch bão hòa
Suy ra 150 gam nước hòa tan được 144.150\100=216 gam KI.
→mKI tách ra=288−216=72 gam
Ở 80 độ C, 192 gam KI tan trong 100 gam nước tạo 292 gam dung dịch bão hòa.
Suy ra 438 gam dung dịch bão hòa chứa
\(m_{KI}=\frac{438.192}{292}=288\left(g\right)\)
\(\Rightarrow m_{H2O}=438-288=150\left(g\right)\)
Ở 20 độ C thì 144 gam KI tan trong 100 gam nước tạo dung dịch bão hòa
Suy ra 150 gam nước hòa tan được \(144.\frac{150}{100}=216\left(g\right)KI\)
\(\Rightarrow m_{KI\left(tach.ra\right)}=288-216=72\left(g\right)\)