Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án D
A: Mg, Zn tác dụng được với dung dịch Fe(NO3)2
B: Mg tác dụng được với dung dịch Fe(NO3)2
C: Cu không tác dụng với HCl

Đáp án D
Phương pháp: Dựa vào dãy điện hóa (quy tắc α)
Hướng dẫn giải:
Kim loại thu được là Ag. Do thu được 1 KL nên Fe, Mg hết.
Thứ tự các kim loại phản ứng với AgNO 3 : Mg, Fe
TH1:
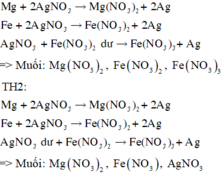

Chọn D
nCu2+ = 0,5V, nMg2+ = 0,3V, nH2 = 0,03mol
KL tan được trong dd HCl => Cu2+ và Ag+ hết
=> Bảo toàn e
0,5V . 2 + 0,3V = 0,045.2 + 0,05.2 – 0,03.2 = 0,13
=> V = 0,1 lít

Đáp án : C
Cu + 2Fe(NO3)3 à 2Fe(NO3)2 + Cu(NO3)2
X có Fe(NO3)2 ; Cu(NO3)2
Fe(NO3)2 + AgNO3 à Fe(NO3)3 + Ag
Y gồm Fe(NO3)3 ; AgNO3 ; Cu(NO3)2
Fe + 2AgNO3 à Fe(NO3)2 + 2Ag
Fe + Cu(NO3)2 à Fe(NO3)2 + Cu
Fe + 2Fe(NO3)3 à 3Fe(NO3)2
=> Có 5 phản ứng

Đáp án C
Ta có: nCu(NO3)2 = 0 , 2 m o l ; n A g N O 3 = 0 , 1 m o l
Ta có: 0,2.64 + 0,1.108 = 23,6 < 24,16 chứng tỏ Cu(NO3)2 và AgNO3 hết, còn kim loại dư.
Dung dịch Y tác dụng với HCl dư thu được 0,01 mol NO chứng tỏ Y chứa 0,03 mol Fe(NO3)2.
Bảo toàn điện tích: n Mg (NO 3 ) 2 = 0 , 2 . 2 + 0 , 1 - 0 , 03 . 2 2 = 0 , 22 m o l
Mặt khác do Y chứa Fe(NO3)2 nên kim loại chỉ có Fe dư và khối lượng Fe dư là 0,56 gam.
→ m x = 0 , 56 + 0 , 03 . 56 + 0 , 22 . 24 = 7 , 52 → %Fe = 29,79%

Chọn đáp án C
X phản ứng được với H2SO4 loãng ⇒ loại A và D.
Y phản ứng được với Fe(NO3)3 ⇒ chọn C.

Chọn C
X phản ứng được với H2SO4 loãng → X phải đứng trước H → Loại A và D
Y phản ứng được với dung dịch Fe3+ → Loại B vì cặp oxi hóa khử Ag+/Ag đứng sau Fe3+/Fe2+.
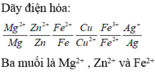
Chọn D