Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D.
Lời giải
M X = 4 , 7 . 4 = 18 , 8 = > m X = 2 M X = 37 , 6 ( g ) T a c ó : m X = m Y = 37 , 6 ( g ) = > n Y = 37 , 6 9 , 4 . 4 = 1 ( m o l )
Số mol khí giảm chính là số mol H2 phản ứng = > n H 2 p h ả n ứ n g = 1 ( m o l )
=
n
H
2
t
r
o
n
g
X
≥
1
(
m
o
l
)
=
>
n
a
n
d
e
h
i
t
t
r
o
n
g
X
≤
1
(
m
o
l
)
=
>
n
a
n
c
o
l
≤
1
(
m
o
l
)
Vì anđehit no, đơn chức, mạch hở => ancol no, đơn chức, mạch hở
⇒ n H 2 sin h r a t ừ p h ả n ứ n g c ộ n g N a = 1 2 n a n c o l ⇒ n H 2 sin h r a t ừ p h ả n ứ n g c ộ n g N a ≤ 0 , 5 ( m o l ) ⇒ V ≤ 11 , 2 ( l )
sinh ra từ phản ứng cộng Na sinh ra từ phản ứng cộng Na
Vậy giá trị lớn nhất của V là 11,2 lít

Ta thấy trong X có các ancol có đặc điểm: số C = số nhóm OH
=> Khi đốt cháy X : \(n_{CO_2}=n_{C\left(X\right)}=n_{OH}=0,25mol\)
=> Khi phản ứng vớ Na => \(n_{H_2}=\frac{1}{2}n_{OH}=0,125mol\)
=> V = 2,8 lít

Dễ thấy cả 2 axit đều có 2 H => HCOOH và HCOO - COOH
Đặt số mol 2 chất là x và y,đặt a = 1 thì
x + y = 1
x + 2y = 1,4
=> x = 0,6 ; y = 0,4
=> %mHCOOH = 43,4%

104,48gam104,48gam
Giải thích các bước giải:
Sơ đồ phản ứng:
⎧⎪ ⎪ ⎪⎨⎪ ⎪ ⎪⎩AlMgFeOFe3O4+HNO3−−−−−→⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩NO,N2OH2O⎧⎪⎨⎪⎩Al(NO3)2Mg(NO3)2Fe(NO3)2to→⎧⎨⎩Al2O3MgOFe2O3+NO2+O2{AlMgFeOFe3O4→+HNO3{NO,N2OH2O{Al(NO3)2Mg(NO3)2Fe(NO3)2→to{Al2O3MgOFe2O3+NO2+O2
Oxi chiếm 20,22%20,22% khối lượng hỗn hợp.
mO=25,32%.25,32=5,12gammO=25,32%.25,32=5,12gam
→nO=0,32mol→nO=0,32mol
Gọi số mol của NONO và N2ON2O lần lượt là xx và yy mol
⎧⎨⎩x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02{x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02
Quy đổi hỗn hợp X thành các nguyên tố: Al,Mg,Fe,OAl,Mg,Fe,O
→mKl=25,32−5,12=20,2g→mKl=25,32−5,12=20,2g
→mO(cr)=30,92−20,2=10,72gam→mO(cr)=30,92−20,2=10,72gam
→nO=0,67mol→nO=0,67mol
3nAl+3nFe+2nMg=2nO(cr)3nAl+3nFe+2nMg=2nO(cr)
Gọi số mol của NH4NO3NH4NO3 là xx mol
Bảo toàn e:
3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O
0,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.80,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.8
→nNH4NO3=0,015mol→nNH4NO3=0,015mol
Khối lượng muối:
m=mKl+mNO−3+mNH4NO3m=mKl+mNO3−+mNH4NO3
=20,2+0,67.2.62+0,015.80=104,48gam

Ta có: \(n_{COOH\left(X\right)}=n_{CO_2}=0,7mol\)
Khi đốt X có: \(n_{CO_2}=0,4mol;n_{CO_2}=0,8mol\)
Theo ĐLBT oxi có \(n_O=2n_{COOH\left(X\right)}+2n_{O_2}=2n_{CO_2}+n_{H_2O}\)
\(\Rightarrow n_{H_2O}=y=0,6mol\)
Đáp án là A
Hỗn hợp X: H2 và CnH2nO
M trước= 18.8 => mtrước=37.6g
2 mol X nhiệt độ, xúc tác Ni sau một thời gian M sau= 9.4*4=37.6
Ta có mtrước = msau => 37.6= 37.6*(2 - nH2 phản ứng)
=>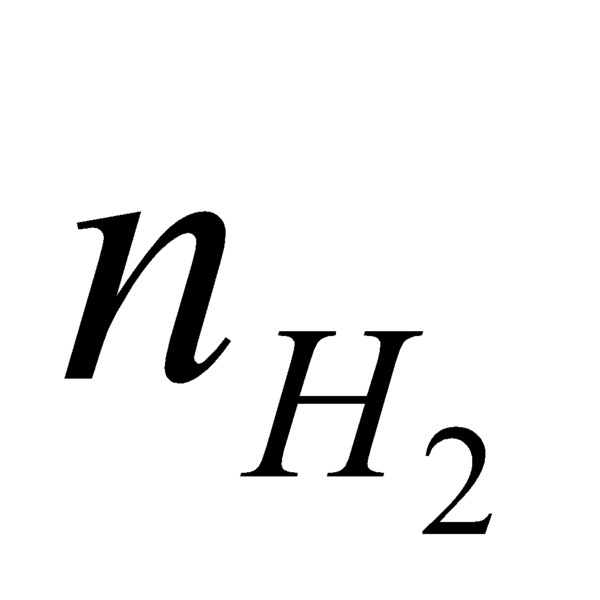 phản ứng = n rượu trong Y =2*
phản ứng = n rượu trong Y =2* 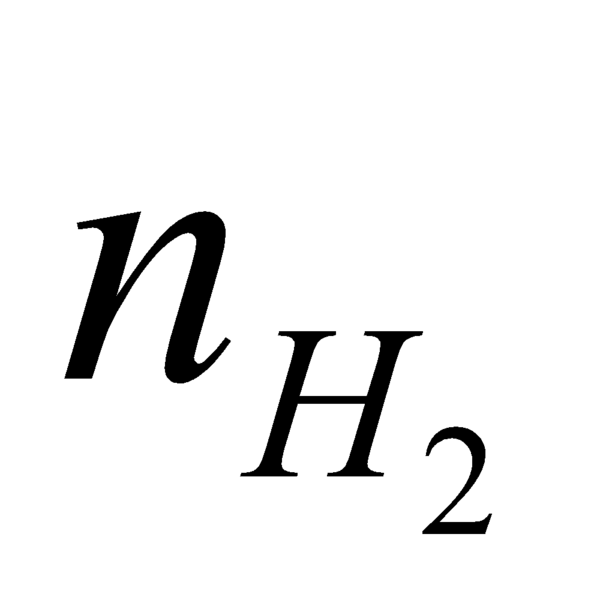 sinh ra = 1 mol
sinh ra = 1 mol
Nên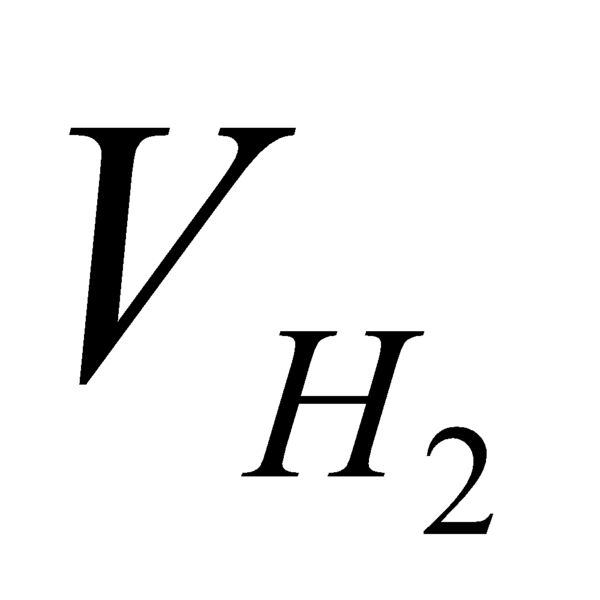 sinh ra=0.5*22.4= 11.2 lit
sinh ra=0.5*22.4= 11.2 lit