Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
a/ C l 2 + 2NaOH → NaCl + NaClO + H 2 O
b/ 2Al + 3 I 2 → x t 2AlI3
c/ M n O 2 + 4HCl → M n C l 2 + C l 2 + 2 H 2 O
d/ S i O 2 + 4HF → S i F 4 + 2 H 2 O
Các phản ứng oxi hóa – khử là: (a), (b), (c).

Chọn đáp án C
a/ 2 C l 2 + 2 C a O H 2 d d → C a C l 2 + C a O C l 2 + 2 H 2 O
b/ B r 2 + 2KI → 2KBr + I 2
c/ 2 K M n O 4 + 16HCl → 2KCl + 2 M n C l 2 + 5 C l 2 + 8 H 2 O
d/ N a 2 C O 3 + 2HCl → 2NaCl + C O 2 + H 2 O
→ chỉ phản ứng d không là phản ứng oxi hóa – khử.
Chú ý: C l 2 + C a O H 2 s ữ a v ô i → 30 0 C C a O C l 2 + H 2 O

Bạn tham khảo ở đây nha:Câu hỏi của Lê Quang Hiếu - Hóa học lớp 12 | Học trực tuyến
vì K+ và Na+ nên viết p.tử không chuẩn
a) khi cho H+ từ từ vào CO32- và HCO3- thì H+ td với CO32- trước vì nộng độ H+trong dd mới tạo thành nhỏ nên sẽ tác dụng từng nấc(vì chỉ từng giọt).lượng H+ chưa dư khi tác dụng với CO32- nên không thể tác dụng tiếp với HCO3- dẫn đến không có hiện tượng
H++CO32- -->HCO3-
b) khi cho H+ từ từ vào CO32- và HCO3- thì H+ td với CO32- trước. H+ tác dụng với CO32- còn dư tác dụng với 1 phần HCO3- tạo CO2 khí ko màu dd còn HCO3- tác dụng với OH- tạo CO32- td Ba2+ tạo kt trắng BaCO3
CO32-+H+-->HCO3-
HCO3-+H+-->H2O+CO2
HCO3-+OH-+Ba2+-->BaCO3+H2O(dư nên khi vậy ko dư ghi tỉ lệ Ba2+:OH-=1:2)
c)cho từ từ CO32- và HCO3- vào H+ thì pứ xảy ra đồng thời tạo đều tạo khí CO2 vì khi cho vào thì mt có nồng độ H+ lớn nên pứ xảy ra theo 2 nấc đồng thời
CO32-+2H+-->H2O+CO2
HCO3-+H+-->H2O+CO2

Đáp án C.
Các phương trình oxi hóa khử là I, II, III, IV.
Các pt phản ứng xảy ra:
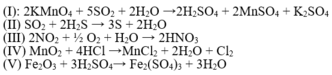

\(n_{H_2} = \dfrac{6,72}{22,4} = 0,3(mol)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ n_{Al} = \dfrac{2}{3}n_{H_2} = 0,2(mol)\\ 2Al + 6H_2SO_4 \to Al_2(SO_4)_3 + 3SO_2 + 6H_2O\\ Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + 2H_2O\\ n_{SO_2} = \dfrac{8,96}{22,4} = 0,4(mol)\\ \Rightarrow \dfrac{3}{2}n_{Al} + n_{Cu} = 0,4\\ \Rightarrow n_{Cu} = 0,1(mol)\\ \Rightarrow m = 0,2.27 + 0,1.64 = 11,8(gam)\)

\(n_{HCl}=2.0,4=0,8\left(mol\right)\rightarrow n_{Cl^-}=0,8\left(mol\right)\\ n_{NaOH}=1,1\left(mol\right)\rightarrow n_{OH^-}=1,1\left(mol\right)\)
PTHH:
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\left(1\right)\\ MgO+2HCl\rightarrow MgCl_2+H_2O\left(2\right)\\ CuO+2HCl\rightarrow CuCl_2+H_2O\left(3\right)\\ FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3\downarrow+3NaCl\left(4\right)\\ MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2\downarrow+2NaCl\left(5\right)\\ CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2\downarrow+2NaCl\left(6\right)\)
Để tạo kết tủa hoàn toàn thì \(n_{OH^-}=n_{Cl^-}\)
Mà thực tế \(n_{OH^-}>n_{Cl^-}\left(1,1>0,8\right)\)
=> Trong ddB có chứa NaOH dư và NaCl

PTPƯ 1:
\(Mg+2HCl->MgCl_2+H_2\)
0,1 0,2 0,1
\(Zn+2HCl->ZnCl_2+H_2\)
0,1 0,2 0,1
Gọi x, y là số mol của H2
Ta có hệ pt:
\(\left\{{}\begin{matrix}24x+65y=8,9\\22,4x+22,4y=4.48\end{matrix}\right.\)
\(=>x=y=0,1\left(mol\right)\)
\(M=\dfrac{n}{V}=\dfrac{0,2}{2}=0,1\left(M\right)\)
Pư 2 làm tg tự nha <3

Chọn C
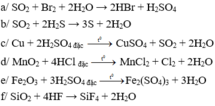
→ Các phản ứng a, b, c và d thuộc phản ứng oxi hóa – khử

1/ AgNO3 + KBr → AgBr + KNO3
AgNO3 + NaCl ⟶ AgCl + NaNO3
2/ Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
3/ \(Al+\dfrac{3}{2}Cl_2-^{t^o}\rightarrow AlCl_3\)
\(Fe+\dfrac{3}{2}Cl_2-^{t^o}\rightarrow FeCl_3\)
4/ CO2 + NaOH → Na2CO3 + H2O
SO2 + NaOH → Na2SO3 + H2O
a, \(8Al+3NaNO_3+5NaOH+2H_2O\rightarrow8NaAlO_2+3NH_3\)
\(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
b, Có lẽ phần này đề cho HI chứ không phải KI bạn nhỉ?
\(Fe_3O_4+8HI\rightarrow3FeI_2+I_2+4H_2O\)