Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)\(2KMnO4-->K2MnO4+MnO2+O2\)
b)\(n_{O2}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{KMnO4}=2n_{O2}=0,4\left(mol\right)\)
\(m_{KMnO4}=0,4.158=63,2\left(g\right)\)
c)\(3Fe+2O2-->Fe3O4\)
\(n_{Fe}=\frac{3}{2}n_{O2}=0,3\left(mol\right)\)
\(m_{Fe}=0,3.56=16,8\left(g\right)\)
\(n_{Fe3O4}=\frac{1}{2}n_{O2}=0,1\left(mol\right)\)
\(m_{Fe3O4}=0,1.232=23,2\left(g\right)\)

B1.
a) 4K + O2 -to-> 2K2O
K2O + H2O -> 2KOH
b) 4P + 5O2 -to-> 2P2O5
P2O5 + 3H2O -> 2H3PO4
2H3PO4 + 3Zn -> Zn3(PO4)2 + 3H2
c)Fe3O4 + 4H2 -to-> 3Fe + 4H2O
Fe + H2SO4 -> FeSO4 + H2
B2.
-Trích các nguyên liệu bài cho sẵn ra các ống nghiệm
-Đem điện phân nước thu được H2 và O2 :
PTHH. 2H2O -đp-> 2H2 + O2
-Dẫn khí H2 vừa thu được vào ống nghiệm đưng CuO cung cấp thêm to ta thu được Cu
PTHH. H2 + CuO -to-> Cu + H2O
-Dẫn khí O2 thu được ở pt 1 vào ống nghiệm đựng S cung cấp thêm to ta thu được SO2.Sau đó tiếp tục đốt SO2 trong O2 ta thu được SO3
PTHH. S + O2 --to-> SO2
2SO2 + O2 -to-> 2SO3
(p/s: chép mấy câu kia cx đc :v nếu ko thì bn chỉ chép pthh thôi nha :v)
Ý kiến. Ý kiến tý. muốn điều chế SO3 từ SO2 ta cần phải có chất xúc tác V2O5(vanadi oxit) theo PTHH:
V2O5
SO2+O2→→→ SO3.
ps: chỉ cần dùng 1 dấu mũi tên thôi. nhuwngddeere làm rõ hơn cho chất xúc tác nên mình làm thế!![]()

1. Khí Hiđro+Chì(||)oxit---->Chì +nước
H2 + PbO -to-> Pb+ H2O
2. Điphotpho pentaoxit +nước--> axit photphoric
P2O5 + 3 H2O -> 2 H3PO4
3. Magiê+axitClohiđric---> magiê clorua+khí Hiđro.
Mg + 2 HCl -> MgCl2 + H2
4. Natri +nước ----> natri hidroxit+khí hiđro
Na + H2O -> NaOH + 1/2 H2
5. Bari oxit+nước --> bari hidroxit.
BaO + H2O -> Ba(OH)2
6. Kali clorat --> Kali clorua+khí oxi
2 KClO3 -to-> 2 KCl + 3 O2
7. Sắt từ oxit+khí hiđro--->sắt+nước
Fe3O4 + 4 H2 -to-> 3 Fe + 4 H2O
8. Canxi +nước-->canxi hidroxit+khí hiđro
Ca + 2 H2O -> Ca(OH)2 + H2
9. ..............+..........--> Kali oxi.
4 K + O2 -to-> 2 K2O
10. Khí Hiđro+sắt(|||)oxit--->sắt+nước
3 H2 + Fe2O3 -to-> 2 Fe + 3 H2O
11. Kẽm +axit sunfuric--->kẽm sunfat +khí hiđro.
Zn + H2SO4 -> ZnSO4 + H2
12. Lưu huỳnh trioxit +nước-->axit sunfuric.
SO3 + H2O -> H2SO4

a) Phương trình hóa học của phản ứng:
3Fe + 2O2 → Fe3O4.
nFe3O4 = 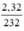 = 0,01 mol.
= 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.

a.\(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1mol\)
\(3Fe+2O_2\rightarrow Fe_3O_4\)
0,3 0,2 0,1 ( mol )
\(m_{Fe}=0,3.56=16,8g\)
\(V_{O_2}=0,2.22,4=4,48l\)
b.\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,4 0,2 ( mol )
\(m_{KMnO_4}=\dfrac{0,4.158}{90\%}=70,22g\)
Em hãy chọn cặp từ thích hợp điền vào chỗ trống:
Em hãy tả một loài cây mà em thích nhất trong đó có sử dụng các biện pháp tu từ,so sánh đó).

a) Phương trình hóa học của phản ứng:
3Fe + 2O\(_2\) → Fe\(_3\)O\(_4\).
nFe3O4 = \(\dfrac{2,32}{232}\) = 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.
a.
\(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,03 0,02 0,01 ( mol )
\(m_{Fe}=0,03.56=1,68g\)
\(m_{O_2}=0,02.32=0,64g\)
b.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,04 0,02 ( mol )
\(m_{KMnO_4}=0,04.158=6,32g\)


3Fe+2O2---->Fe3O4
a) n FE3O4=2,32/232=0,01(mol)
n Fe=3n Fe3O4=0,03(mol)
m Fe=0,03.56=1,68(g)
n O2=2n FE3O4=0,02(mol)
V O2=0,02.22,4=4,48(l)
b) 2KMnO4--->K2MnO4+MnO2+O2
n KMnO4=2n O2=0,04(mol)
m KMnO4=0,04.158=6,32(g)
1. 2 SO2 + O2 \(\xrightarrow[xt]{t^o}\) 2 SO3
2. Chưa rõ. Điều chế như thế nào nhỉ?
CuO + H2 -to-> Cu + H2O
2 H2 + O2 \(\underrightarrow{đp}\) 2 H2O
3. Fe + 2 HCl -> FeCl2 + H2
4. 2 KMnO4 -to-> K2MnO4 + MnO2 + O2
5. CuCl2 + Mg -> MgCl2 + Cu
6. 2 NO2 + H2O + 1/2 O2 -> 2 HNO3
7. 3 H2 + Fe2O3 -to-> 2 Fe + 3 H2O
8. K2O + H2O -> 2 KOH
1 S + O2➜SO2
2CuO +H2➜Cu +H2O
3 Fe + HCl➜FeCl2+H2
4 KMnO4 ➜K2MnO4 +MnO2 +O2
5 CuCl2+Mg➜Cu + MgCl2
6 NO2 +O2 +H2O➜HNO3
7 H2+Fe2O3➜Fe +H2O
KCl+O2➜KClO3