Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

gọi hóa trị của M trong hợp chất MCl2 là \(x\)
\(\rightarrow M^x_1Cl^I_2\rightarrow x.1=I.2\rightarrow x=II\)
vậy M hóa trị II
ta có CTHH: \(M^{II}_x\left(SO_4\right)^{II}_y\)
\(\rightarrow II.x=II.y\rightarrow\dfrac{x}{y}=\dfrac{II}{II}=\dfrac{1}{1}\rightarrow\left\{{}\begin{matrix}x=1\\y=1\end{matrix}\right.\)
\(\rightarrow CTHH:MSO_4\)
Gọi x là hóa trị của M
\(M_1^xCl_2^I\Rightarrow x=2\cdot I=2\Rightarrow M\left(II\right)\)
\(CTTQ:M_a^{II}\left(SO_4\right)_b^{II}\\ \Rightarrow a\cdot II=b\cdot II\Rightarrow\dfrac{a}{b}=1\Rightarrow a=1;b=1\\ \Rightarrow MSO_4\)

Do A hóa trị III => \(CTHHcủaX:A_2\left(SO_4\right)_3\)
\(M_X=171.2=342\left(đvC\right)\)
Ta có : \(2A+96.3=342\)
=> A=27 (Al)
=>\(CTHHcủaX:Al_2\left(SO_4\right)_3\)

a. gọi hóa trị của \(X\) và \(Y\) là \(x\)
\(\rightarrow X_1^xO^{II}_1\rightarrow x.1=II.1\rightarrow x=II\)
vậy \(X\) hóa trị \(II\)
\(\rightarrow Y_1^x\left(OH\right)^I_3\rightarrow x.1=I.3\rightarrow x=III\)
vậy \(Y\) hóa trị \(III\)
ta có: \(X_x^{II}Y^{III}_y\rightarrow II.x=III.y\)
\(\rightarrow\dfrac{x}{y}=\dfrac{III}{II}=\dfrac{3}{2}\rightarrow\left[{}\begin{matrix}x=3\\y=2\end{matrix}\right.\)
\(\rightarrow CTHH:X_3Y_2\)
b. ta có:
\(2X+1O=62\)
\(2X+1.16=62\)
\(2X=62-16\)
\(2X=46\)
\(X=\dfrac{46}{2}=23\left(đvC\right)\)
\(\Rightarrow X\) là\(Na\left(Natri\right)\)
\(\rightarrow CTHH:Na_2O\)

Ta có :
$M_{hợp\ chất} = X + 16 = 40 \Rightarrow X = 24$
Vậy X là nguyên tố Magie
CTHH với nhóm $NO_3$ là : $Mg(NO_3)_2

– Fe(III) với Cl(I).
Công thức chung có dạng: F e x C l y
Theo quy tắc hóa trị, ta có:
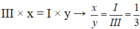
Công thức hóa học là: F e C l 3
Phân tử khối F e C l 3 là: 56 + 35,5 × 3 = 162,5 đvC.
– Các hợp chất của Nguyên tố sắt (III) với nhóm S O 4 (II); nhóm N O 3 (I); nhóm P O 4 (III); nhóm OH (I) lần lượt là: F e 2 ( S O 4 ) 3 , F e ( N O 3 ) 3 , F e P O 4 , F e ( O H ) 3 .
Phân tử khối của F e 2 ( S O 4 ) 3 là 56 × 2 + (32 + 16 × 4) × 3 = 400 đvC.
Phân tử khối của F e ( N O 3 ) 3 là 56 + (14 + 16 × 3) × 3 = 242 đvC.
Phân tử khối của F e P O 4 là 56 + 31 + 16 × 4 = 151 đvC.
Phân tử khối của F e ( O H ) 3 là 56 + (1 + 16) × 3 = 107 đvC.

Gọi hợp chất cần tìm là \(R_2O_3\)
a)Theo bài ta có:
\(PTK_{R_2O_3}=0,475M_{Br_2}=0,475\cdot81\cdot2=76\left(đvC\right)\)
b)Mà \(2M_R+3M_O=76\Rightarrow M_R=\dfrac{76-3\cdot16}{2}=14\left(đvC\right)\)
Vậy R là nguyên tố N(nito).
c)Gọi hóa trị của N là x.
Ta có: \(x\cdot2=2\cdot3\Rightarrow x=3\)
Vậy nguyên tố R có hóa trị lll.

Câu 1:
\(1,PTK_{H_2SO_4}=2+32+16\cdot4=98\left(đvC\right)\\ 2,PTK_{NaCl}=23+35,5=58,5\left(đvC\right)\\ 3,PTK_{Fe_3\left(PO_4\right)_2}=56\cdot3+\left(31+16\cdot4\right)\cdot2=358\left(đvC\right)\)
Câu 2:
\(a,SO_2\\ b,Na_2SO_4\)
Câu 3:
\(a,PTK_A=PTK_{H_2}\cdot40=2\cdot40=80\left(đvC\right)\\ b,NTK_X=PTK_A-3\cdot NTK_O=80-3\cdot16=32\left(đvC\right)\)
Do đó X là lưu huỳnh (S)
\(c,SO_3\)
Câu 1.
1) \(H_2SO_4\)\(\Rightarrow2+32+4\cdot16=98\left(đvC\right)\)
2) \(NaCl\Rightarrow23+35,5=58,5\left(đvC\right)\)
3) \(Fe_3\left(PO_4\right)_2\)\(\Rightarrow3\cdot56+31\cdot2+8\cdot16=360\left(đvC\right)\)
Câu 2.
a) \(SO_3\) b) \(Na_2SO_4\)
Câu 3.
Gọi hợp chất A cần tìm là: \(XO_3\) có phân tử khối nặng gấp 40 phân tử khí H2.
\(\Rightarrow\)Phân tử khối hợp chất A là 40*2=80(đvC)
\(\Rightarrow M_X+3M_O=80\) \(\Rightarrow M_X=80-3\cdot16=32\)
Vậy X là lưu huỳnh.KHHH: S
Hợp chất A tạo bởi 1 nguyên tử nguyên tố X và 3 nguyên tử Oxi nên hợp chất A cần tìm là \(SO_3\)

Câu 3 :
\(M_R=0.5M_S=0.5\cdot32=16\left(\dfrac{g}{mol}\right)\)
\(R:O\)
O là : nguyên tố phi kim
b.
Oxi tạo nên đơn chất : O2
Câu 2:
CT dạng chung : \(Fe_x\left(NO_3\right)_y\)
Áp dụng qui tắc về hóa trị, ta có: \(x\cdot II=y\cdot I\) hoặc \(\left(x\cdot III=y\cdot I\right)\)
Rút ra tỉ lệ : \(\dfrac{x}{y}=\dfrac{I}{II}=\dfrac{1}{2}\) hoặc \(\dfrac{x}{y}=\dfrac{I}{III}=\dfrac{1}{3}\)
CTHH : \(Fe\left(NO_3\right)_2\) hoặc \(Fe\left(NO_3\right)_3\)
\(M_{Fe\left(NO_3\right)_2}=56+62\cdot2=180\left(đvc\right)\)
hoặc
\(M_{Fe\left(NO_3\right)_3}=56+62\cdot3=242\left(đvc\right)\)
CTHH: Fe2O3
\(\%m_{Fe}=\dfrac{56.2}{56.2+16.3}.100\%=70\%\\ \%m_O=100\%-70\%=30\%\)
a. F2O3: %mFe = 70%; %mO = 30%
b. Al(NO3)3: %mAl = 12,7%; %mN = 19,7%; %mO = 67,6%
c. Fe2(SO4)3: mFe = 28%; %mS= 24%; %mO= 48%