Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(2NaCl+H_2SO_4\rightarrow Na_2SO_4+2HCl\)
15299_____________________15299
\(m_{dd_{HCl}}=1250.100.1,19=1487500\)
\(m_{HCl}=1487500.37\%=550375\)
\(n_{HCl}=\frac{550375}{36,5}=15079\)
\(n_{NaCl}=\frac{0,895.1000.1000}{58,5}=15299\)
\(\Rightarrow H=\frac{15079}{15299}.100=98,56\%\)

Lượng NaCl nguyên chất:
1000kg x 95% = 950kg
Lượng HCl thu được theo lí thuyết :
2NaCl + H2SO4 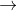 Na2SO4 + 2HCl
Na2SO4 + 2HCl
58,5 g 36,5g
950kg x = 589kg
Lượng HCl thu được theo thực tế:
1250 lit x 1,19kg/lit x 37% = 550,375 kg
Hiệu suất của quá trình điều chế:
H% = 550,375\589 x100% = 92,44 %
=>A

20 tấn = 20 000 kg
\(m_{NaCl} = 20 000.90\% = 18000(kg)\\ n_{NaCl} = \dfrac{18000}{58,5}= \dfrac{4000}{13}(kmol)\\ n_{NaCl\ pư} = \dfrac{4000}{13}.65\% = 200(kmol)\\ 2NaCl + 2H_2O \xrightarrow{đpdd} 2NaOH + Cl_2 + H_2\\ n_{Cl_2} = \dfrac{1}{2}n_{NaCl} = 100(kmol)\\ V_{Cl_2} = 100.22,4 = 2240(m^3)\)

1.
mNaCl lí thuyết = \(\dfrac{4,68.100}{80}\) = 5,85 (g)
=> nNaCl lí thuyết = \(\dfrac{5,85}{58,5}\) = 0,1 (mol)
2Na + Cl2 ----> 2NaCl
0,1 0,05 0,1 (mol)
=> mNa = 0,1.23 = 2,3 (g)
=> VCl2 = 0,05.22,4 = 1,12 (l)
2.
nZn = \(\dfrac{19,5}{65}\)= 0,3 (mol)
nCl2 = \(\dfrac{7}{22,4}\)= 0,3125 (mol)
Zn + Cl2 ----> ZnCl2
0,3 0,3 (mol)
Tỉ lệ: \(\dfrac{0,3}{1}<\dfrac{0,3125}{1}\)=> Zn phản ứng hết, Cl2 phản ứng dư.
=> mZnCl2 lí thuyết 0,3.136 = 40,8 (g)
=> H = \(\dfrac{36,72.100}{40,8}\)= 90%

Người ta có thể điều chế Cl 2 , Br 2 , I 2 bằng cách cho hỗn hợp dung dịch H 2 SO 4 đặc và MnO 2 tác dụng với muối clorua, bromua, iotua
Các sản phẩm trung gian là HCl, HBr, HI bị hỗn hợp ( MnO 2 + H 2 SO 4 ) oxi hoá thành Cl 2 , Br 2 , I 2 . Các PTHH có thể viết như sau :
NaCl + H 2 SO 4 → Na HSO 4 + HCl
MnO 2 + 4HCl → Mn Cl 2 + Cl 2 + 2 H 2 O
Các phản ứng cũng xảy ra tương tự đối với muối NaBr và NaI.
Không thể áp dụng phương pháp trên để điều chế F 2 vì hỗn hợp oxi hoá ( MnO 2 + H 2 SO 4 ) không đủ mạnh để oxi hoá HF thành F 2
Cách duy nhất điều chế F 2 là điện phân KF tan trong HF lỏng khan Dùng dòng điện một chiểu 8-12 von ; 4000 - 6000 ampe ; Bình điện phân có catôt làm bằng thép đặc biệt hoặc bằng đồng và anôt làm bằng than chì (graphit).
Ở catot: 2 H + + 2 e → H 2
Ở anot: 2 F - → F 2 + 2 e

Điều chế HF, HCl bằng cách cho H 2 SO 4 đặc tác dụng với muối florua, clorua vì H 2 SO 4 à chất oxi hoá không đủ mạnh để oxi hoá được HF và HCl. Nói cách khác, HF và HCl có tính khử yếu, chúng không khử được H 2 SO 4 đặc
Ca F 2 + H 2 SO 4 → Ca SO 4 + 2HF
NaCl + H 2 SO 4 → NaH SO 4 + HCl
Nhưng không thể dùng phương pháp trên để điều chế HBr và HI vì H 2 SO 4 đặc oxi hoá được những chất này thành Br 2 và I 2 . Nói cách khác, HBr và HI là những chất có tính khử mạnh hơn HCl và HF.
NaBr + H 2 SO 4 → HBr + NaH SO 4
2HBr + H 2 SO 4 → Br 2 + SO 2 + 2 H 2 O
NaI + H 2 SO 4 → NaH SO 4 + HI
2HI + H 2 SO 4 → I 2 + SO 2 + 2 H 2 O
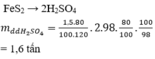
\(m_{NaCl\left(bd\right)}=\dfrac{1.89,5.10^6}{100}=895000\left(g\right)\)
\(m_{ddHCl}=1250.10^3.1,19=1487500\left(g\right)\)
=> \(n_{HCl}=\dfrac{1487500.37\%}{36,5}=\dfrac{550375}{36,5}\left(mol\right)\)
=> \(n_{NaCl\left(pư\right)}=\dfrac{550375}{36,5}\left(mol\right)\)
=> \(H\%=\dfrac{\dfrac{550375}{36,5}.58,5}{895000}.100\%=98,56\%\)
Một tấn muối ăn chứa 10,5% tạp chất.
\(\Rightarrow\)Nó chứa 89,5% muối nguyên chất.
\(\Rightarrow m_{NaCl}=1\cdot89,5\%=0,895tấn\)
\(m_{ddHCl}=D\cdot V=1,19\cdot1250\cdot1000=1487500g\)
\(\Rightarrow m_{HCl}=\dfrac{1487500\cdot37\%}{100\%}=550375g\)
\(\Rightarrow n_{HCl}=15078,76712mol\)
\(n_{NaCl}=\dfrac{0,895\cdot10^6}{23+35,5}=15299,1453mol\)
\(H=\dfrac{n_{HCl}}{n_{NaCl}}=\dfrac{15078,76712}{15299,1453}=98,56\%\)