
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


TỰ LUẬN
1. Tham khảo SGK lớp 8 để trả lời nha em!
2. a) \(CuS+2HCl-^{t^o}\rightarrow CuCl_2+H_2S\) (Theo mình nhớ thì cái phản ứng này không xảy ra nhưng mà không biết vì sao trong đề vẫn cho phản ứng nên mình cứ viết thôi :3 )
\(b.CaCO_3-^{t^o}\rightarrow CaO+CO_2\\ c.4P+5O_2-^{t^o}\rightarrow2P_2O_5\\ d.Cl_2+H_2-^{t^o}\rightarrow2HCl\)
3. \(a.m_{CuO}=0,05.\left(64+16\right)=4\left(g\right)\\ b.V_{H_2}=0,02.22,4=0,448\left(l\right)\\ c.Tacó:n_{H_2}=\dfrac{P.V}{R.T}=0,02\\ \Rightarrow\dfrac{1.V}{0,082.\left(273+25\right)}=0,02\\ \Rightarrow V_{H_2}=0,48872\left(l\right)\\ d.Tacó:n_{H_2}=\dfrac{P.V}{R.T}=0,02\\ \Rightarrow\dfrac{1.V}{0,082.\left(273+20\right)}=0,02\\ \Rightarrow V_{H_2}=0,48052\left(l\right)\)

10 :
Hidro có tính khử
có thể tác dụng với 1 số oxit kim loại :
VD: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
có thể tác dụng với Oxi
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
11
thu khí Oxi bằng cách đẩy kk phải để ngửa bình vì Oxi nặng hơn kk
ko thể áp dụng với H2 vì H2 nhẹ hơn kk nên phải đặt úp bình
12
a ) \(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
b) \(Ag_2O+H_2\underrightarrow{t^o}2Ag+H_2O\)

$2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
$n_{O_2} = a = \dfrac{3}{2}n_{KClO_3} = \dfrac{3}{2}(mol)$
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
$n_{O_2} = b = \dfrac{1}{2}n_{KMnO_4} = \dfrac{1}{2}(mol)$
\(\dfrac{a}{b}=\dfrac{\dfrac{3}{2}}{\dfrac{1}{2}}=3\). Suy ra a = 3b
Đáp án B

Trả lời :
Câu 10. Hợp chất của một nguyên tố R với hiđro có công thức hoá học là RH4 chứa 25% hiđro về khối lượng. Tên của R là
A. nhôm B. photpho C. silic D. cacbon
HD : Xét về hoá trị với hydro ta loại được 2 trường hợp nhôm và photpho (hợp chất tương ứng của chúng là : \(AlH_3\) (Aluman) và \(PH_3\) (Photphin))
Còn lại 2 trường hợp ta ghép và tính phân tử khối rồi tính thành phần % nguyên tố. Ta thấy \(CH_4\) là hợp lệ với đề bài.
Vậy nguyên tố cần chọn là cacbon
~HT~

Bài 1:
\(a,4P+5O_2\xrightarrow{t^o}P_2O_5\\ b,8HCl+Fe_3O_4\to FeCl_2+2FeCl_3+4H_2O\)

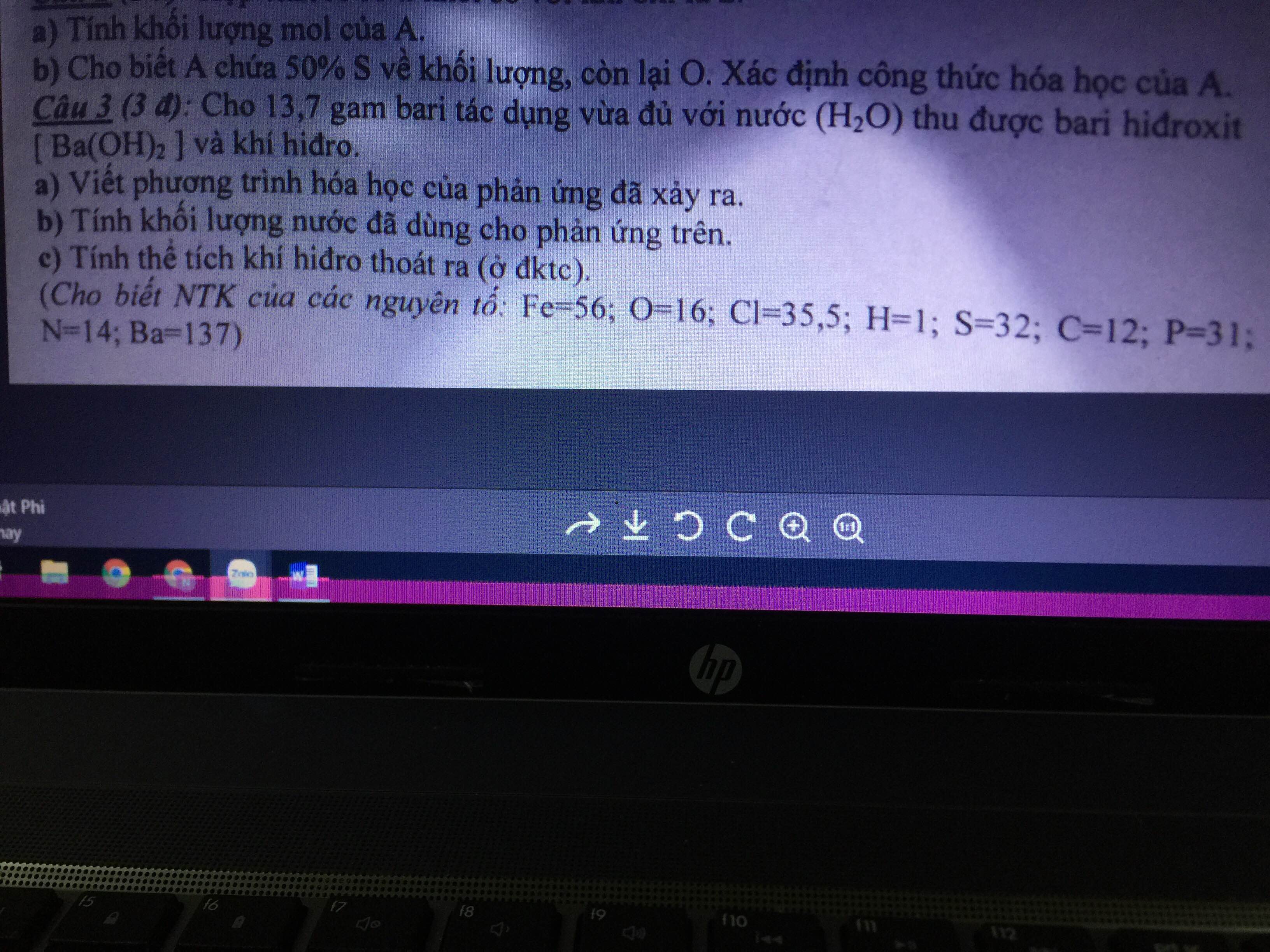
\(a.PTHH:Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
\(b.n_{Ba}=\dfrac{m}{M}=\dfrac{13,7}{137}=0,1\left(mol\right)\)
\(\Rightarrow n_{H_2O}=\dfrac{1}{2}.n_{Ba}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\\ \Rightarrow m_{H_2O}=n.M=0,9\left(g\right)\)
\(c.n_{Ba}=0,1\left(mol\right)\Rightarrow n_{H_2}=n_{Ba}=0,1\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=n.22,4=0,1.22,4=2,24\left(l\right)\)

Câu 1:
a, \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
b, \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,3\left(mol\right)\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
c, \(n_{HCl}=3n_{Al}=0,6\left(mol\right)\)
\(\Rightarrow C\%_{HCl}=\dfrac{0,6.36,5}{200}.100\%=10,95\%\)
d, \(n_{AlCl_3}=n_{Al}=0,2\left(mol\right)\Rightarrow m_{AlCl_3}=0,2.133,5=26,7\left(g\right)\)
 tự luận nha
tự luận nha



8.
Số nguyên tử Fe: \(6.10^{23}.2,5=1,5.10^{24}\)
9.
Số phân tử NaCl: \(4.6.10^{23}=2,4.10^{24}\)
10.
\(V_{O_2}=22,4.0,75=16,8\left(l\right)\)
Câu 8:
Số nguyên tử Fe trong 2,5 mol Fe:
2,5.6.1023= 15.1023=1,5.1024 (nguyên tử)
=> CHỌN D
Câu 9:
Số phân tử NaCl trong 4 mol phân tử muối ăn NaCl:
6.1023.4=2,4.1024 (phân tử)
=> CHỌN D
Câu 10:
V(O2,đktc)=nO2.22,4=0,75.22,4=16,8(l)
=> CHỌN A