Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Zn + 2HCl \to ZnCl_2 + H_2\\ Zn + H_2SO_4 \to ZnSO_4 + H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ Fe + H_2SO_4 \to FeSO_4 + H_2\\ n_{Fe} = n_{Zn} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)\\ m_{Fe} = 0,1.56 = 5,6(gam) ; m_{Zn} = 0,1.65 = 6,5(gam)\)

a. Phương trình hóa học có thể điều chế hiđro.
Zn + 2HCl → ZnCl2 + H2
Fe + H2SO4 (loãng) → FeSO4 + H2
Zn + H2SO4 → ZnSO4 + H2
Fe + 2HCl → FeCl2 + H2
b. Số mol khí hiđro là: n = 0,1 (mol)
Khối lượng kẽm cần dùng là: m = 0,1x65 = 6,5 (g)
Khối lượng sắt cần dùng là: m = 0,1x56 = 5,6 (g).
Phan Thùy Linh tại sao lại số mol của H2 bằng 0,1 (vậy số liệu 2,24 l đang ở đâu, làm sao có kết quả này).
Khi viết m, viết n em có biết khối lượng của cái gì hay là số mol của cái gì đâu. dù đã dẫn ở lời giải nhưng vẫn phải viết chứ.
Đối với những phản ứng điều chế khí thì khí thường bay hơi nên phải có chiều mũi tên đi lên nhé.
Đối với phản ứng số (3) thì Zn chỉ phản ứng được với "H2SO4 (loãng)" thôi.

Phương trình hóa học của phản ứng:
Fe + H2SO4 → FeSO4 + H2.
Zn + H2SO4 → ZnSO4 + H2.
Fe + 2HCl → FeCl2 + H2.
Zn + 2HCl → ZnCl2 + H2.
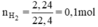
Theo phương trình (3) mFe cần dùng: 56.0,1 = 5,6g.
Theo phương trình (4) mZn cần dùng: 65.0,1 = 6,5g.

Câu 5:
PTHH : H2+ Cl2 -to-> 2 HCl
Vì số mol , tỉ lệ thuận theo thể tích , nên ta có:
25/1 = 25/1 => P.ứ hết, không có chất dư, tính theo chất nào cũng được
=> V(HCl)= 2. V(H2)= 2. 25= 50(l)
Câu 4: mFe2O3= 0,6. 80= 48(g)
=> nFe2O3= 48/160=0,3(mol)
mCuO= 80-48=32(g) => nCuO=32/80=0,4(mol)
PTHH: CuO + CO -to-> Cu + CO2
0,4_______0,4_____0,4____0,4(mol)
Fe2O3 + 3 CO -to-> 2 Fe +3 CO2
0,3_____0,9____0,6______0,9(mol)
=>nCO= 0,4+ 0,9= 1,3(mol)
=> V(CO, đktc)= 1,3. 22,4=29,12(l)

![]()
Để điều chế 0,05 mol H 2 thì:
n Z n = n M g = 0,05 mol mà M M g < M Z n
⇒ Dùng Mg sẽ cần khối lượng nhỏ hơn
n H C l = 2 . n H 2 = 0,05 . 2 = 0,1 mol ⇒ m H C l = 0,1 . 36,5 = 3,65 g
n H 2 S O 4 = n H 2 = 0,05 mol ⇒ m H 2 S O 4 = 0,05 .98 = 4,9g
⇒ Dùng axit HCl sẽ cần khối lượng nhỏ hơn
Nên với những chất đã cho muốn dùng với khối lượng nhỏ nhất để điều chế H 2 ta dùng Mg và axit HCl

1. Tính khối lượng chất tham gia và sản phẩm
* Các bước giải:
- Đổi số liệu đầu bài. Tính số mol của chất mà đầu bài cho.
- Lập phương trình hoá học.
- Dựa vào số mol chất đã biết để tính số mol chất cần tìm.
2. Tính thể tích khí tham gia và tạo thành
H2+Cl2->2HCl
\(n_{H_2}=67,2:22,4=3\left(mol\right)\)
Ta có: \(n_{H_2}=n_{Cl_2}=3\left(mol\right)\)
\(V_{Cl_2}=3.22,4=67,2l\)
\(n_{HCl}=2n_{Cl_2}=2.3=6\left(mol\right)\)
\(m_{HCl}=6.36,5=219g\)

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH:
Mg + 2HCl ---> MgCl2 + H2
Zn + 2HCl ---> ZnCl2 + H2
Fe + 2HCl ---> FeCl2 + H2
Mg + H2SO4 ---> MgSO4 + H2
Zn + H2SO4 ---> ZnSO4 + H2
Fe + H2SO4 ---> FeSO4 + H2
Theo các pthh trên: \(\left\{{}\begin{matrix}n_{HCl}=2n_{H_2}=2.0,1=0,2\left(mol\right)\\n_{H_2SO_4}=n_{H_2}=0,1\left(mol\right)\\n_{Fe}=n_{Zn}=n_{Mg}=n_{H_2}=0,1\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}\left\{{}\begin{matrix}m_{HCl}=0,2.36,5=7,3\left(g\right)\\m_{H_2SO_4}=98.0,1=9,8\left(g\right)\end{matrix}\right.\\\left\{{}\begin{matrix}m_{Fe}=0,1.56=5,6\left(g\right)\\m_{Zn}=0,1.65=6,5\left(g\right)\\m_{Mg}=0,1.24=2,4\left(g\right)\end{matrix}\right.\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}m_{HCl}< m_{H_2SO_4}\\m_{Mg}< m_{Fe}< m_{Zn}\end{matrix}\right.\)
Vậy chọn HCl và Mg thì đièu chế vs lượng nhỏ nhất
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
Nếu dùng HCl:
\(n_{HCl}=2n_{H_2}=0,2mol\Rightarrow m_{HCl}=0,2\cdot36,5=7,3g\)
Nếu dùng \(H_2SO_4\) :
\(n_{H_2SO_4}=n_{H_2}=0,1mol\Rightarrow m_{H_2SO_4}=0,1\cdot98=9,8g\)
\(\Rightarrow\)Dùng \(HCl\) để cần một khối lượng nhỏ nhất.
Nếu dùng Mg:
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,1 0,1
\(m_{Mg}=0,1\cdot24=2,4g\)
Nếu dùng Zn:
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,1
\(m_{Zn}=0,1\cdot65=6,5g\)
Nếu dùng Fe:
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,1
\(m_{Fe}=0,1\cdot56=5,6g\)
\(\Rightarrow\)Dùng Mg để có khối lượng nhỏ nhất.
Vậy dùng kim loại Mg và axit HCl.
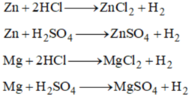
a. Phương trình hóa học có thể điều chế hiđro.
Zn + 2HCl → ZnCl2 + H2 ↑
Fe + H2SO4 (loãng) → FeSO4 + H2 ↑
Zn + H2SO4 → ZnSO4 + H2 ↑
Fe + 2HCl → FeCl2 + H2 ↑
b. Ta có
nH2 = \(\dfrac{2,24}{22,4}\) = 0,1 (mol)
mzn = 0,1 . 65 = 6,5 ( gam )
mFe = 0,1 . 56 = 5,6 ( gam ).
a. Phương trình hóa học có thể điều chế hiđro.
Zn + 2HCl → ZnCl2 + H2 ↑
Fe + H2SO4 (loãng) → FeSO4 + H2 ↑
Zn + H2SO4 → ZnSO4 + H2 ↑
Fe + 2HCl → FeCl2 + H2 ↑
b. Số mol khí hiđro là: n = \(\dfrac{2,24}{22,4}\)= 0,1 (mol)
Khối lượng kẽm cần dùng là: m = 0,1x65 = 6,5 (g)
Khối lượng sắt cần dùng là: m = 0,1x56 = 5,6 (g).