Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Tốc độ góc ω = v/r.
Trong chuyển động của e quanh hạt nhân thì lực tương tác điện giữa hạt nhân và e đóng vai trò là lực hướng tâm.

Mà
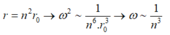
→ Trong các mức năng lượng từ K đến P sẽ có 3 khả năng làm giảm tốc độ góc của electron 8 lần (tức tăng bán kính quỹ đạo 2 lần) đó là:
- Electron từ quỹ đạo K (n = 1) chuyển lên quỹ đạo L (n = 2)
- Electron từ quỹ đạo L (n = 2) chuyển lên quỹ đạo N (n = 4)
- Electron từ quỹ đạo M (n = 3) chuyển lên quỹ đạo P (n = 6).

+ Bán kính nguyên tử Hidro theo mẫu Bo được xác định bởi rn = n2r0
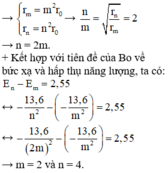
→ Bước sóng nhỏ nhất mà nguyên tử có thể phát ra ứng với sự chuyển từ mức năng lượng n = 4 về mức năng lượng cơ bản n = 1.
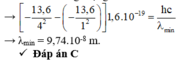

+ Bán kính nguyên tử Hidro theo mẫu Bo được xác định bởi rn = n2r0
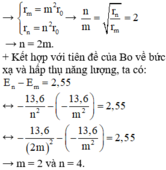
→ Bước sóng nhỏ nhất mà nguyên tử có thể phát ra ứng với sự chuyển từ mức năng lượng n = 4 về mức năng lượng cơ bản n = 1.
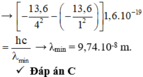

+ Bán kính nguyên tử Hidro theo mẫu Bo được xác định bởi rn = n2r0
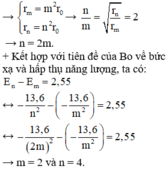
→ Bước sóng nhỏ nhất mà nguyên tử có thể phát ra ứng với sự chuyển từ mức năng lượng n = 4 về mức năng lượng cơ bản n = 1.
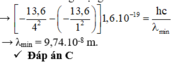

Đáp án: B
rm = m2r0; rn = n2r0 ( với r0 bán kính Bo)
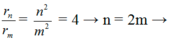
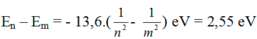
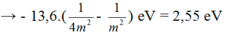
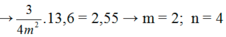
Bước sóng nhỏ nhất ng tử hidro có thể phát ra:
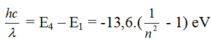
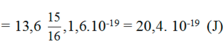
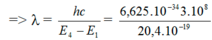
![]()

Đáp án C
Bán kính quỹ đạo được xác định theo biểu thức r = n2r0
Vì bán kính quỹ đạo tăng lên 9 lần nên n = 3.
Bước sóng của bức xạ có năng lượng lớn nhất ứng với sự chênh lệch năng lượng nhiều nhất, tức là chuyển từ mức 3 về mức 1 nên có:
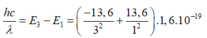
→ λ = 0,103 µm.

Đáp án A
Khi electron chuyển động quanh hạt nhân thì lực điện đóng vai trò là lực hướng tâm nên:
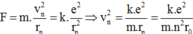
Khi electron chuyển từ quỹ đạo n về quỹ đạo m thì:
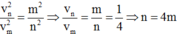
=> Electron chuyển từ quỹ đạo N (n=4) về quỹ đạo K (m=1).

Đáp án D
Bán kính quỹ đạo tỉ lệ với bình phương của số quỹ đạo
Ở mức năng lượng K; L; M, N, O, P thì có n tương ứng là: 1; 2; 3; 4; 5; 6
Công thức tính bán kính của của các quỹ đạo tương ứng: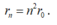 .
.
Bán kính tăng 4 lần chỉ có:
Vậy có 2 khả năng kích thích electron tăng bán kính quỹ đạo lên 4 lần