Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1. C + H2O \(\underrightarrow{t^o}\) CO + H2
C + 2H2O \(\underrightarrow{t^o}\) CO2 + 2H2.
2. Lượng Cu thu được là 0,4 mol, suy ra lượng đồng (II) oxit phản ứng là 0,4 mol. Lượng nguyên tử oxi phản ứng là 0,4 mol.
Suy ra, tổng lượng CO và H2 trong X là 0,4 mol. Lượng khí X là 0,5 mol. Suy ra, số mol CO2 là 0,1 mol.
Gọi a mol và b mol lần lượt là số mol của CO và H2 có trong X.
Lượng C và H2O ban đầu lần lượt là (0,1+a) mol và b mol.
BTKL: 12(0,1+a)+18b=28a+2b+44.0,1 (1)
a+b=0,4 (2).
Từ (1) và (2), suy ra a=0,1 và b=0,3.
Tỉ lệ phần trăm thể tích các khí có trong X:
%VCO=0,1/0,5=20%, %\(V_{H_2}\)=0,3/0,5=60%, %\(V_{CO_2}\)=20%.
Phân tử khối trung bình của X là (28.0,1+2.0,3+44.0,1)/0,5=7,6.
Tỉ khối của X so với oxi là dX/O=7,6/16=0,475.

PT: Fe2O3+3H2to→2Fe+3H2O
CuO+H2to→Cu+H2O
a, Ta có: mFe2O3=20.60%=12(g)
⇒nFe2O3=\(\dfrac{12}{160}\)=0,075(mol
mCuO=20−12=8(g
⇒nCuO=\(\dfrac{8}{80}\)=0,1(mol)
Theo pT:
nFe=2nFe2O3=0,15(mol)
nCu=nCuO=0,1(mol)
⇒mFe=0,15.56=8,4(g)
mCu=0,1.64=6,4(g)
b, Theo PT: nH2=3nFe2O3+nCuO=0,325(mol)
⇒VH2=0,325.22,4=7,28(l)
c. Zn+2HCl->ZnCl2+H2
0,65----------0,325
=>m HCl=0,65.36,5=23,725g

nCu = 8: 80=0,1(mol)
a) PTHH : CuO + H2 -t--> Cu +H2O
0,1-> 0,1------>0,1(mol)
mCu = 0,1.64=6,4(g)
VH2 = 0,1.22,4=2,24(l)

\(n_{Fe}=\dfrac{2,8}{56}=0,05mol\)
\(\Rightarrow m_{Cu}=6-2,8=3,2g\)\(\Rightarrow n_{Cu}=0,05mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,05 0,05
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
0,075 0,05
\(\Rightarrow\Sigma n_{H_2}=0,075+0,05=0,125mol\)
\(\Rightarrow V=0,125\cdot22,4=2,8l\)

\(m_{CuO}=50.20\%=10\left(g\right)\)
\(n_{CuO}=\dfrac{10}{80}=0,125\left(mol\right)\)
\(m_{Fe_2O_3}=50-10=40\left(g\right)\)
\(n_{Fe_2O_3}=\dfrac{40}{160}=0,25\left(mol\right)\)
PTHH :
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
0,125 0,125 0,125
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
0,25 0,75 0,5
\(a,V_{H_2}=\left(0,75+0,125\right).22,4=19,6\left(l\right)\)
\(b,m_{Cu}=0,125.64=8\left(g\right)\)
\(m_{Fe}=0,5.56=28\left(g\right)\)

Gọi: \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_X=b\left(mol\right)\end{matrix}\right.\) ⇒ 56a + MX.b = 21,4 (1)
- Đốt A trong oxi.
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(2X+O_2\underrightarrow{t^o}2XO\)
Theo PT: \(n_{O_2}=\dfrac{2}{3}n_{Fe}+\dfrac{1}{2}n_X=\dfrac{2}{3}a+\dfrac{1}{2}b=\dfrac{4,48}{22,4}=0,2\left(mol\right)\left(2\right)\)
- Cho pư với HCl
+ TH1: X không pư với HCl.
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{Fe}=n_{H_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)=a\)
Thay vào (2) được b = -1/15 → vô lý.
+ TH2: X có pư với HCl.
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(X+2HCl\rightarrow XCl_2+H_2\)
Theo PT: \(n_{H_2}=n_{Fe}+n_X=a+b=\dfrac{7,84}{22,4}=0,35\left(mol\right)\left(3\right)\)
Từ (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}a=0,15\left(mol\right)\\b=0,2\left(mol\right)\end{matrix}\right.\). Thay vào (1) được MX = 65 (g/mol)
Vậy: X là kẽm. (Zn)

a)
$CO_2 +C a(OH)_2 \to CaCO_3 + H_2O$
n CO2 = n CaCO3 = 5/100 = 0,05(mol)
$CO + O_{oxit} \to CO_2$
n O(oxit) = n CO2 = 0,05(mol)
CTHH của oxit : RxOy
=> n oxit = 0,05/y (mol)
=> (Rx + 16y).0,05/y = 4
<=> Rx = 64y
Với x = y = 1 thì R = 64(Cu)
Vậy oxit là CuO
b)
X gồm CO(a mol) và CO2(0,05 mol)
M X = 19.2 = 38
=> 28a + 0,05.44 = (a + 0,05).38
<=> a = 0,03
n CO = n CO2 + n CO dư = 0,08(mol)
=> V = 0,08.22,4 = 1,792 lít
%m CO = 0,03.28/(0,03.28 + 0,05.44) .100% = 27,63%
%m CO2 = 100% -27,63% = 72,37%
\(n_{CaCO_3}=\dfrac{5}{100}=0.05\left(mol\right)\)
\(n_{CO_2}=0.05\left(mol\right)\)
\(n_{CO}=a\left(mol\right)\)
\(\overline{M}=\dfrac{28a+0.05\cdot44}{a+0.05}=19\cdot2=38\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow x=0.03\)
\(M_xO_y+yCO\underrightarrow{^{t^0}}xM+yCO_2\)
\(\dfrac{0.05}{y}.................0.05\)
\(M=\dfrac{4}{\dfrac{0.05}{y}}=80y\)
\(\Leftrightarrow xM+16y=80y\)
\(\Leftrightarrow xM=64y\)
\(x=y=1,M=64\)
\(CT:CuO\)
\(V_{CO}=\left(0.05+0.03\right)\cdot22.4=1.792\left(l\right)\)
\(\%m_{CO}=\dfrac{0.03\cdot28}{0.03\cdot28+0.05\cdot44}\cdot100\%=27.63\%\)
\(\%m_{CO_2}=72.37\%\)
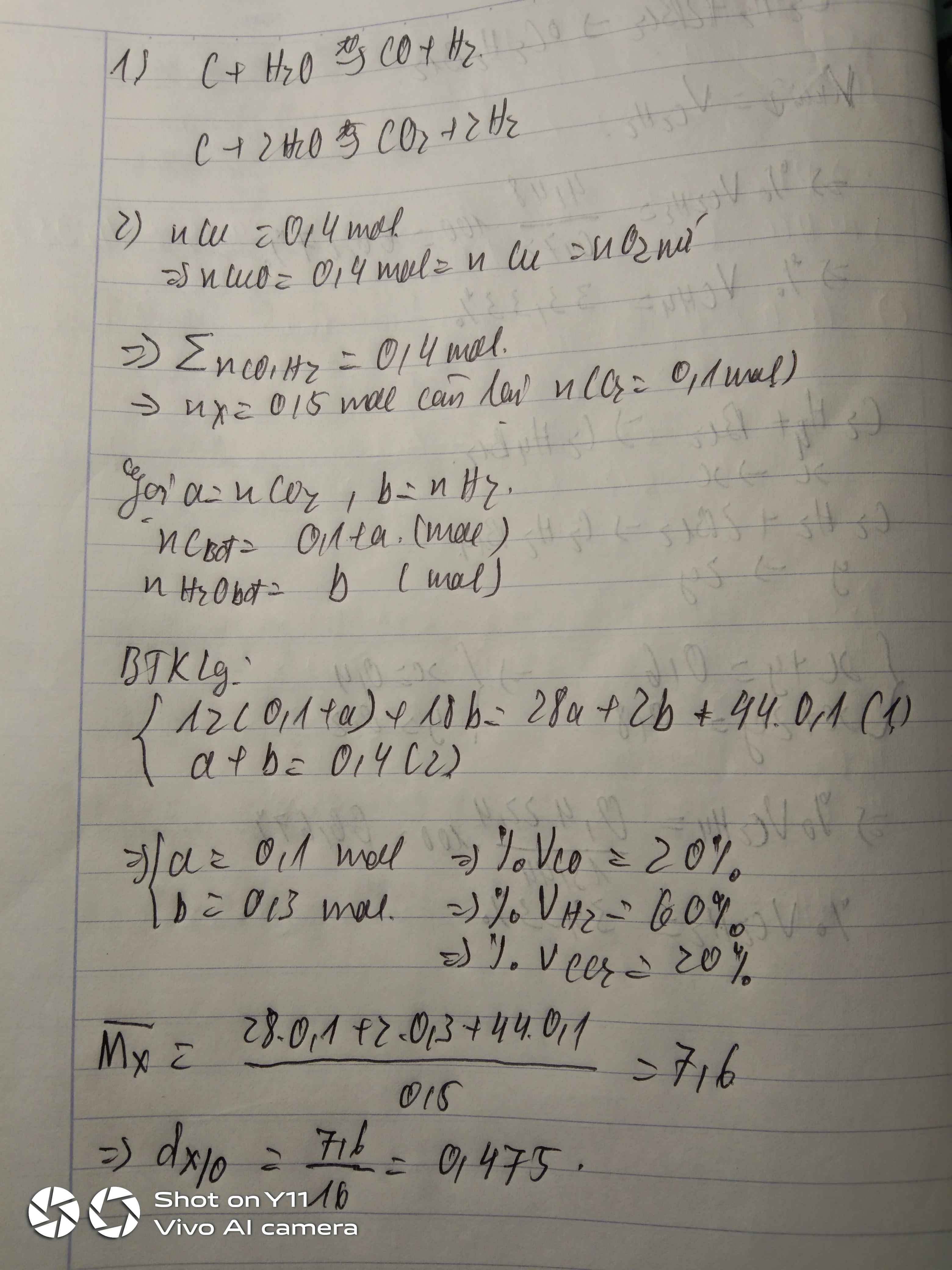
1)
\(C+H_2O\underrightarrow{t^O}CO+H_2\) (1)
\(C+2H_2O\underrightarrow{t^o}CO_2+2H_2\) (2)
2)
Gọi số mol CO, CO2 là a, b (mol)
\(n_{H_2\left(1\right)}=n_{CO}=a\left(mol\right)\)
\(n_{H_2\left(2\right)}=2b\left(mol\right)\)
=> \(n_{H_2}=a+2b\left(mol\right)\)
=> a + b + (a+2b) = \(\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
=> 2a + 3b = 0,5
PTHH: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(CuO+CO\underrightarrow{t^o}Cu+CO_2\)
=> \(n_{H_2}+n_{CO}=n_{Cu}=\dfrac{25,6}{64}=0,4\)
=> (a + 2b) + a = 0,4
=> 2a + 2b = 0,4
=> a = 0,1 ; b = 0,1
=> X chứa \(\left\{{}\begin{matrix}CO:0,1\left(mol\right)\\CO_2:0,1\left(mol\right)\\H_2:0,3\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,1}{0,5}.100\%=20\%\\\%V_{CO_2}=\dfrac{0,1}{0,5}.100\%=20\%\\\%V_{H_2}=\dfrac{0,3}{0,5}.100\%=60\%\end{matrix}\right.\)
\(\overline{M}_X=\dfrac{0,1.28+0,1.44+0,3.2}{0,5}=15,6\left(g/mol\right)\)
=> \(d_{X/O_2}=\dfrac{15,6}{32}=0,4875\)
u là trời cảm ơn bạn nha