Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

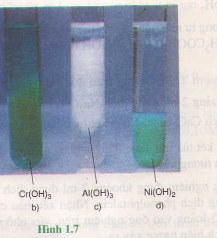
Cr(NO3)3 + 3NaOH(vừa đủ) → Cr(OH)3↓ + 3NaNO3 ;
AlCl3 + 3KOH (vừa đủ) → Al(OH)3↓ + 3KC1 ;
Ni(NO3)2 + 2NaOH → Ni(OH)2↓+ 2NaNO3.
nhìn cái ảnh này là thể hiện tự đăng rồi. Bữa trước môn sinh cũng thế chứ đâu

Đáp án C
Ba(HCO3)2 + NaHSO4® BaSO4 ↓+ NaHCO3 + CO2 ↑+ H2O
Vậy sau phản ứng, trong dung dịch còn lại các ion Na+ và HCO3-.

dùng bảo toàn nguyên tố nha cậu
xong tính khối lượng muối = khối lượng kim loại+ khối lượng gốc axit
1.
nh+ =0,8 *2 =1,6 suy ra nhcl =ncl- =1,6 suy ra m = 12 +1,6 * 35,5 =68,8
2.
nh+ =1,4 * 10-3
gọi nhcl = 2x nh2so4 = x
áp dụng định luận bảo toàn nguyên tố ta có: 2x+x = 1,4*10-3 suy ra x=0,005
suy ra m = 18,2 + 0,005 *2 *35,5 +0,005*96 = 19,035
CHÚC BẠN THÀNH CÔNG

Dùng dd AgNO3/NH3 nhận biết đc C2H2 do tạo kt vàng C2Ag2
C2H2 +2AgNO3 +2NH3 =>C2Ag2 + 2NH4NO3
Dùng dd Br2 C2H4 làm dd Br2 nhạt màu
C2H4 +Br2 =>C2H4Br2
C2H6 ko hien tuong
dẫn các khí đi qua dung dịch \(AgNO_3\)/\(NH_3\)
khí nào bị giữ lại , tạo kết tủa vàng là \(C_2H_2\)
\(C_2H_2+2\left(Ag\left(NH_3\right)_2\right)OH->C_2Ag_2+4NH_3+2H_2O\)
dẫn 2 khí còn lại đi qua dung dịch \(Br_2\)
khí nào làm mất màu dung dịch \(Br_2\) là \(C_2H_4\)
\(C_2H_4+Br_2->C_2H_4Br_2\)
khí nào không làm mất màu dung dịch \(Br_2\) là \(C_2H_6\)

Đáp án C