Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

300ml = 0,3l
\(n_{HNO3}=1.0,3=0,3\left(mol\right)\)
Pt : \(NaOH+HNO_3\rightarrow NaNO_3+H_2O|\)
1 1 1 1
0,3 0,3 0,3
\(n_{NaOH}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
200ml = 0,2l
\(C_{M_{NaOH}}=\dfrac{0,3}{0,2}=1,5\left(M\right)\)
\(n_{NaNO3}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
⇒ \(m_{NaNO3}=0,3.85=25,5\left(g\right)\)
Sau phản ứng :
\(V_{dd}=0,2+0,3=0,5\left(l\right)\)
\(C_{M_{NaNO3}}=\dfrac{0,3}{0,5}=0,6\left(M\right)\)
Chúc bạn học tốt
\(n_{HNO_3}=0,3\left(mol\right)\)
\(NaOH+HNO_3\rightarrow NaNO_3+H_2O\)
Theo PT: \(n_{NaOH}=n_{NaNO_3}=n_{HNO_3}=0,3\left(mol\right)\)
\(\Rightarrow CM_{NaOH}=\dfrac{0,3}{0,2}=1,5M\)
\(m_{NaNO_3}=0,3.85=25,5\left(g\right)\)

\(n_{H_2SO_4}=0,4\cdot1=0,4mol\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+H_2O\)
0,8 0,4
\(V_{NaOH}=\dfrac{0,8}{0,5}=1,6l\)

nMg = 3,6/24 = 0,15 mol; nFeCl3 = 0,25.1 = 0,25 mol
Mg + 2FeCl3 → MgCl2 + 2FeCl2
0,125dư 0,025←0,25 → 0,125 → 0,25 (mol)
Mg + FeCl2 → MgCl2 + Fe
0,025→0,025 →0,025→0,025 (mol)
Vậy chất rắn sau phản ứng là Fe: nFe = 0,025 mol
=> m = mFe = 0,025.56 = 1,4 (gam)
Dung dịch X sau phản ứng gồm:
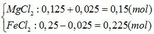
Nồng độ của các chất trong dung dịch X:
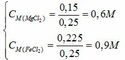

a) \(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: CO2 + 2NaOH → Na2CO3 + H2O
Mol: 0,15 0,3 0,15
\(C_{M_{ddNaOH}}=\dfrac{0,3}{0,2}=1,5M\)
b) Na2CO3: natri cacbonat
\(m_{Na_2CO_3}=0,15.106=15,9\left(g\right)\)
c)
PTHH: 2NaOH + H2SO4 → Na2SO4 + 2H2O
Mol: 0,15 0,075
\(V_{ddH_2SO_4}=\dfrac{0,075}{1}=0,075\left(l\right)=75\left(ml\right)\)

Ta có nH2SO4 = 0,2 . 1,5 = 0,3 ( mol )
nBa(OH)2 = 0,3 . 0,8 = 0,24 ( mol )
H2SO4 + Ba(OH)2 → BaSO4 + 2H2O
0,3...........0,24
⇒Lập tỉ số 0,3/1:0,24/1 = 0,3 > 0,24
⇒Sau phản ứng H2SO4 dư , Ba(OH)2 hết
⇒mBaSO4 = 0,24 . 233 = 55,92 ( gam )
⇒nH2SO4 dư = 0,3 - 0,24 = 0,06 ( mol )
⇒CM H2SO4 dư = 0,06 : 0,5 = 0,12 M

\(nBaCl_2=\dfrac{70}{1000}.1=0,07mol\)
\(C_{MBaCl_2}=\dfrac{0,07}{0,07}=1M\)