Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

MgCO3 + 2HCl → MgCl2 + CO2 + H2O (1)
BaCO3 + 2HCl → BaCl2 + CO2 + H2O (2)
CO2 + Ca(OH)2 → CaCO3↓ + H2O. (3)
Theo (1), (2) và (3), để lượng kết tủa B thu được là lớn nhất thì:
nCO2 = nMgCO3 + nBaCO3 = 0,2 mol
Ta có:  = 0,2
= 0,2
=> a = 29,89.

Số mol H3PO4: 0,050 x 0,50 = 0,025 (mol).
H3PO4 + 3NaOH → Na3PO4 + 3H2O
1 mol 3 mol
0,025 mol 3 x 0,025 mol
Thể tích dung dịch NaOH: 0,075 lít hay 75 ml

Đáp án A
Ta có nH+=0.02, nOH-=0.04 nên sau phản ứng nOH- = 0,02 và V = 0,2
→ Cm OH- = 0,1 => pH = 1

Chọn A
Ta có nH2SO4 = 0,05.0,1 = 0,005 mol; nHCl = 0,1.0,1 = 0,01 mol
⇒ ∑nH+ = 2nH2SO4 + nHCl = 2.0,005 + 0,01 = 0,02 mol
nNaOH = 0,2.0,1 = 0,02 mol; nBa(OH)2 = 0,1.0,1 = 0,01 mol
⇒ ∑nOH- = nNaOH + 2nBa(OH)2 = 0,02 + 2.0,01 = 0,04 mol
Khi trộn axit với kiềm thì bản chất của phản ứng là:
H+ + OH- → H2O
(0,02) (0,04)
⇒ nOH-còn dư = 0,04 – 0,02 = 0,02 mol ⇒ [OH-] còn dư = 0,02/0,2 = 0,1M
⇒ Dung dịch X có pOH = - lg[OH-]còn dư = 1 ⇒ pH = 14 – 1 = 13

C2H2 + 2AgNO3 + 2NH3 → C2Ag2 ↓ + 2NH4NO3
CH3CHO + 2AgNO3 + 3NH3 + H2O → CH3COONH4 + 2Ag ↓ + 2NH4NO3
C2Ag2 + 2HCl → 2AgCl ↓ + C2H2 ↑
Y(AgCl, Ag) + HNO3 --> ...
Ag + 2HNO3 → AgNO3 + NO2 ↑ + H2O
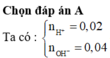
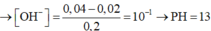

Chọn A
∑ nH+ = 2nH2SO4 + nHCl = 2. 0,1.0,05 + 0,1.0,1 = 0,02 (mol)
∑ nOH- = nNaOH + 2nBa(OH)2 = 0,1.0,2 + 2. 0,1.0,1 = 0,04 (mol)
H+ + OH- → H2O
0,02 → 0,02
=> nOH- dư = 0,04 – 0,02 = 0,02 (mol)
=> [OH-] = n: V = 0,02 : 0,2 = 0,01 M
pH = 14 + log(OH-) = 14 + (-1) = 13