
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\([H^{+}]=0,004+0,0008.2=0,0056M\\ pH=-log(0,0056)=2,25\)

a) pH= -log[H+]= -log[0,1]=1
b) pH= 14- p[OH-]= 14+log[0,1]=13
Bạn ơi bạn có thể cho mình hỏi là pH=14-p(OH-) mà số 14 đó ở đâu ra được hem

Đáp án C
Gọi x là số mol của Ca(OH)2
n H C O 3 - = 2 n C a 2 + + 2 n M g 2 + = 0 , 014
Đầu tiên ta có phản ứng:
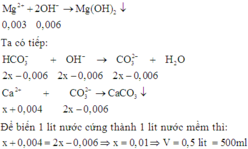

a) \(\left[H^+\right]=0,01.2=0,02M\)
=> pH = 1,7
b) \(\left[OH^-\right]=0,03.2=0,06M\)
=> pOH= 1,22
=> \(pH=14-1,22=12,78\)
a) pH= -log[H+]= -log[0,01.2]=1,69
b) pH= 14 - pOH= 14 + log[OH-]= 14+ log[0,03.2]=12,78


\(\left\{{}\begin{matrix}n_{HCl}=0,12\left(mol\right)\\n_{Ca\left(OH\right)_2}=0,05\left(mol\right)\end{matrix}\right.\)
\(HCl\left(0,12\right)\rightarrow H^+\left(0,12\right)+Cl^-\)
\(Ca\left(OH\right)_2\left(0,05\right)\rightarrow Ca^{2+}+2OH^-\left(0,1\right)\)
\(\Rightarrow n_{H^+}\left(dư\right)=0,02\left(mol\right)\)
\(\Rightarrow\left[H^+\right]=0,1\left(M\right)\)
\(\Rightarrow pH=1\)
\([OH^-]=0,004.2=0,008M \\ pOH=-log(0,008) \approx 2,1 \\ \Rightarrow pH=14-2,1=11,9\)