
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{H_3PO_4}=0,6.2=1,2\left(mol\right)\Rightarrow m_{H_3PO_4}=1,2.98=117,6\left(g\right)\)
mdd sau khi pha = 600.1,2+200.1,1 = 940 (g)
\(C\%_{ddH_3PO_4}=\dfrac{117,6.100\%}{940}=12,51\%\)
Cái 200ml dd H3PO4 có D=1,1g/ml thì cái đó có cho CM không? hay số mol gì đó

có công thức liên hệ giữa nồng độ mol(CM) và nồng độ %(C%) và khối lượng riêng(D) : CM=C%\(\frac{10\cdot D}{Mct}\) đó là dấu nhân nha bạn
Chúc bạn học tốt

\(n_{NaOH}=0,2.1=0,2\left(mol\right)\\ n_{H_2SO_4}=0,3.1,5=0,45\left(mol\right)\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
0,2------->0,1--------->0,1
Xét \(\dfrac{0,2}{2}< \dfrac{0,45}{1}\Rightarrow\) \(H_2SO_4\)dư
Trong dung dịch D có:
\(\left\{{}\begin{matrix}n_{H_2SO_4}=0,45-0,1=0,35\left(mol\right)\\n_{Na_2SO_4}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}CM_{H_2SO_4}=\dfrac{0,35}{0,5}=0,7M\\CM_{Na_2SO_4}=\dfrac{0,1}{0,5}=0,2M\end{matrix}\right.\)
b
\(Ca\left(OH\right)_2+H_2SO_4\rightarrow CaSO_4+2H_2O\)
0,35<---------0,35
\(V_{Ca\left(OH\right)_2}=\dfrac{0,35.74}{1,2}=\dfrac{259}{12}\approx21,58\left(ml\right)\\ \Rightarrow V_{dd.Ca\left(OH\right)_2}=\dfrac{\dfrac{259}{12}.100\%}{10\%}=\dfrac{1295}{6}\approx215,83\left(ml\right)\)

\(V_{ddH2SO4\left(5M\right)}=\dfrac{200}{1,29}=155\left(ml\right)\)
V dd H2SO4 nhận được = 0,15 + 0,155 = 0,305 lít
\(n_{H2SO4\left(2M\right)}=0,3\left(mol\right)\)
\(n_{H2SO4\left(5M\right)}=0,775\left(mol\right)\)
=> CM dd H2SO4 nhận được = \(\dfrac{0,3+0,775}{0,305}=3,525M\)

\(n_{Fe}=\dfrac{1,12}{56}=0,02(ml)\\n_{CuSO_4}=0,2.0,1=0,02(mol)\\ m_{dd_{CuSO_4}}=1,2.200=240(g)\\ a,PTHH:Fe+CuSO_4\to FeSO_4+Cu\\ LTL:\dfrac{0,02}{1}=\dfrac{0,02}{1}\Rightarrow \text{p/ứ hoàn toàn}\\ \Rightarrow n_{FeSO_4}=n_{Cu}=0,02(mol)\\ b,C\%_{FeSO_4}=\dfrac{0,02.152}{1,12+240-0,02.64}.100\%=1,27\%\\ C_{M_{FeSO_4}}=\dfrac{0,02}{0,2}=0,1M\)
Chọn đáp án A
NST số 1 giảm phân tạo giao tử: 1/2 bình thường, 1/2 đột biến
Các NST khác giảm phân bình thường tạo giao tử bình thường
→ Một thể đột biến trong đó cặp NST số 1 có 1 chiếc bị mất đoạn, khi giảm phân nếu các NST phân li bình thường thì trong số các loại giao tử được tạo ra giao tử không mang NST đột biến có tỉ lệ: ½

Chọn D
Gọi số mol của FeO và CuO lần lượt là x và y mol
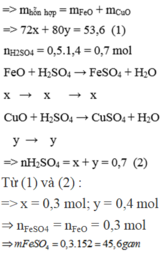
Ta có: m d d H 2 S O 4 = D . V = 1 , 2 . 500 = 600 g a m
Vì phản ứng không tạo ra chất khí hay kết tủa nên:
m d d s a u p ư = m t r ư ớ c p ư = m h h A + m d d a x i t = 53 , 6 + 600 = 653 , 6 g a m .
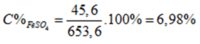

PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
a_______a________a______a (mol)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\)
b_______\(\dfrac{3}{2}\)b_________\(\dfrac{1}{2}\)b_____\(\dfrac{3}{2}\)b (mol)
a) Ta lập HPT: \(\left\{{}\begin{matrix}24a+27b=8,25\\a+\dfrac{3}{2}b=\dfrac{2,24}{22,4}=0,1\end{matrix}\right.\) \(\Leftrightarrow\) Hệ có nghiệm âm
*Bạn xem lại đề !!!

\(n_K=\dfrac{7,8}{39}=0,2\left(mol\right)\)
Pt : \(2K+2H_2O\rightarrow2KOH+H_2|\)
2 2 2 1
0,2 0,2
a) \(n_{KOH}=\dfrac{0,2.2}{2}=0,2\left(mol\right)\)
\(C_{M_{ddKOH}}=\dfrac{0,2}{0,5}=0,4\left(l\right)\)
b) Pt : \(HCl+KOH\rightarrow KCl+H_2O|\)
1 1 1 1
0,2 0,2
\(n_{HCl}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
\(m_{ddHCl}=\dfrac{7,3.100}{15}\simeq48,67\left(g\right)\)
\(V_{ddHCl}=\dfrac{48,67}{1,2}=40,56\left(ml\right)\)
Chúc bạn học tốt
Thiếu đề nhé.