K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Các câu hỏi dưới đây có thể giống với câu hỏi trên
NH
1

16 tháng 8 2019
Đáp án C
H+ + OH– → H2O || Trung hòa ⇒ nOH– = nH+ = 0,01 mol.
⇒ x = 0,01 ÷ 0,05 = 0,2M

30 tháng 3 2017
Đáp án B
H2C2O4 là axit oxalic.
H2C2O4 + 2NaOH → Na2C2O4 + 2 H2O (1)
nH2C2O4 = 25/1000.0,05 = 0,00125(mol)
Theo (1): nNaOH = 0,00125.2 = 0,0025(mol)
Nông độ mol của NaOH là: 0,0025/0,0465 = 0,05376(M)
NH
1

27 tháng 9 2017
Chọn đáp án A
Trung hòa: H+ + OH– → H2O ||⇒ nOH– = nH+ = 0,002 mol
⇒ x = 0,002 ÷ 0,01 = 0,2M ⇒ chọn A.
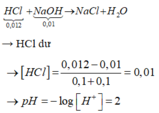
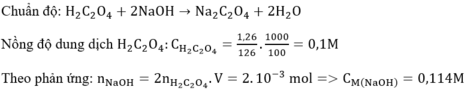
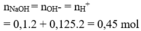
H trong pha loãng
Đề bài:
Tính K và điều chỉnh nồng độ dung dịch NaOH trong pha loãng.
Giải thích:
\(C_{1} V_{1} = C_{2} V_{2}\)
Trong đó:
Cách tính hệ số pha loãng K:
\(K = \frac{C_{1}}{C_{2}} = \frac{V_{2}}{V_{1}}\)
Ví dụ:
Có 100 ml NaOH 1M, muốn pha thành dung dịch 0,2M:
\(K = \frac{1}{0 , 2} = 5\)\(V_{2} = K \cdot V_{1} = 5 \times 100 = 500 \&\text{nbsp};\text{ml}\)
=> Thêm 400 ml nước vào dung dịch ban đầu.
Kết luận:
Nếu bạn cần giải chi tiết với số liệu cụ thể, vui lòng cung cấp thêm dữ kiện!