Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
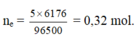
Fe + dung dịch sau điện phân → sinh khí NO
⇒ dung dịch sau điện phân chứa H+⇒ Cl– bị điện phân hết.
► Quy đổi sản phẩm điện phân về CuO và CuCl2 với số mol x và y.
ne = 2x + 2y = 0,32 mol; mdung dịch giảm = 80x + 135y = 15(g).
||⇒ giải hệ có: x = 0,12 mol; y = 0,04 mol ⇒ nKCl = nCl– = 2y = 0,08 mol.
⇒ nCu2+ = nCu(NO3)2 = 0,08 × 3 = 0,24 mol ⇒ nCu2+/dung dịch = 0,08 mol.
nO2 = 0,5x = 0,06 mol ⇒ nH+ = 0,06 × 4 = 0,24 mol.
► 4H+ + NO3– + 3e → NO + 2H2O || Cu2+ + 2e → Cu.
ne nhận tối đa = 3/4nH+ + 2nCu2+ = 0,34 mol < ne cho tối thiểu = 2nFe = 0,5 mol.
||⇒ Fe dư ⇒ Fe chỉ lên số oxi hóa +2 ⇒ nFe phản ứng = 0,34 ÷ 2 = 0,17 mol.
► Hỗn hợp rắn gồm 0,08 mol Fe và 0,08 mol Cu ⇒ m = 9,6(g).

Đáp án B
ne = 5 x 6176 / 96500 = 0,32 mol. Fe+ dung dịch sau điện phân → sinh khí NO
⇒ dung dịch sau điện phân chứa H+ ⇒ Cl– bị điện phân hết.
► Quy đổi sản phẩm điện phân về CuO và CuCl2 với số mol x và y.
ne = 2x + 2y = 0,32 mol; mdung dịch giảm = 80x + 135y = 15(g).
⇒ giải hệ có: x = 0,12 mol; y = 0,04 mol ⇒ nKCl = nCl– = 2y = 0,08 mol.
⇒ nCu2+ = nCu(NO3)2 = 0,08 × 3 = 0,24 mol ⇒ nCu2+/dung dịch = 0,08 mol.
nO2 = 0,5x = 0,06 mol ⇒ nH+ = 0,06 × 4 = 0,24 mol.
► 4H+ + NO3– + 3e → NO + 2H2O
Cu2+ + 2e → Cu.
ne nhận tối đa = 3/4nH+ + 2nCu2+ = 0,34 mol < ne cho tối thiểu = 2nFe = 0,5 mol.
⇒ Fe dư ⇒ Fe chỉ lên số oxi hóa +2 ⇒ nFe phản ứng = 0,34 ÷ 2 = 0,17 mol.
► Hỗn hợp rắn gồm 0,08 mol Fe và 0,08 mol Cu ⇒ m = 9,6(g)

Chọn đáp án B.
Dung dịch điện phân chứa 3x mol Cu(NO3)2 và x mol KCl.
Áp dụng định luật điện phân Faraday, ta có ne trao đổi = It : 96500 = 0,32 mol.
Dung dịch điện phân ra x mol CuCl2 và y mol CuO. Ta có: 2x + 2y = 0,32 mol và 135x + 80y = 15 gam
Giải hệ được x = 0,04 mol và y = 0,12 mol
→ dung dịch sau điện phân có Cu(NO3)2; KNO3 và HNO3.
Bảo toàn nguyên tố H có nH2O = 0,12 mol → bảo toàn nguyên tố O có nNO = 0,06 mol.
Tiếp tục bảo toàn N suy ra số mol Fe(NO3)2 là 0,17 mol. Bảo toàn khối lượng kim loại ta có:0,25 x 56 + 0,08 x 64 = 0,17 x 56 + m → m = 9,6 gam

Đáp án B
Dung dịch điện phân chứa 3x mol Cu(NO3)2 và x mol KCl.
Áp dụng định luật điện phân Faraday, ta có ne trao đổi = It ¸ 96500 = 0,32 mol.
Dung dịch điện phân ra x mol CuCl2 và y mol CuO. Ta có: 2x + 2y = 0,32 mol và 135x + 80y = 15 gam.
Giải hệ được x = 0,04 mol và y = 0,12 mol.
® dung dịch sau điện phân có Cu(NO3)2; KNO3 và HNO3.
Bảo toàn nguyên tố H có nH2O = 0,12 mol ® bảo toàn nguyên tố O có nNO = 0,06 mol.
Tiếp tục bảo toàn N suy ra số mol Fe(NO3)2 là 0,17 mol. Bảo toàn khối lượng kim loại ta có: 0,25 x 56 + 0,08 x 64 = 0,17 x 56 + m →m = 9,6 gam

Đáp án C
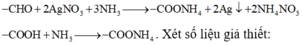
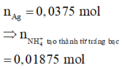
M à ∑ g ố c m u ố i N H 4 + n = 0 , 02 m o l ⇒ n N H 4 + t ạ o t h à n h t ừ a x i t = 0 , 02 - 0 , 01875 = 0 , 00125 m o l
So sánh khối lượng của X và muối amoni (CHO với COONH4; COOH với COONH4)
Khối lượng tăng từ phản ứng tráng bạc = 0,01875*(62-29) = 0,61875 gam
Khối lượng tăng từ axit = 0,00125*(62-45) = 0,02125 gam.
Theo đó, giá trị m = 1,86 - ( 0,61875- 0,02125) = 1,22 gam




Đáp án B