Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(d_{\dfrac{B}{O_2}}=0,5\\ \Leftrightarrow\dfrac{M_B}{M_{O_2}}=0,5\\ \Rightarrow M_B=M_{O_2}.0,5=32.0,5=16\left(\dfrac{g}{mol}\right)\\ d_{\dfrac{A}{B}}=2,125\\ \Leftrightarrow\dfrac{M_A}{M_B}=2,125\\ \Rightarrow M_A=2,125.M_B=2,125.16=34\left(\dfrac{g}{mol}\right)\)
Em coi xem có chỗ nào không hiểu hỏi lại nha!

\(d_{B/O_2}=\dfrac{M_B}{M_{O_2}}=\dfrac{M_B}{32}=0,5=>M_B=0,5.32=16\)
\(d_{A/B}=\dfrac{M_A}{M_B}=\dfrac{M_A}{M_B}=\dfrac{M_A}{16}=2,125=>M_A=2,125.16=34\)
Chúc bạn học tốt

a) Có 2R+(96x3)=342
Suy ra: R=27 là nhôm(Al)
b) MB=32x0,5=16
Suy ra: MA=16x2,125=34
Ta có : HuSv
5,88%=100u/34 =>u=2
94,12%=32 x 100 x v/34 => v=1
Vậy công thức hoá học của A là: H2S
Chúc bạn học tốt!

\(d_{B\text{/}O_2}=0.5\Rightarrow M_B=32\cdot0.5=16\left(\text{g/mol}\right)\)
\(d_{A\text{/}B}=2.125\Rightarrow M_A=2.125\cdot M_B=2.125\cdot16=34\left(g\text{/}mol\right)\)
Các yếu tố làm thay đổi tốc độ phản ứng : nồng độ, nhiệt độ, áp suất, diện tích bề mặt tiếp xúc, chất xúc tác.

Ta có: \(d_{B/O_2}=\dfrac{M_B}{M_{O_2}}=0,25\Rightarrow M_B=0,25.32=8\left(g/mol\right)\)
\(d_{A/B}=\dfrac{M_A}{M_B}=2,5\Rightarrow M_A=2,5.M_B=20\left(g/mol\right)\)

a/ => MX = 22 x 2 = 44 (g/mol)
b) dX/KK= \(\frac{44}{29}\) =1,52
=> Khí X nặng hơn không khí 1,52 lần
a) MX= 2 . 22 = 44 g/mol
b) dX/kk = \(\frac{44}{29}\approx1,517\)
=> Tỉ khối khí X lớn hơn tỉ khối của không khí là 1,517 lần
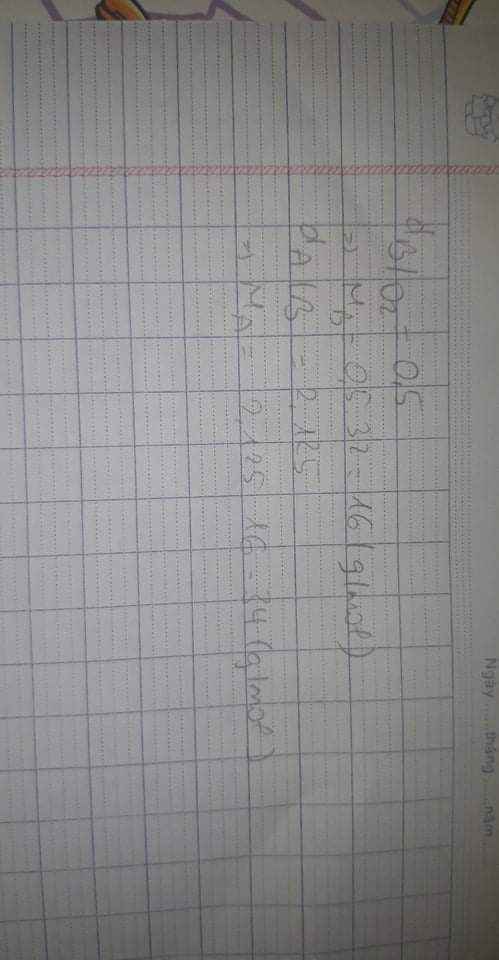
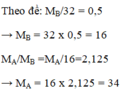
-khối lượng mol của khí B là:
\(\dfrac{MB}{MO2}\)=0,5.
=>MB=0,5*32=16.
-khối lượng mol trung bình của khí A là:
\(\dfrac{MA}{MB}\)=2,125.
=>\(\dfrac{MA}{16}\)=2,125.
=>MA=2,125*16=34.
chào bạn mình gặp được bạn sau 8 năm...;J