Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
n C r 2 O 3 = 0 , 03 m o l
Cho toàn bộ X tác dụng với HCl loãng nóng thu được 0,12 mol H2.
Ta thấy 0,12 > n C r =0,06 do vậy Al dư
Vậy X chứa Cr 0,06 mol, Al2O3 0,03 mol và Al dư
→ n A l = 0 , 12 - 0 , 06 1 , 5 = 0 , 04 m o l
X tác dụng với lượng dư NaOH → n N a O H = 0 , 03 . 2 + 0 , 04 = 0 , 1 m o l

PTPU:
C2H2 + 2H2 \(\rightarrow\) C2H6
x \(\rightarrow\) 2x \(\rightarrow\) x
C2H2 + H2 \(\rightarrow\) C2H4
y \(\rightarrow\) y \(\rightarrow\) y
Gọi x, y lần lượt là số mol của C2H2 tham gia phản ứng.
\(n_{\text{kết tủa}}\) = 24/240 = 0,1 mol => \(n_{C_2H_2\left(dư\right)}\) = 0,1 mol
Vì ta thấy rằng tỉ khối hơi của X so với H2 bằng 8, từ đây ta biết được một điều là H2 dư sau phản ứng.
Vậy sau phản ứng ta có hỗn hợp khí X gồm:
C2H2 (dư) = 0,1 mol
H2 (dư) = 0,65 – (2x + y)
C2H4 = y mol
C2H6 = x mol
hỗn hợp khí X có tỉ khối so với H2 bằng 8. Ta có phương trình:
[26 . 0,1 + (0,65 – 2x – y) .2 + 30.x + 28.y]/(0,1 + 0,65 – 2.x – y + x +y) = 8.2 = 16
\(\Rightarrow\) 42x + 26y = 8,1 (1)
Mà ta lại có phương trình
x + y = 0,35 – 0,1 = 0,25 ( số mol C2H2 tham gia phương trình phản ứng) (2)
Từ (1) và (2) ta có hệ phương trình:
\(\Rightarrow\) x = 0,1 mol
y = 0,15 mol
Sau phản ứng hỗn hợp khí Y gồm C2H6 (0,1 mol) và C2H4 (0,15 mol)
Vậy sẽ có 0,15 mol Br2 tham gia phản ứng.

Chọn A
nH+ = 12nN2 + 10nNH4+ + 2nO (oxit) ⇒ nNH4+ = 0,05
Trong dung dịch Y có a mol Mg2+; b mol Fe3+; c mol Fe2+
⇒ nKOH = 2a + 3b + 2c + nNH4+ = 3,15 ⇒ 2a + 3b + 2c = 3,1 (1)
Sau khi tác dụng với KOH thì phần dung dịch chứa 3,15 mol K+; 1,54 mol SO42- và nNO3- = 0,07
Bảo toàn N ⇒ nNO3- ban đầu = 2nN2 + nNH4+ + nNO3- (trong Y) = 0,2
⇒ mX = 24a + 56(b + c) + 62.0,2 + 1,05.16 = 86 (2)
Bảo toàn ne ⇒ 3nAl phản ứng = 3nFe3+ + 2nFe2+ ⇒ nAl phản ứng = b + 2c/3
⇒ mtăng = 56(b + c) – 27(b + 2c/3) = 28 (3)
(1), (2), (3) ⇒ a = 0,15; b = 0,9; c = 0,05
Oxit thu được gồm MgO (0,15 mol) và Fe2O3 (0,95/2 = 0,475) ⇒ m = 0,15.40 + 0,475.160 = 82



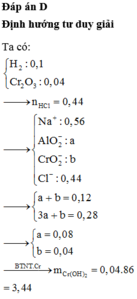
Đáp án D
Ta có:
→ n H 2 = n C r = 0 , 03 m o l < n H 2 (đề bài) = 0,045 mol
→ Chứng tỏ Y phải có Al dư và 0,06 mol Cr.
Như vậy Y A l : 0 , 01 m o l A l 2 O 3 : 0 , 015 m o l C r : 0 , 03 m o l → n N a O H = 0 , 04 m o l
Chú ý: Cr không phản ứng với NaOH kể cả NaOH đặc nóng